Clear Sky Science · zh
依赖 Tbr2 的平行通路调控不同 ipRGC 亚型的发展
我们的眼睛如何报告时间与形状
除了形成影像外,我们的眼睛还在默默地保持生物钟节律、控制瞳孔开合,并帮助感知整体亮度。一小群特殊的视网膜神经元,称为内在光敏性视网膜神经节细胞(ipRGCs),承担了许多这些功能。它们通过一种称为黑色素视紫红质的色素响应光,并将信号传入大脑深处。本研究提出了一个基础却意义重大的问题:一群早期发育的神经细胞如何分化为若干不同的 ipRGC 类型,每一种又如何为不同的任务接线?
一个主开关,生成多种感光细胞类型
在小鼠视网膜中,已知的六种 ipRGC 亚型均来源于一群在早期激活基因 Tbr2 的神经节细胞。该基因像一个主开关,开启形成 ipRGC 所需的发育程序并维持黑色素视紫红质基因 Opn4 的活性。但单一主开关无法解释六种不同 ipRGC 如何产生——它们在形态、光响应和投射目标上各不相同。作者通过对发育中小鼠视网膜进行 RNA 测序,寻找依赖 Tbr2 的基因。在一小组候选基因中,两种基因脱颖而出:Irx1 和 Tbx20,它们在身体其他部位已知参与细胞身份的调控。 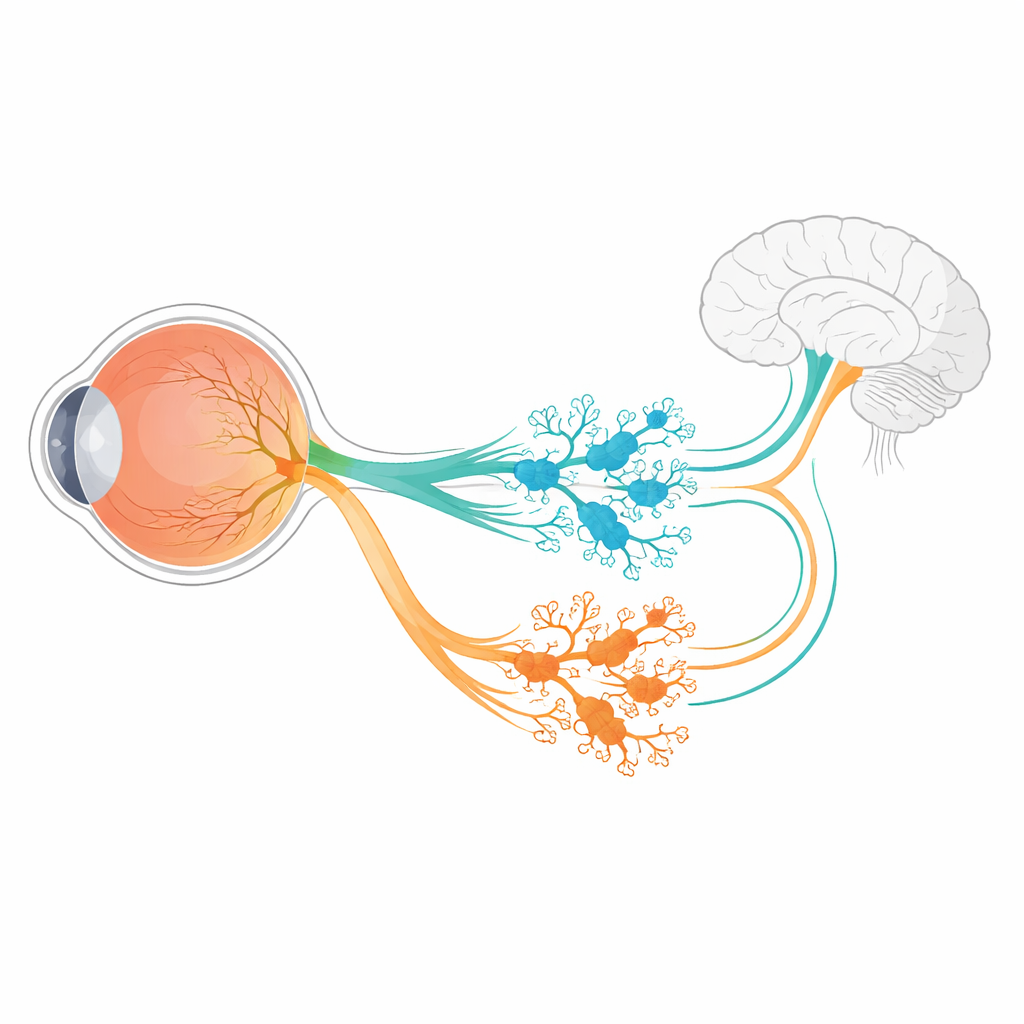
视网膜内的两条分化路径
研究者利用新构建的小鼠系,在产生 Irx1 和 Tbx20 的细胞上打标为荧光或酶标记,追踪这些因子何时何地被激活。他们发现 Irx1 与 Tbx20 在胚胎中期出现于重叠的年轻神经节细胞群,但到成体阶段几乎分成了互不相交的集合。Irx1 主要存在于标记为 M3、M4 和 M5 的 ipRGCs,而 Tbx20 则集中在 M1、M2 和 M6 细胞中,仅在部分 M3 和 M5 细胞中有少量重叠。精细成像、电生理记录和脑区投射追踪显示,每一种因子标记的一组 ipRGC 都具有特定的树突布局、光学响应特征以及投射到参与生物钟设定、反射和视觉处理的特定脑区的模式。
调节光敏感性与细胞存活的开关
团队接着研究删除每个因子会发生什么。去除发育中视网膜的 Irx1 后,被 Irx1 标记的 ipRGC 数量与基本结构大体保留,但它们的黑色素视紫红质水平显著下降。换言之,Irx1 对于在 M3、M4 和 M5 细胞中充分启动 Opn4 的感光程序是必要的,但对这些细胞的初期形成并非必需。Tbx20 则表现出不同的作用:删除 Tbx20 不仅降低了 Opn4 的表达,还使 Tbx20 阳性的 ipRGC 数量大约减少一半,并在随后降低了这些细胞的存活率。这表明 Tbx20 有助于构建并维持特定的 ipRGC 亚型(尤其是 M1、M2 和 M6),同时支持其基于黑色素视紫红质的光敏感性。 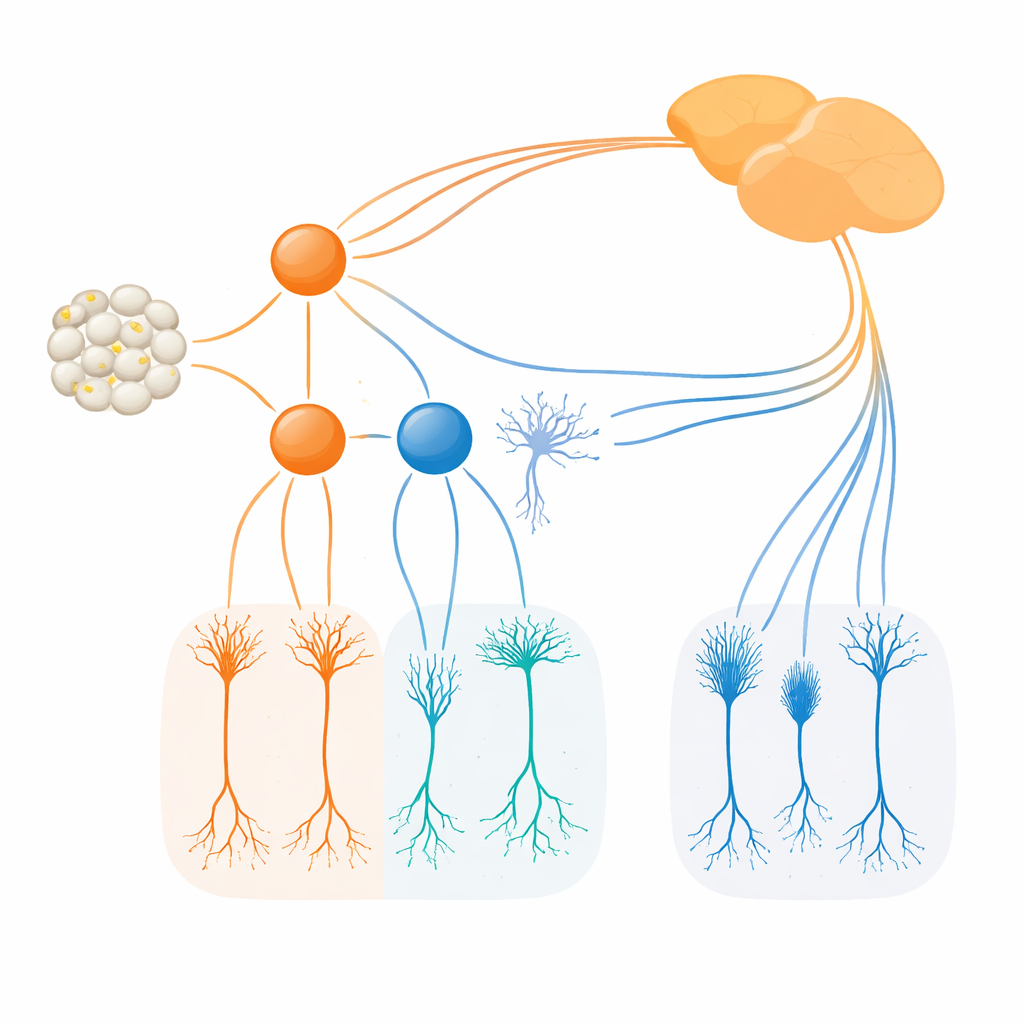
决定分化为不同细胞家族的时序
通过在精确的胚胎日短暂激活遗传报告基因,作者能够对表达 Irx1 或 Tbx20 的细胞进行“时间标记”,并追踪它们到成体的命运。这些实验显示,Tbx20 标记的细胞比 Irx1 标记的细胞略早决定其最终的 ipRGC 身份,大多数决定在出生前不久就已锁定。在一个短暂的时间窗内,部分细胞可同时共表达 Irx1 与 Tbx20,而同时缺失这两个基因的双敲除小鼠相比任一单基因突变体显示出更严重的黑色素视紫红质阳性 ipRGC 丢失。这提示两条通路在短期内协同工作,随后分化并引导不同子集的 ipRGC 沿各自的发育轨迹前行。
对视觉与健康理解的意义
对非专业读者而言,主要结论是单一早期基因 Tbr2 并非孤立发挥作用。相反,它分流到两条平行的控制通路——一条以 Irx1 为中心,另一条以 Tbx20 为中心。这些通路决定年轻细胞将成为哪种 ipRGC,调节其感光强度,并决定它是否连接到用于生物钟调节、瞳孔反射或其他视觉功能的大脑区域。这项工作为我们体内“光计”的构建提供了更清晰的接线图,并突出了在这些细胞丢失或功能受损时可能涉及的特定遗传步骤,对睡眠紊乱、季节性情绪变化以及损伤视网膜的疾病具有潜在相关性。
引用: Kiyama, T., Chen, CK., Altay, H.Y. et al. Tbr2-dependent parallel pathways regulate the development of distinct ipRGC subtypes. Commun Biol 9, 347 (2026). https://doi.org/10.1038/s42003-026-09645-4
关键词: 视网膜神经节细胞, 黑色素视紫红质, 神经发育, 昼夜节律, 转录因子