Clear Sky Science · zh
结构分析揭示水分子介导了 GPR99 的自我激活
这个受体为何与炎症有关
我们的气道和其他组织不断感知提示感染或刺激的化学信号。位于细胞表面的蛋白 GPR99 正成为哮喘和鼻息肉等炎症性疾病中的一个重要开关。本研究以原子级细节说明了 GPR99 如何在没有外来化学触发的情况下自行开启——以及微小的水分子簇如何帮助它实现这一点——为设计新的抗炎药物提供了线索。
细胞感受器内置的“开启”开关
GPR99 属于一大类将细胞外信息传递到细胞内的膜蛋白,这类蛋白常通过构象变化并招募称为 G 蛋白的伙伴来传递信号。与大多数此类受体不同,GPR99 即使在没有配体结合时也异常活跃。作者显示,位于 GPR99 外侧的一段柔性环,称为第二细胞外环,表现得像一个内部钥匙:它折叠进入通常的结合口袋,模仿激活性信号,从而使受体自发开启。
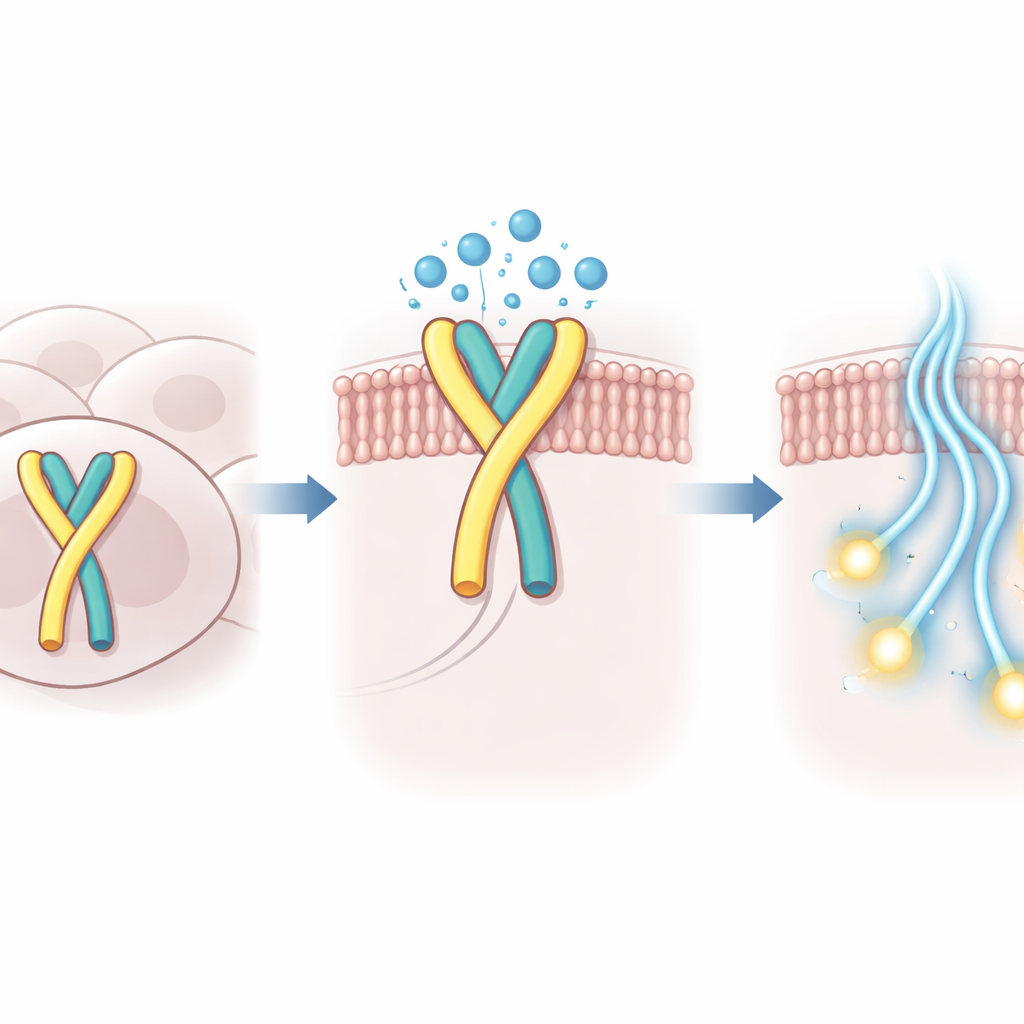
水如何帮助固定这个开关
研究人员利用高分辨率冷冻电镜捕获了人类 GPR99 与其 G 蛋白伙伴结合的自激活状态三维结构。在外来分子通常位于的结合口袋中,他们观察到不仅有折入的环,还有一小簇有序的水分子。这些水分子在环与周围蛋白之间形成极性桥梁,补偿了环较浅的插入并稳定了受体的活性构象。当将环或邻近口袋中的关键氨基酸改变,以削弱这些水介导的接触时,GPR99 在细胞实验中的内置活性显著下降。
为持续信号传导重排内部机制
研究组将他们观察到的自激活结构与家族中其他成员进行了比较,包括一个与代谢副产物琥珀酸结合的密切相关受体,以及与代谢物2‑氧戊二酸结合的 GPR99 活性构象。他们发现,缺乏外源配体的 GPR99 已经完全处于一种就绪的活性构象:其螺旋内核内的若干保守“微开关”采用了通常仅在受体受刺激时才出现的构象。那些通常帮助将受体维持在关闭状态的关键位点在 GPR99 中被替换或重新定位,放松了内在约束,促进了有利于接受 G 蛋白伙伴的开放构型。
将信号传到细胞内部
在膜的内侧,结构显示了 GPR99 如何抓住传递其信号的 Gq 型 G 蛋白。G 蛋白的一段螺旋尾巴嵌入由 GPR99 某段螺旋外摆打开的腔体,与受体的内环和尾部形成一系列极性和疏水性接触。破坏这一界面的突变也会降低信号传导,证实外侧环和水簇产生的自激活能有效耦合到胞内伙伴。总体而言,这些结构快照将受体外表面的变化与其在细胞内触发的钙信号波联系起来。
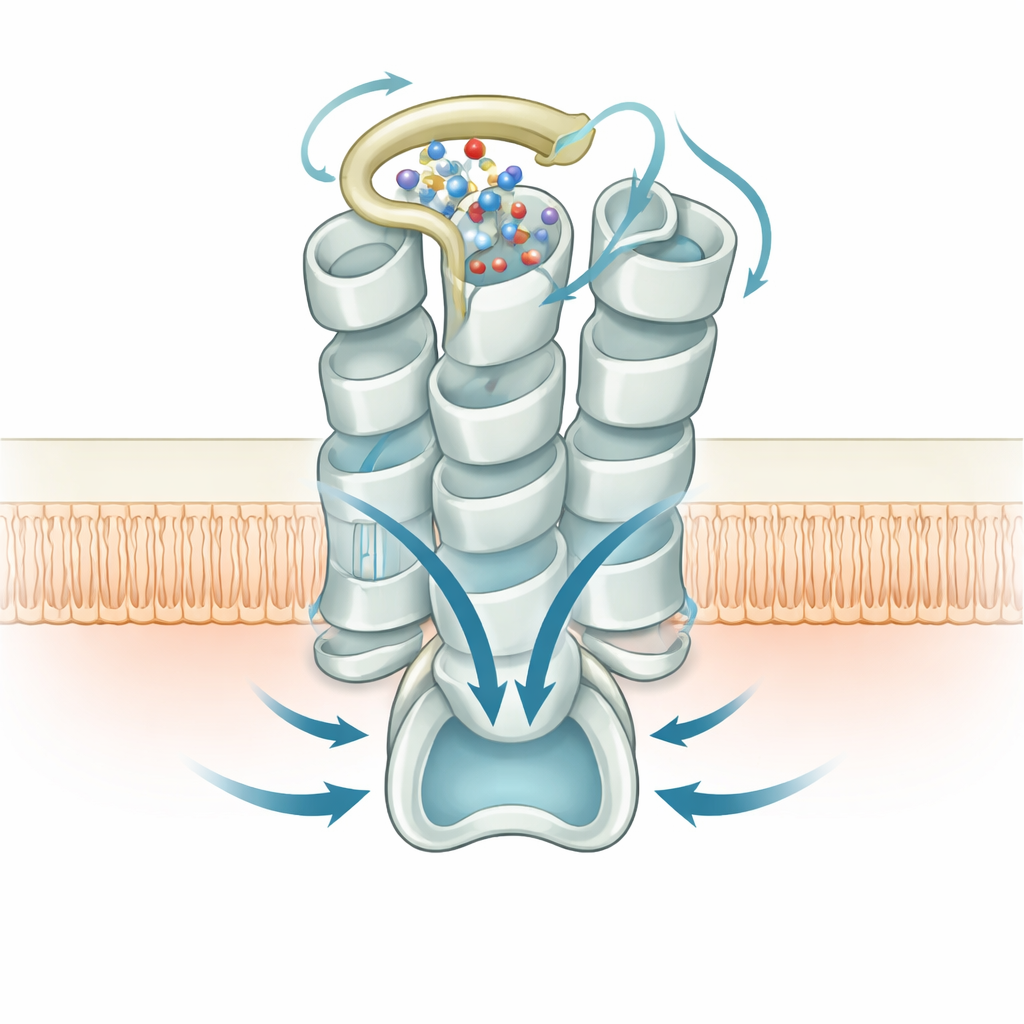
对呼吸及其他方面的影响
作者提出,GPR99 由结构性水分子强化的内置活性可能使气道组织处于“待命”状态——在炎性脂质或代谢变化出现时,准备分泌黏液并发起免疫反应。由于 GPR99 即使在无外界信号下也高度活跃,且其激活依赖于特定的环‑水排列,这些结构学发现为药物设计者提供了明确的靶点。可以通过小分子破坏该内部开关或其水网络来抑制过度炎症,而精细调节该相互作用的化合物则可能利用 GPR99 的敏感性带来治疗益处。
引用: Xiao, M., Bao, X., Guo, Y. et al. Structural analysis reveals that water molecules mediate self-activation of GPR99. Commun Biol 9, 342 (2026). https://doi.org/10.1038/s42003-026-09644-5
关键词: GPR99, GPCR 激活, 结构生物学, 炎症, 水介导的信号传导