Clear Sky Science · zh
抗MHC-I抗体阻断抑制性NK细胞受体在肿瘤免疫中的结构机制
解锁体内沉默的癌症杀手
我们的免疫系统拥有一类强大的哨兵——自然杀伤(NK)细胞,它们能够识别并消灭癌细胞和被病毒感染的细胞。然而肿瘤常常学会让这些哨兵保持沉默。本文以原子级细节揭示了一种经特殊设计的抗体如何移除这种“静音按钮”,重新唤醒NK细胞,使其更有效地攻击肿瘤。该研究将最前沿的结构生物学方法与小鼠实验结合,展示了一种抗体如何补充现有的癌症免疫疗法。
我们细胞表面的免疫身份标签
我们体内的每个细胞表面都展示着被称为MHC I类分子的分子“身份标签”。这些标签帮助免疫细胞分辨正常组织与已转变为癌变或被病毒感染的危险细胞。NK细胞不断扫描这些标签;当它们感知到正常模式时,NK细胞上的抑制性受体会发出抑制信号,防止攻击。肿瘤经常保持这些标签的可见性,将其作为保护屏障:只要抑制信号存在,NK细胞就会保持克制,肿瘤得以生长。
抓住保护盾的抗体
研究人员研究了一种名为B1.23.2的单克隆抗体,该抗体能强烈结合肿瘤细胞上许多人类MHC I类变体。通过冷冻电子显微镜和X射线晶体学,他们精确描绘了该抗体如何在MHC表面结合。B1.23.2钩住了MHC分子上一个保守的脊状区域——α2螺旋——而不接触其轻链伙伴,并且仅对所呈递的肽有很弱的感知。这意味着该抗体可以以很高的亲和力识别多种人类MHC-A、-B和-C分子,同时对MHC所展示的特定小蛋白片段相对不敏感。
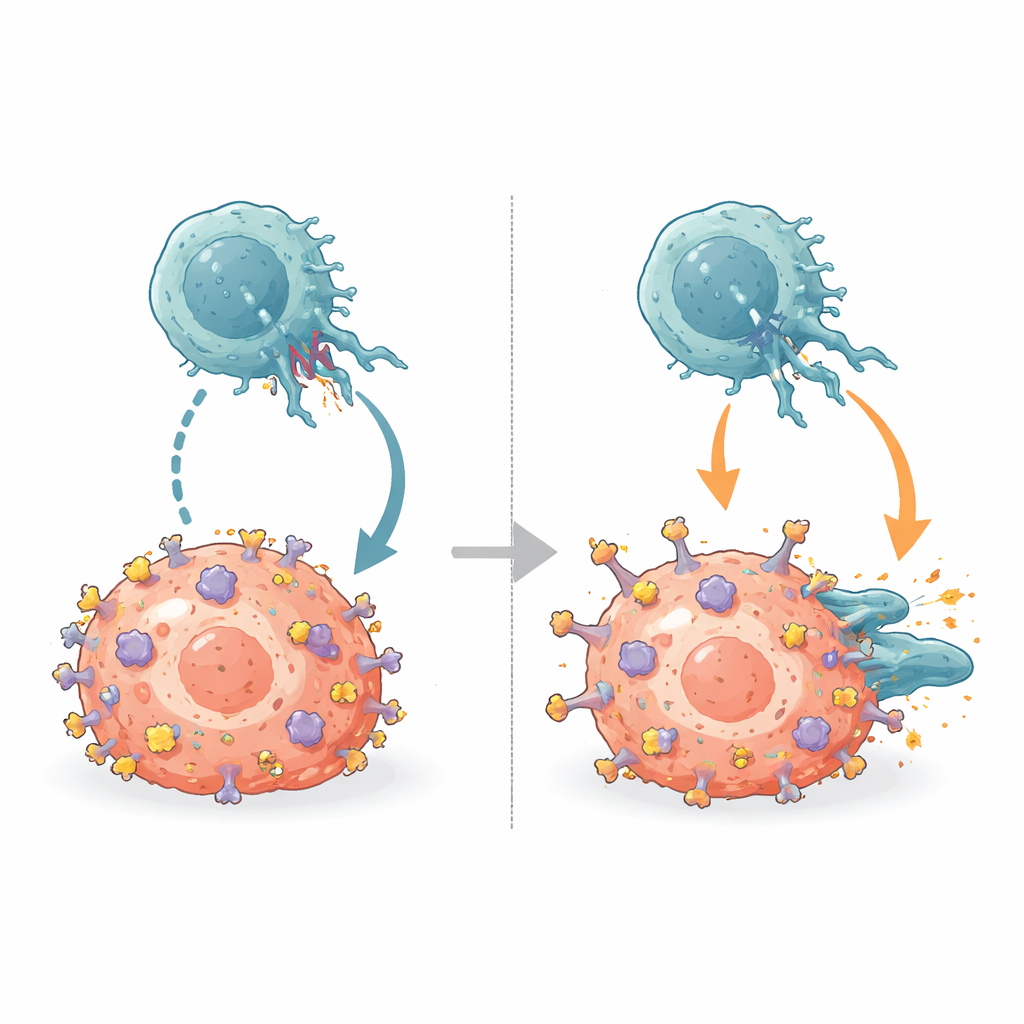
胜过免疫制动器
NK细胞携带称为KIR的抑制性受体,通常也停靠在MHC的同一α2脊上。通过将新的抗体–MHC结构与已知的KIR–MHC结构比对,团队显示B1.23.2在物理上占据了KIR需要抓握的那片MHC表面。抗体的结合位点与KIR的接触足迹高度重叠,二者无法同时结合。B1.23.2对MHC的结合也比KIR更紧密,因而在这场分子角力中获胜。因此,当抗体包裹在肿瘤细胞的MHC分子上时,NK细胞上的KIR便无法再传递抑制信号,平衡被推向NK细胞激活的一方。
微调契合度并扩大适用范围
尽管B1.23.2主要靶向保守的MHC表面,作者发现MHC所结合肽的细微差异可以微妙地调节抗体强度。通过系统地替换肽中单个氨基酸位置,他们展示了结合力的适度变化——总体通常在约十倍范围内——但并未丧失总体识别能力。他们还探究了为何某些常见MHC类型,例如HLA-A*02:01,会逃避结合。通过将来自一种可响应MHC变体的关键接触残基移植到HLA-A*02:01中,团队构建了抗体现在能识别的工程化版本,精确确认了形成关键对接面的位点。这些洞见提示未来可设计抗体变体以覆盖更多MHC类型或选择性地避开某些类型。
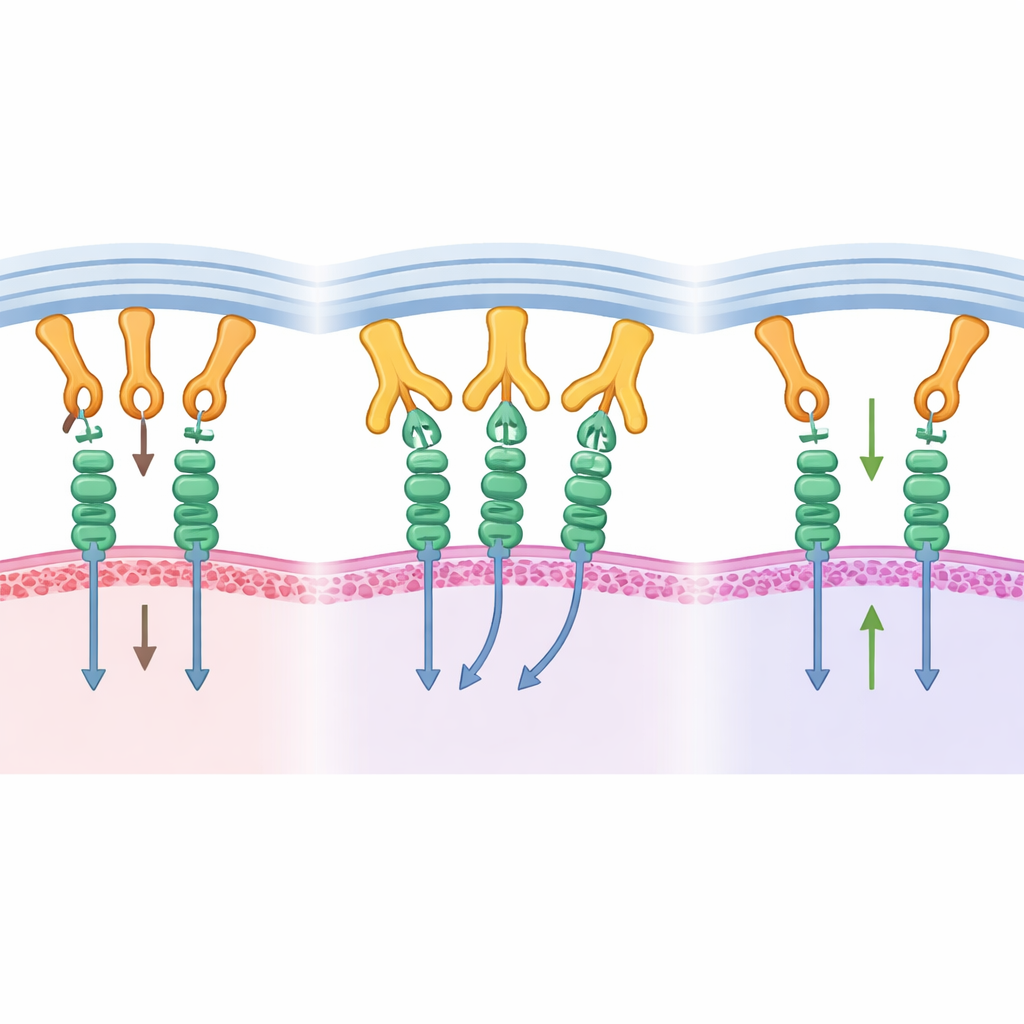
将结构学洞见转化为肿瘤控制
这种分子阻断作用真的能帮助对抗肿瘤吗?为检验这一点,研究人员使用了携带人类胰腺癌的人源化小鼠模型。他们构建了一种无法通过自身Fc尾段发出效应信号的B1.23.2形式,以便任何效果主要来自阻断MHC–KIR相互作用。当小鼠在给予该抗体并移入人NK细胞后,肿瘤生长明显减慢。NK细胞显示出增殖增加、生长和信号通路活性更高,以及与杀伤癌细胞相关的炎性分子产生增多。在肿瘤组织内,NK细胞表现出更多的激活受体,符合它们摆脱持续抑制输入后的状态。
这对未来癌症疗法可能意味着什么
简而言之,这项研究展示了一种抗体如何在肿瘤细胞与免疫系统的制动器之间插入,阻断通常使NK细胞保持安静的“不要攻击”信号。通过原子分辨率绘制相互作用并在动物中确认其效应,该工作为一类新疗法提供了蓝图:针对肿瘤身份标签而非直接靶向免疫受体的抗体。这类制剂可与现有的检查点抑制剂或细胞疗法联合使用,以动员NK细胞和T细胞,从另一个角度增强免疫系统对难治性癌症的攻击力。
引用: Jiang, J., Panda, A.K., Natarajan, K. et al. Structural mechanism of anti-MHC-I antibody blocking of inhibitory NK cell receptors in tumor immunity. Commun Biol 9, 350 (2026). https://doi.org/10.1038/s42003-026-09641-8
关键词: 自然杀伤细胞, MHC I类分子, 癌症免疫治疗, 单克隆抗体, 抑制性受体