Clear Sky Science · zh
LukS-PV 靶向 C5aR 通过 BCL6/HDAC6/HSPD1 轴抑制肝细胞癌的上皮-间质转化
将细菌武器变为抗癌利器
肝细胞癌是最常见的肝癌类型,往往致命,原因在于它能从肝脏扩散到其他器官。本文探讨了一个出人意料的对抗转移的盟友:一种名为 LukS-PV 的蛋白,最初属于金黄色葡萄球菌产生的毒素。研究人员展示了该蛋白如何结合肝癌细胞上的特定受体,并且不对正常组织造成危害,而是关闭促进癌细胞脱落、迁移和形成新肿瘤的关键步骤。
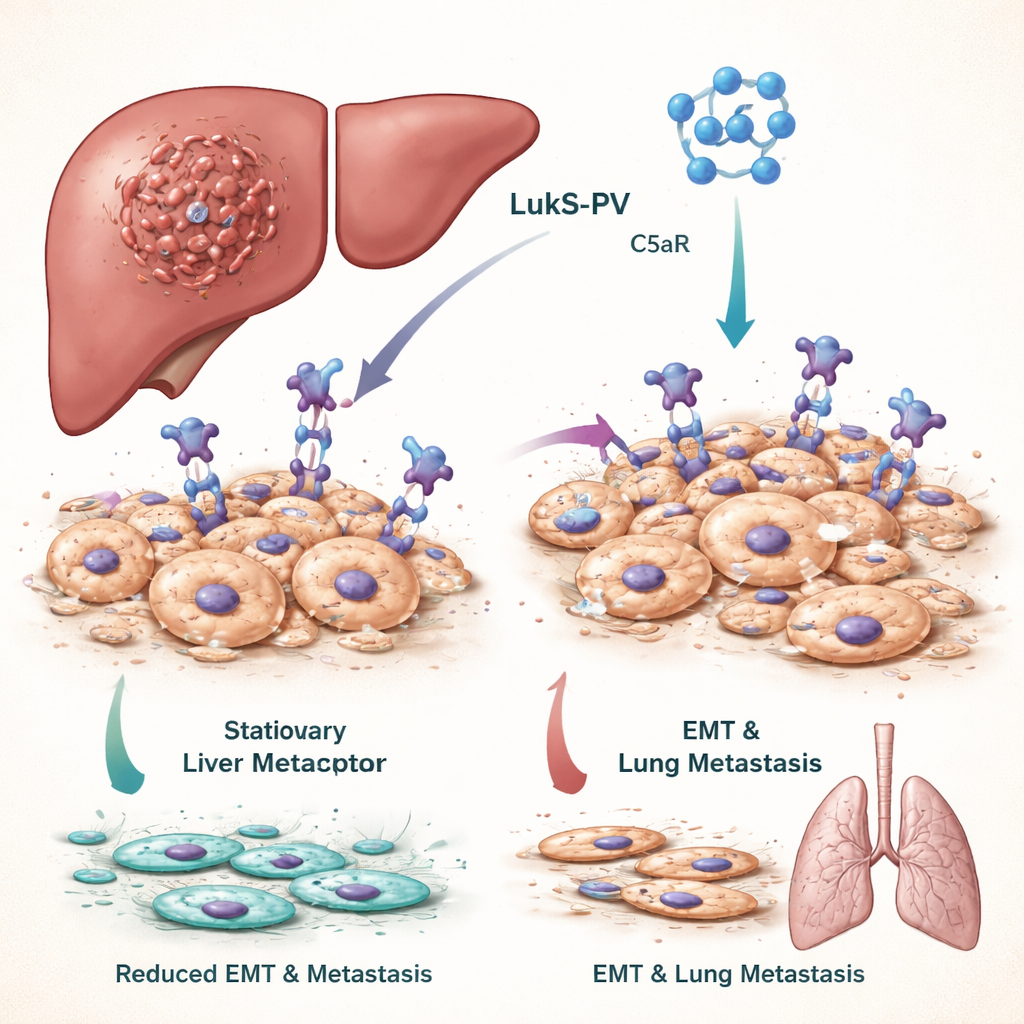
为何阻止癌细胞变形很重要
要让肝癌发生远处转移,肿瘤细胞必须经历一种显著的形态和行为改变,称为上皮-间质转化(EMT)。在 EMT 过程中,原本紧密排列、固定不动的细胞变得更具可塑性、移动性和侵袭性,使其能进入血管并在肺等远处器官播种。肿瘤呈现高 EMT 活性的患者通常预后较差。团队关注的是由分子 C5a 及其受体 C5aR 驱动的信号通路,该受体在许多肿瘤细胞上异常丰富,并已知助长 EMT 和转移。
一个能靶向癌症信号的毒素成分
潘通-瓦伦丁白细胞毒素(Panton–Valentine leukocidin)是金黄色葡萄球菌的一种毒素,其中的 LukS-PV 成分天然能识别并结合 C5aR。作者先前的工作显示,重组的、不会形成孔的 LukS-PV 版本可以抑制多种癌症的生长,且在动物中未见明显毒性。在本研究中,他们用 LukS-PV 处理肝癌细胞系,观察到细胞迁移性和侵袭性下降。分子层面的检测表明,表征安定、行为良好细胞的标志物上升,而表征侵袭性、易移动细胞的标志物下降。在将肝癌细胞注入小鼠的体内实验中,LukS-PV 处理组肺部的肿瘤结节明显更少,表明转移被抑制。
阻断肿瘤细胞内的连锁反应
进一步探查时,研究人员发现了 LukS-PV 干扰的肿瘤细胞内一条控制级联。首先,LukS-PV 结合在细胞表面的 C5aR 并有效阻断来自 C5a 的促转移信号。这种对 C5aR 信号的抑制使一种称为 BCL6 的蛋白水平下降,BCL6 是一种通常在细胞核内开启特定基因表达的转录因子。BCL6 的靶点之一是 HDAC6,一种去除蛋白上乙酰基的小酶。当 BCL6 丰富时,HDAC6 水平升高,细胞更倾向于发生 EMT 并迁移。LukS-PV 对 C5aR 的干预降低了 BCL6,从而减少 HDAC6 的产生并减缓这一促转移程序。
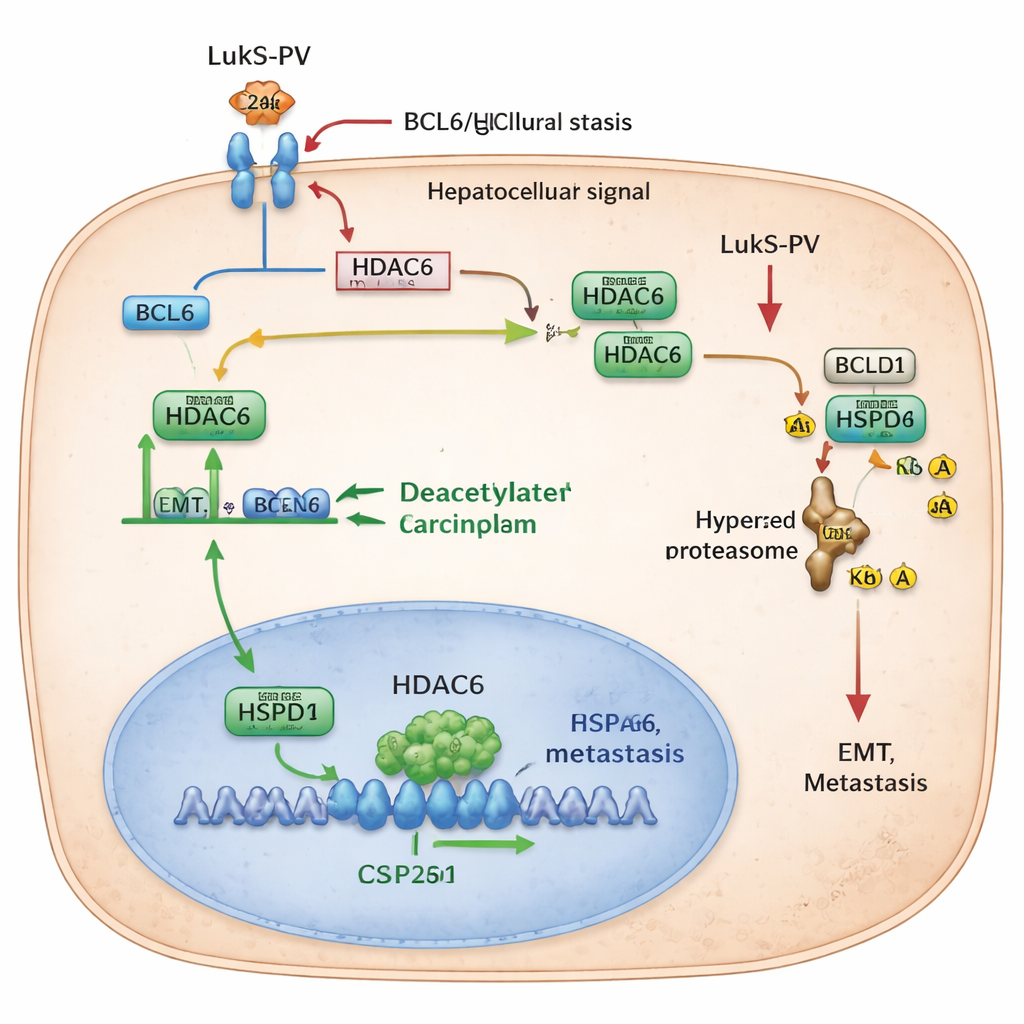
标记伴侣蛋白以促其降解
团队随后鉴定出 HDAC6 的一个关键伙伴 HSPD1(亦称 HSP60),这是一种“伴侣蛋白”,帮助其他蛋白折叠并维持稳定性。在肝癌中,HSPD1 的表达高于邻近的正常组织,并与患者较差的生存率相关。研究人员发现 HDAC6 与 HSPD1 存在物理相互作用,并去除其两个特定位点的乙酰基。当这些乙酰标签被移除后,HSPD1 更加稳定并支持 EMT 与转移。当通过基因手段或 LukS-PV 处理减少 HDAC6 时,HSPD1 变得更多乙酰化。这种高乙酰化形式会被细胞的废物处理机制识别并标记上泛素,随后被降解。随着 HSPD1 水平下降,癌细胞迁移、侵袭和在肺部定植的能力部分丧失。
从复杂通路到一个简单结论
对非专业读者来说,结论是作者绘制出肝癌细胞内的一连串多米诺效应:细胞表面受体(C5aR)提升一个调控蛋白(BCL6),后者提高一种酶(HDAC6),该酶保护一个伴侣蛋白(HSPD1)免于被降解。共同作用下,这些因子帮助癌细胞改变形态、移动并扩散。实验室里被重新用途化的细菌蛋白 LukS-PV 在细胞表面便可中断这一序列,最终导致 HSPD1 的降解并抑制转移。尽管仍处于实验阶段,这项工作提示,基于 LukS-PV 的药物——或针对 BCL6、HDAC6 或 HSPD1 的治疗——可能为阻止肝肿瘤转移、改善患者预后提供新途径。
引用: Ding, P., Shi, L., Xu, X. et al. LukS-PV targeting C5aR inhibits EMT in hepatocellular carcinoma via the BCL6/HDAC6/HSPD1 axis. Commun Biol 9, 314 (2026). https://doi.org/10.1038/s42003-026-09640-9
关键词: 肝细胞癌, 转移, 上皮-间质转化, HDAC6, 细菌毒素疗法