Clear Sky Science · zh
周期性受限细胞迁移在癌细胞系中驱动部分可逆的染色质重构
被压迫的癌细胞如何“记住”应激经历
脱离肿瘤的癌细胞必须在体内的组织和血管间隙中爬行。为此,它们需要将柔软的细胞内部——尤其是包含DNA的细胞核——挤过有时比细胞核还小的空间。本研究探讨了在反复受压过程中DNA包装发生了什么,并提出一个关键问题:细胞核是会简单地恢复原状,还是会保留一种可能帮助癌症扩散的“机械记忆”?
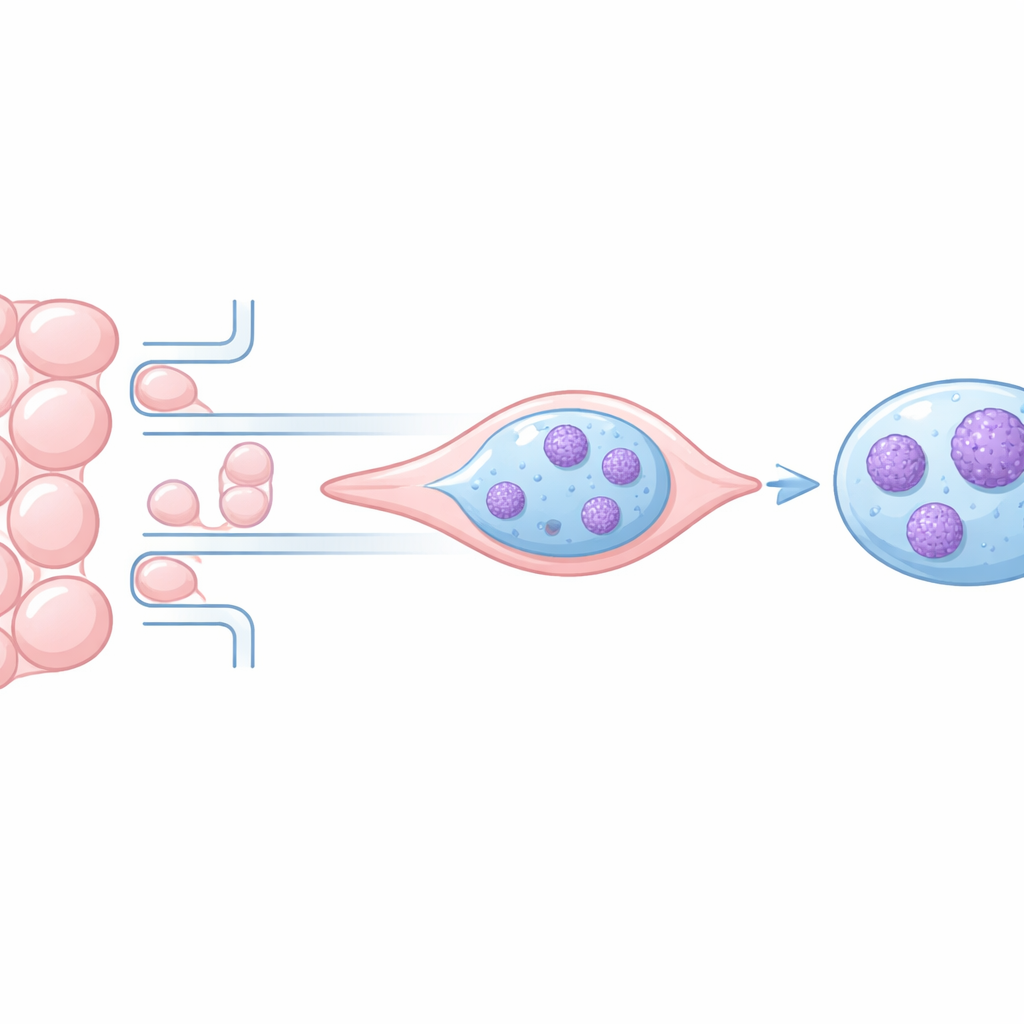
为什么DNA包装在细胞移动时如此重要
在细胞核内,DNA缠绕在蛋白质上并折叠成染色质,染色质可以松散或高度凝聚。较松散的区域通常处于活跃状态,承载经常被使用的基因,而高度凝聚的区域则趋向沉默。当细胞穿过狭窄空间时,细胞核会发生变形,先前的研究表明这可能暂时致使染色质致密化,甚至损伤DNA。但尚不清楚这些变化是否会完全逆转,或是否留下持久痕迹,从而改变癌细胞的侵袭性。
用微型迷宫挤压单个癌细胞
研究人员构建了一个定制的微流体装置——一块透明芯片,包含数十条在宽段和窄段间反复交替的微通道。两种不同的癌细胞系被工程化使染色质在显微镜下发光,并在化学引诱物的引导下爬过这些通道。高分辨率的时间推移成像使团队能够追踪每个细胞核的运动,测量细胞核尺寸并逐帧映射明亮的高度凝聚染色质簇,在超过100个单细胞中进行分析。
细胞核在受压时发生了什么
每当细胞进入狭窄的收缩段时,其细胞核的投影面积会突然缩小,反映出核体积的可逆减少。与此同时,高度凝聚染色质占据核区的比例激增——常常增加两到三倍——然后在细胞进入较宽区域后回落到基线。这一模式在连续几个收缩段和两种癌细胞类型中重复出现,表明总体致密染色质量是一种对机械应力的灵活短期反应,而非永久性改变。然而,对荧光强度模式的更细致观察显示,在挤压过程中既有极高强度像素也有极低强度像素的数量增加,暗示内部重排比简单的均匀压实更为复杂。
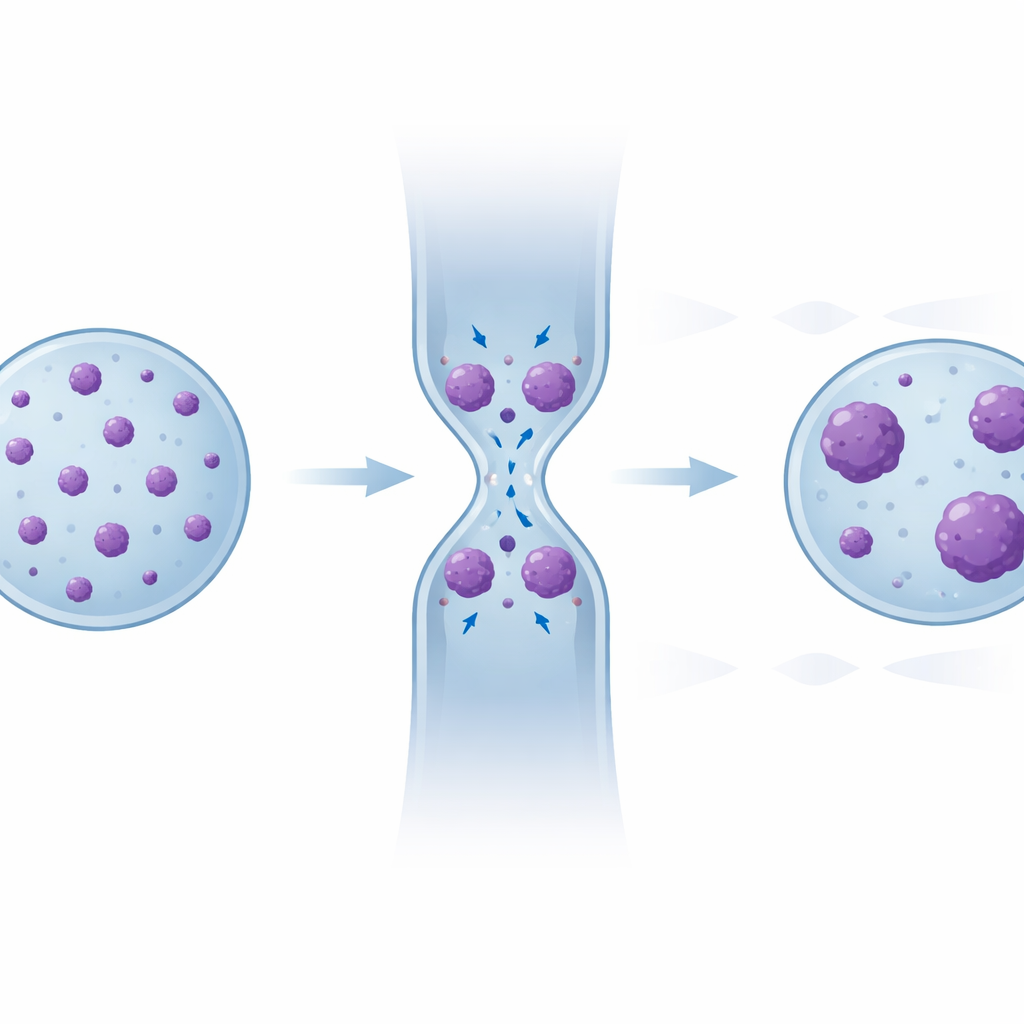
DNA簇图案中隐藏的记忆
为了揭示这种隐藏的重组,团队检查了每一个单独的凝聚染色质簇——其大小以及每个细胞核所含簇的数量——在受限前、受限中和受限后如何变化。在挤压期间,小簇倾向于合并成更大的簇。细胞核放松后,总的凝聚区域面积恢复到原始水平,但图案并未完全回到初始状态:与起始状态相比,经过多个收缩段的细胞总体上簇的数量更少,且偏向于更大的尺寸。统计比较证实,随后“恢复”区域的分布越来越像受限期间看到的分布。免疫荧光染色进一步显示,这些致密区域中许多与已知的“沉默”染色质标记重叠,而将染色质视为相互作用聚合物的计算模型仅凭变形使粘性的DNA片段聚集,就能再现这种部分但不完全的松弛行为。
这对癌症扩散与未来疗法意味着什么
通俗地说,这项研究发现,当癌细胞核反复被挤压时,其DNA包装行为像带有记忆的减压球。细胞核在尺寸上可以弹回,总体的致密程度可以复位,但致密DNA块的细节图谱并不会完全恢复。经过多次挤压循环,细胞核最终呈现出更少但更大的致密区域,可能改变哪些基因更容易或更难被访问。这种“机械记忆”可能帮助癌细胞更好地耐受未来的变形,从而在侵入新组织时更加适应。理解并最终针对这种物理力与DNA组织耦合的机制,或许能开辟通过干扰癌细胞适应机械应激来限制转移的新途径。
引用: Blazquez-Romero, M.d.V., Mendivil-Carboni, M., Sarasquete-Martinez, M. et al. Periodic confined cell migration drives partially reversible chromatin reorganization in cancer cell lines. Commun Biol 9, 366 (2026). https://doi.org/10.1038/s42003-026-09637-4
关键词: 受限细胞迁移, 染色质凝聚, 细胞核力学, 机械记忆, 癌症转移