Clear Sky Science · zh
通过泛素连接酶 Nedd4-1(NE) 对 NF-κB 通路的负向调控
为什么终止炎症很重要
免疫系统依赖快速的炎症反应来对抗感染和促进损伤愈合,但如果这些反应持续过久,同样的机制会损伤组织并助长癌症发生。本文探讨人类及其他灵长类细胞如何通过一种新鉴定的内在“刹车”来避免这一危险,在任务完成后安抚机体的一个核心报警系统。
细胞内的一个核心报警开关
这一故事的中心是 NF-κB,这是一个蛋白家族,像主开关一样控制着数百个参与炎症、细胞存活和免疫反应的基因。当细胞感知到诸如炎症分子 TNFα 等应激信号时,一系列事件使 NF-κB 从细胞液相中的“伴侣蛋白”中释放出来,允许它进入细胞核,开启促炎和促存活基因。由于该通路威力巨大,细胞必须对其激活与关闭进行严格调控。未能及时关闭该通路已与慢性炎症性疾病和多种癌症相关联。
一种仅见于灵长类的报警刹车
研究人员将注意力集中在 Nedd4-1 上——这是一类大型酶家族的成员,负责将小分子泛素标记添加到其他蛋白上。这一标记往往将蛋白指向降解或在细胞内重新定位,从而重塑信号网络。此前发现的 Nedd4-1 剪接变体 Nedd4-1(NE) 仅在灵长类中存在,并在其前端携带一段较长的额外序列,改变了其在细胞中的定位和识别对象。与可以通过其他伙伴促进 NF‑κB 活性的标准 Nedd4-1 形式相反,团队发现 Nedd4-1(NE) 具有相反作用:它抑制 NF‑κB 信号,尤其是在持续 TNFα 刺激后。
两种抑制 NF-κB 的方式
为揭示该刹车如何发挥作用,作者使用了邻近标记和蛋白质拉下法来识别与 Nedd4-1(NE) 发生物理相互作用的分子。他们鉴定出 NF‑κB 通路的关键成分,包括激酶 IKKβ 和 NF‑κB 前体蛋白 NF‑κB1(也称 p105)。后续实验显示 Nedd4-1(NE) 向 IKKβ 添加泛素标记,导致其降解。IKKβ 水平降低后,其常见靶标 IκBα 不再被有效磷酸化和降解。因此,IκBα 更加稳定,继续将活性 NF‑κB 亚基 p50 围留在细胞质中,阻止其进入细胞核从而启动炎症基因。
由适配子引导的交接到刹车装置
Nedd4-1(NE) 还在下游通过限制 NF‑κB1 水平发挥作用。在这里,该酶并非独自工作:它与另一种泛素标记蛋白 KPC1 协同。KPC1 有助于将 NF‑κB1 前体 p105 处理成活性 p50 并存在于称为晚期内体的细胞区室中,而 Nedd4-1(NE) 也定位于这些区室。团队表明 Nedd4-1(NE) 可以对 KPC1 进行泛素化,被修饰的 KPC1 作为适配子将 NF‑κB1 招募到位于晚期内体的 Nedd4-1(NE)。这一三方复合体促进 p105 和 p50 的不稳定化,再次减少可进入细胞核的 NF‑κB 库存。
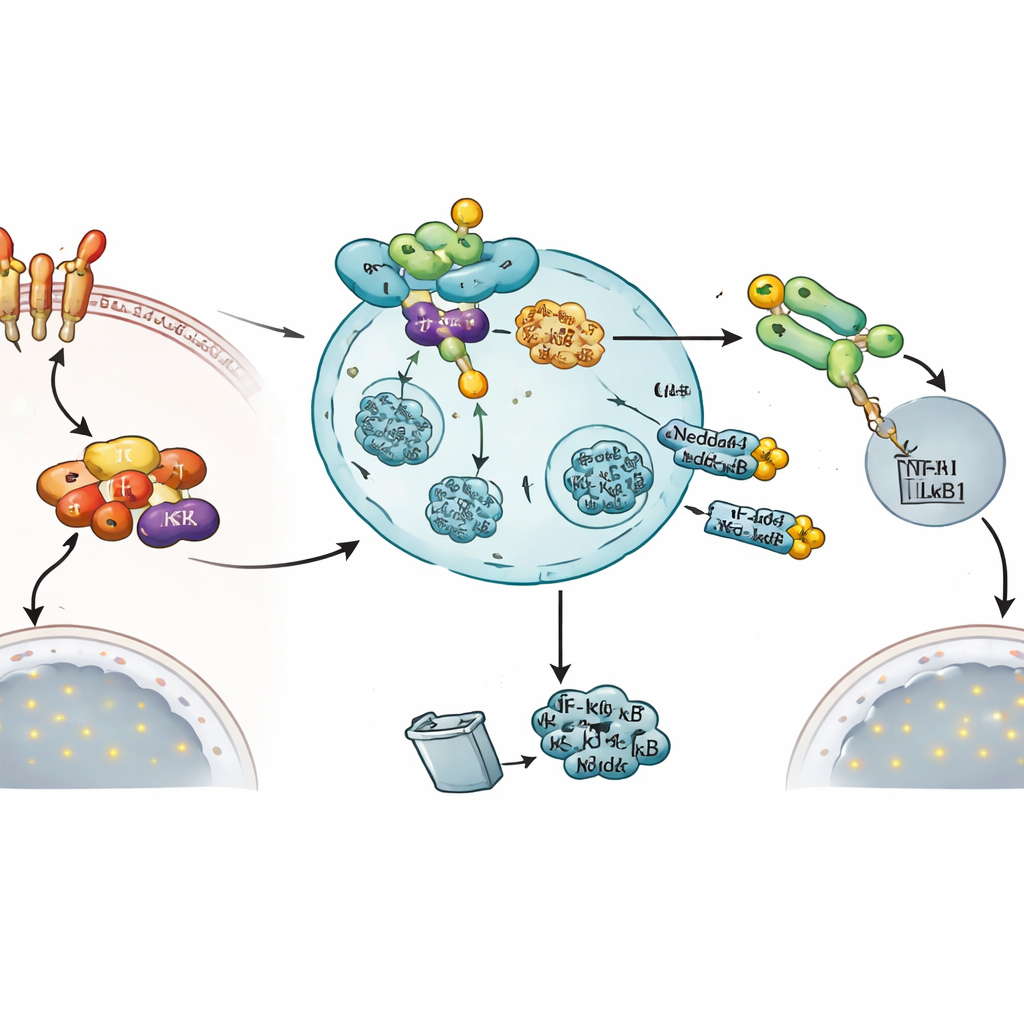
结束信号的内置反馈回路
值得注意的是,激活 NF‑κB 的同一信号似乎也会诱导这一刹车机制。当细胞用 TNFα 处理时,Nedd4-1(NE) 的信使 RNA 水平显著上升,而标准 Nedd4-1 形式未见变化。功能性读数支持 Nedd4-1(NE) 是一个关闭阀的观点:增加活性 Nedd4-1(NE) 可减少 NF‑κB1 进入细胞核的移动,降低 NF‑κB 应答报告基因的活性,并减少受 NF‑κB 调控的炎症基因 TNFAIP3 的表达。综合这些发现描绘出一个负反馈回路:NF‑κB 通路的激活最终提升 Nedd4-1(NE),后者针对两个关键节点——IKKβ 和 NF‑κB1——将炎症反应拉回。
这对健康与疾病意味着什么
对普通读者而言,关键信息是:我们的细胞包含一个额外的、仅在灵长类存在的安全机制,以防止炎症信号失控。通过选择性地标记和剪裁 NF‑κB 系统的核心成分,Nedd4-1(NE) 有助于终止对 TNFα 的应答,并可能维持长期免疫平衡。理解这一内置刹车可能为治疗那些 NF‑κB 长期过度活化的疾病(如自身免疫性疾病和某些癌症)提供新思路,提示可通过模拟或增强这一自然关闭过程来干预。
引用: Persaud, A., Kefalas, G., Shteiman, A. et al. Negative regulation of the NF-κB pathway by the ubiquitin ligase Nedd4-1(NE). Commun Biol 9, 374 (2026). https://doi.org/10.1038/s42003-026-09634-7
关键词: NF-kB 信号传导, 炎症, 泛素连接酶, Nedd4-1(NE), 肿瘤坏死因子 α