Clear Sky Science · zh
Notch3 调控结直肠癌中周细胞的表型可塑性
为何肿瘤周围的血管至关重要
结直肠癌是全球最常见且致死性高的癌症之一,但大多数疗法直接针对肿瘤细胞,常常忽视了帮助肿瘤生长的周围支持系统。本文聚焦于一类较少为人所知的支持细胞——包绕微小血管的周细胞。通过揭示名为 Notch3 的信号开关如何改变周细胞的行为,作者展示了肿瘤血供如何被推动向有利于癌症的渗漏、混乱血管,或向更接近正常、有助于抑制病情并改善治疗效果的血管方向发展。 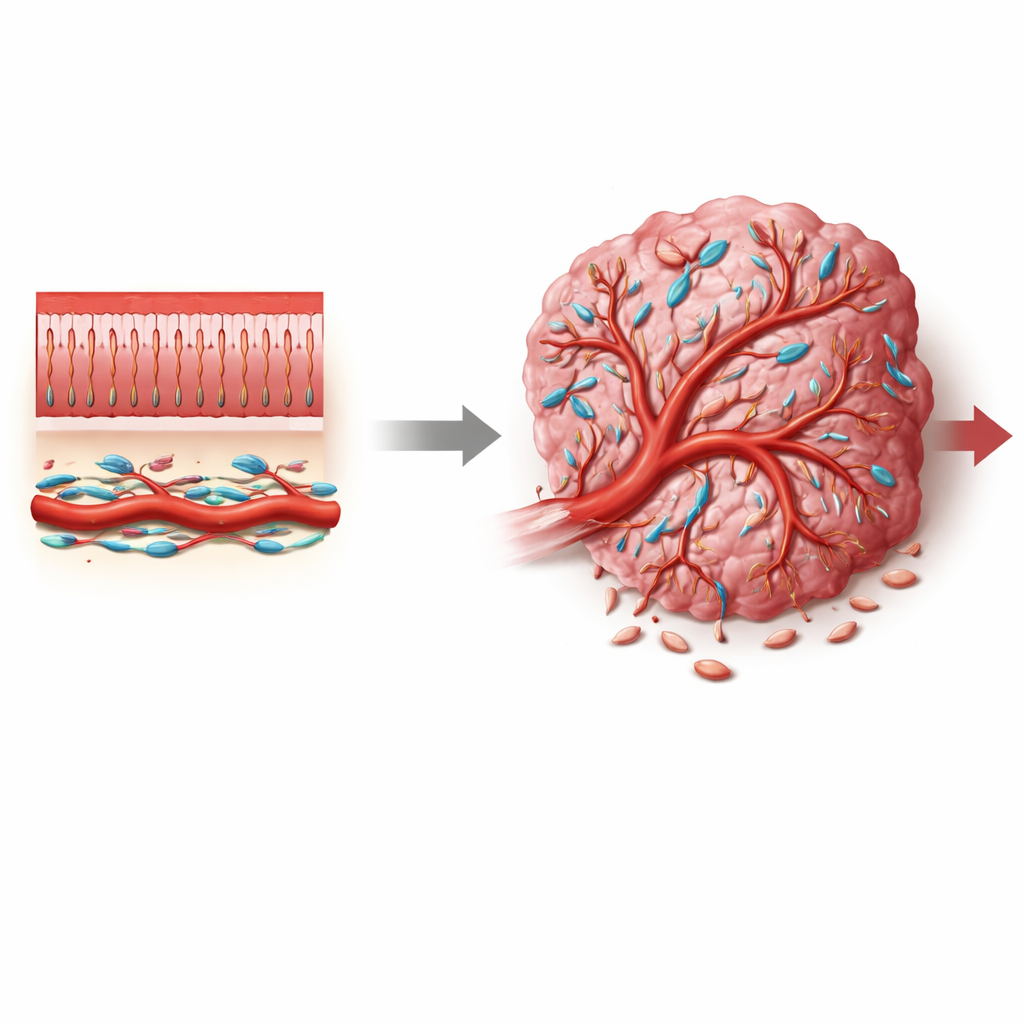
肿瘤血管周围的隐形帮手
血管不仅仅是空心管道。在健康组织中,小血管被周细胞紧密包围——这种专门化细胞可稳定血管壁、调节血流并控制渗漏。然而在肿瘤中,这些周细胞常表现出不同的形态和行为:它们可能脱落、增殖或改变身份,从而促进典型癌症所见的异常、渗漏血管。在结直肠肿瘤中,微环境充斥着成纤维细胞、免疫细胞和血管细胞,人们尚不清楚肿瘤相关周细胞来自何处、处于何种状态,以及哪些分子信号将它们推向助长肿瘤的角色。
在肿瘤形成过程中追踪周细胞
为追踪周细胞的命运,研究者使用了结肠炎相关结直肠癌的小鼠模型,在这些模型中他们可以基因标记特定细胞类型并观察其命运。他们显示,肿瘤中发现的周细胞主要来源于正常、组织驻留的周细胞,这些细胞在癌症发展过程中扩增和增殖,而不是来自远处如骨髓的来源。通过先进的单细胞 RNA 测序,他们对来自小鼠肿瘤和正常结肠的数万条间质细胞进行了编目,发现周细胞在肿瘤微环境中明显富集。他们还在多个人类结直肠癌数据集中识别出相似的周细胞扩增,强调这并非仅限于小鼠的现象。
改变周细胞行为的分子开关
团队进一步探究了哪些信号在肿瘤内部塑造周细胞行为,发现在肿瘤周细胞中,Notch3——一种使细胞与邻居交流的受体——特别活跃。细胞间通信的计算分析表明,周细胞既发送也接收与 Notch 相关的信号,尤其是通过血管细胞上的配体。通过在周细胞中人工激活 Notch3,研究者观察到这些细胞增殖更多,但表达与血管稳固行为相关的收缩蛋白减少。此类小鼠的肿瘤血管变得更大、更易渗漏,并有更多增殖的内皮细胞,显示血管不稳。相反,删除 Notch3 则减少了内皮细胞增殖、缩小了血管尺寸并降低渗漏,表明血管朝向更正常化的方向转变,而早期肿瘤数量或大小并未发生显著改变。 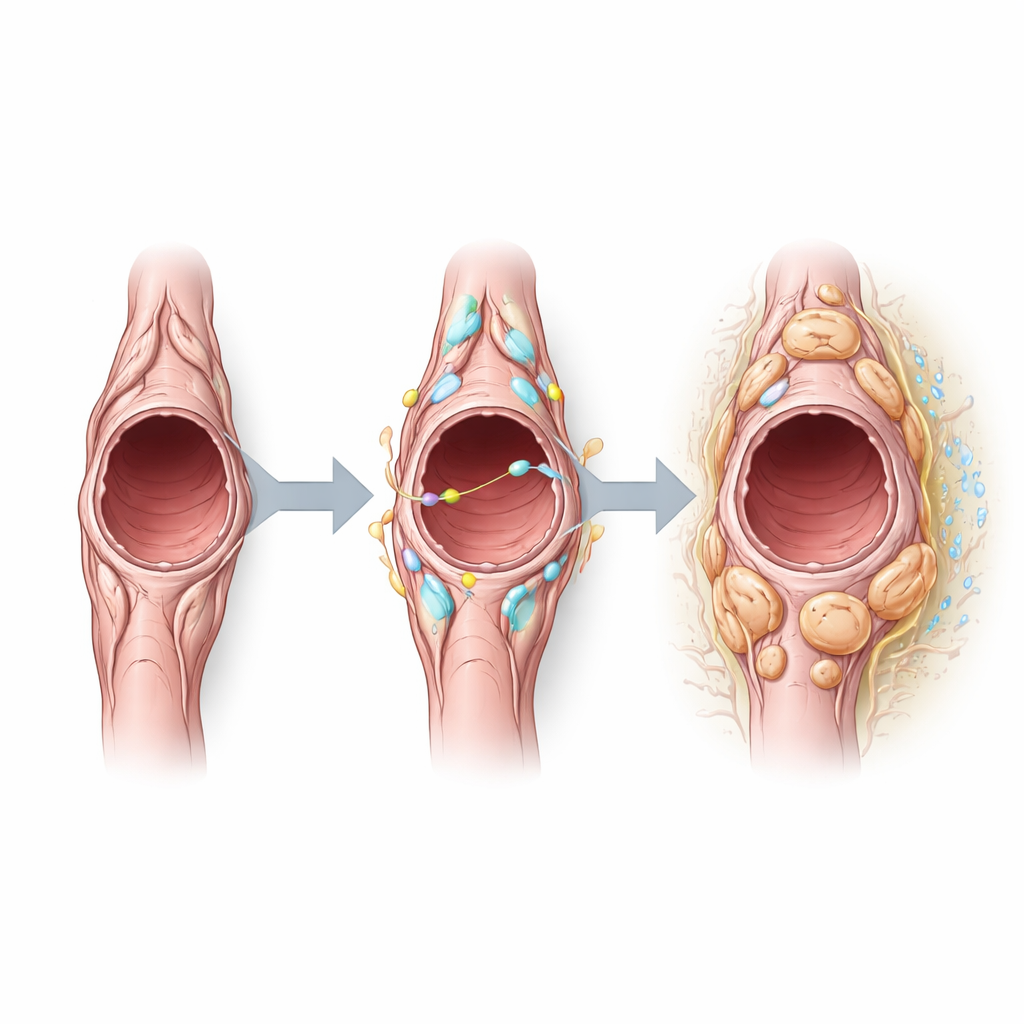
肿瘤内周细胞的多重面貌
除了简单的开关式变化之外,研究显示肿瘤周细胞存在多种不同状态。部分亚群显示高度收缩的特征,另一些产生大量细胞外基质,有些呈现炎性特征,还有一小部分携带通常见于内皮细胞的签名。Notch3 活性并非均衡分布:在“合成”或基质生成的周细胞群体中富集,而在更具收缩性的亚群中较低。轨迹分析提示,随着 Notch3 活性的上升,周细胞可以从收缩状态向合成、增殖状态转变。当作者检查人类结直肠癌数据时,发现可比的周细胞状态谱,并再次在肿瘤相关和增殖的周细胞中看到更高的 Notch3 靶基因活性,反映了小鼠结果。
将血管混乱转化为治疗机会
总体而言,该研究将 Notch3 描绘为调节周细胞身份的关键旋钮,并通过周细胞影响肿瘤血管的结构与功能。高 Notch3 活性将周细胞推向增殖、收缩性较低的状态,伴随血管扩张和渗漏,利于肿瘤进展。低 Notch3 活性则与更具收缩性的周细胞、更平静的内皮细胞和更正常化的血管相关,这可能抑制肿瘤生长并改善药物输送。通过特异性地在周细胞中靶向 Notch3,未来疗法或可将肿瘤血管从混乱引导向稳定,为与现有药物联合治疗晚期结直肠癌提供新的思路。
引用: Chalkidi, N., Stavropoulou, A., Arvaniti, VZ. et al. Notch3 regulates pericyte phenotypic plasticity in colorectal cancer. Commun Biol 9, 343 (2026). https://doi.org/10.1038/s42003-026-09629-4
关键词: 结直肠癌, 肿瘤微环境, 周细胞, Notch3 信号, 肿瘤血管