Clear Sky Science · zh
内皮细胞TRIM47通过KEAP1/NRF2信号通路在小鼠中调控血脑屏障完整性与认知
为何保护微小脑血管重要
脑小血管病是在大脑中悄然作祟的问题。它损害最小的血管,增加中风风险,并逐步侵蚀记忆与认知,但临床上仍缺乏能针对其根本生物学机制的治疗方法。本研究聚焦于一种在脑血管内皮细胞中存在的特定蛋白TRIM47,提出一个简单且关键的问题:它是否有助于维持大脑的防护屏障——血–脑屏障的完整性,这对认知是否重要?
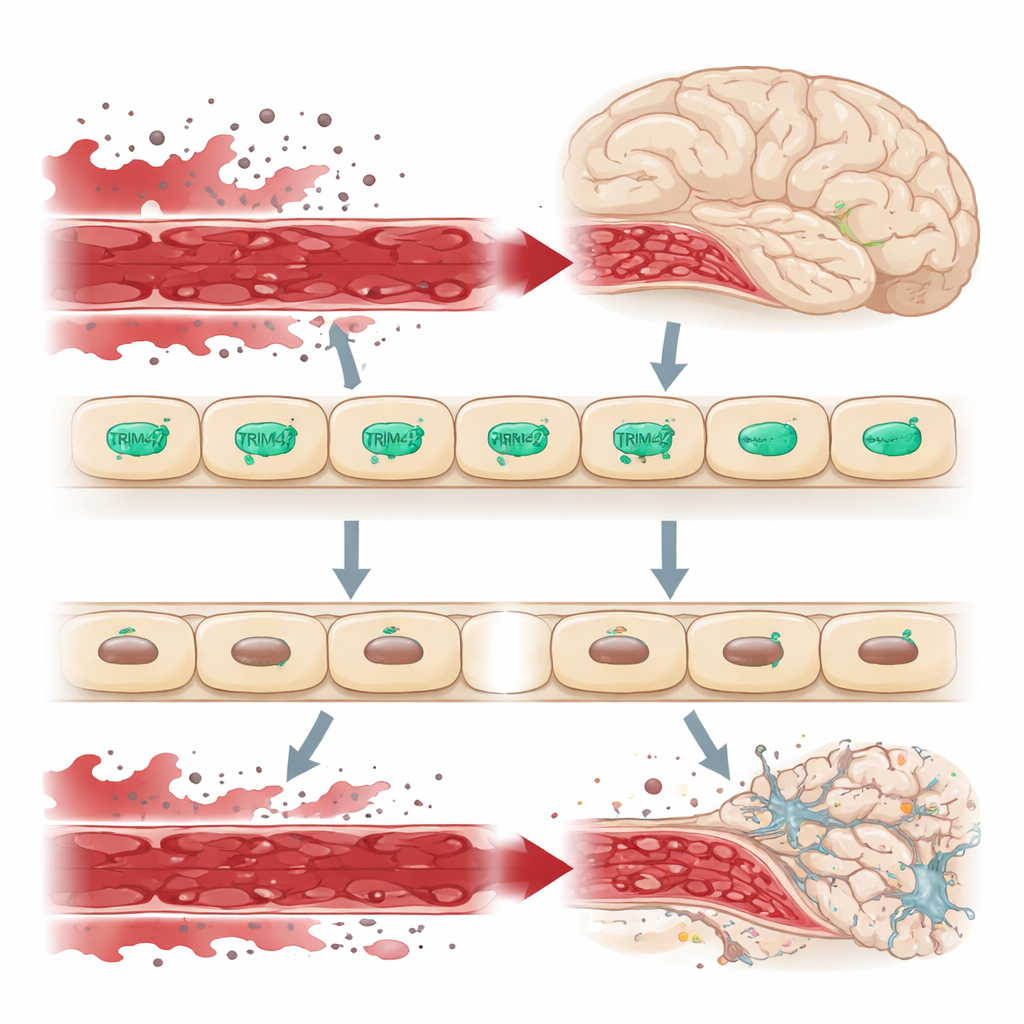
大脑边界上的守门员
血–脑屏障由紧密封闭的内皮细胞层构成,严格控制进入脑组织的物质,从而将大脑与全身循环隔离。当该屏障出现渗漏时,血液中的有害分子会渗入脑内,给神经元和支持细胞带来压力,并促成诸如痴呆等疾病。大规模人群的基因研究曾指出含有TRIM47基因的那段DNA是脑小血管病的风险区。TRIM47在脑内皮细胞中特别活跃,提示它可能是维持该屏障的重要守护因子。
TRIM47如何增强细胞对氧化应激的防御
作者首先在体外培养的人脑内皮细胞中通过RNA干扰降低TRIM47水平。此举引发了广泛的基因表达变化,其中受影响最显著的网络以NRF2为中心,NRF2是细胞抗氧化防御的主控因子。在正常情况下,NRF2被另一种蛋白KEAP1抑制并导向降解。研究团队证明TRIM47可与KEAP1结合,帮助阻止NRF2被降解。在TRIM47存在时,NRF2得以积累、进入细胞核并启动清除活性氧的基因程序。当TRIM47缺失时,NRF2水平下降,抗氧化基因活性减弱,内皮细胞对氧化应激变得更脆弱。
从血管渗漏到小鼠的记忆障碍
为了在活体中观察这一机制的影响,研究者构建了全身缺失Trim47基因的小鼠模型,以及另一个仅在内皮细胞中可删除Trim47的系。两种模型的成年动物均出现明确的空间学习与记忆障碍,在Y迷宫和莫里斯水迷宫等任务中表现不佳,但运动能力正常。对其大脑的检查显示血–脑屏障已变得渗漏:小型荧光示踪物和血液蛋白从血管漏入周围组织。构成内皮细胞紧密连接和黏附连接的关键“封闭”蛋白,尤其是Claudin-5和Occludin,表达下降。邻近的星形胶质细胞——对损伤反应迅速的支持细胞——出现活化,尽管在该阶段尚未看到明显的广泛炎症或神经元丧失迹象。
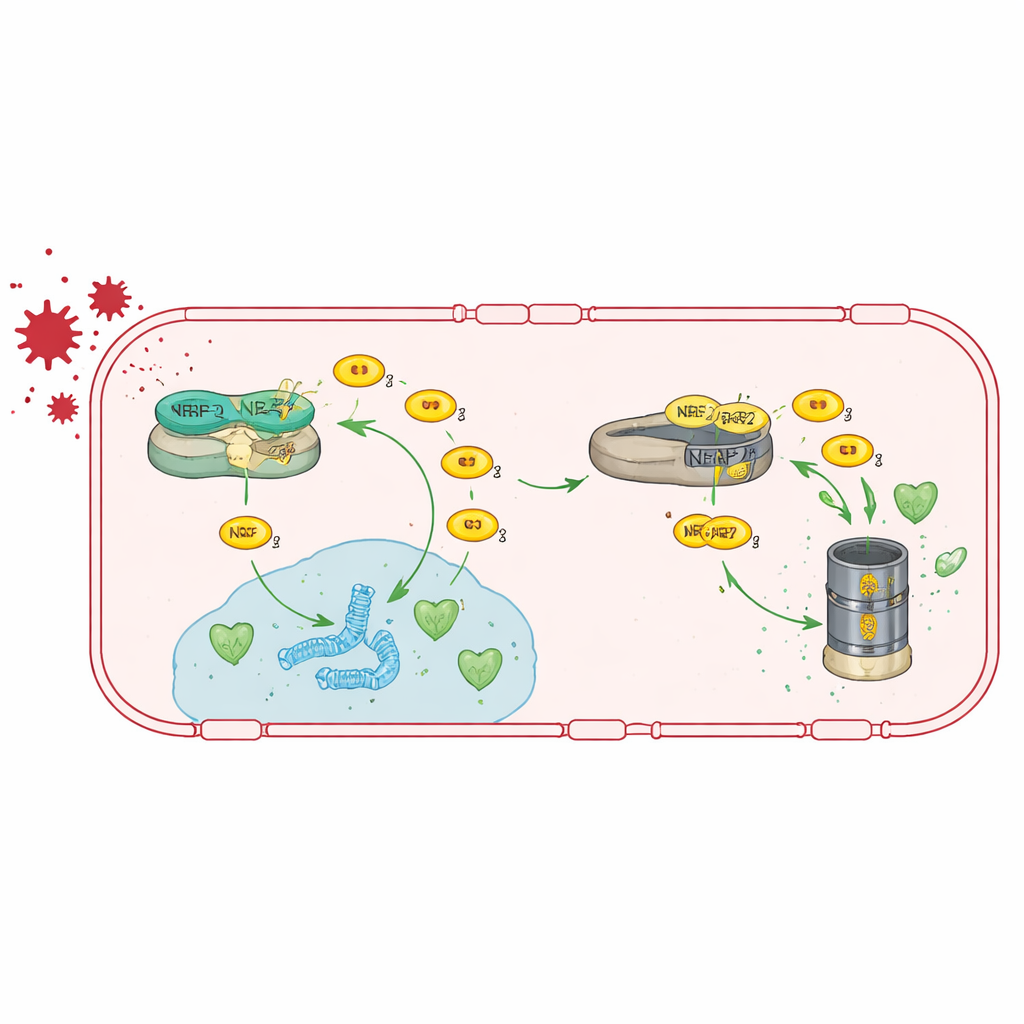
重新激活抗氧化通路
鉴于TRIM47主要通过提升NRF2活性发挥作用,研究团队测试了是否可以通过直接刺激NRF2来弥补TRIM47的缺失。他们给Trim47缺陷小鼠饲喂含有叔丁基氢醌(tBHQ)的饮食,这是一种已知能稳定NRF2并激活其靶基因的化合物。该处理恢复了脑内皮细胞中抗氧化基因的活性,使紧密连接基因表达接近正常,并减少了血–脑屏障的渗漏。更显著的是,它还使星形胶质细胞的活化恢复正常并挽救了动物在记忆测试中的表现,表明加强该抗氧化通路至少在小鼠中可以逆转血管和认知问题。
来自人类血液的线索与下一步
为将小鼠实验与人类疾病连接,研究者分析了数千名接受脑部MRI扫描的人的血样中与NRF2通路相关的蛋白水平。几种受NRF2调控的蛋白水平与脑小血管病的影像学标志有关,如围血管间隙增大和白质改变。这支持了TRIM47–NRF2信号改变在人类中也具有相关性的观点,并暗示这些蛋白可能成为疾病严重度或进展的生物标志物。
对脑健康的意义
综合来看,这项工作将TRIM47描绘为一种分子保镖,通过稳定NRF2抗氧化系统帮助脑血管抵御氧化损伤。当TRIM47缺失或功能受损时,血–脑屏障变弱,微小脑损伤积累,记忆开始衰退。重新激活NRF2通路可以修补屏障并恢复小鼠的认知,这突显了该信号轴作为血管性痴呆治疗靶点的潜力。尽管tBHQ本身不适合作为人用药物,但更安全的NRF2激活剂或模拟TRIM47保护作用的策略,未来或许能通过强化最小且最脆弱的脑血管来帮助维护脑健康。
引用: Delobel, V., Grenier, C., Boulestreau, R. et al. Endothelial TRIM47 regulates blood-brain barrier integrity and cognition via the KEAP1/NRF2 signalling pathway in mice. Commun Biol 9, 399 (2026). https://doi.org/10.1038/s42003-026-09628-5
关键词: 脑小血管病, 血–脑屏障, TRIM47, NRF2通路, 血管性痴呆