Clear Sky Science · zh
HCN2 通道中熵驱动与负协同结合所需的亚基间通路
心脏微小起搏器如何感知化学信号
每一次心跳以及许多大脑节律都依赖于位于细胞膜上开合的微观通道。这些称为 HCN 起搏通道的蛋白通道,不仅受电压控制,还受称为环核苷酸的小型信使分子的调节。本文探讨了一个看似简单但影响深远的问题:这些微小分子如何以协调的方式结合到 HCN2 通道上,以及该过程中的细微故障如何可能导致如癫痫等疾病?
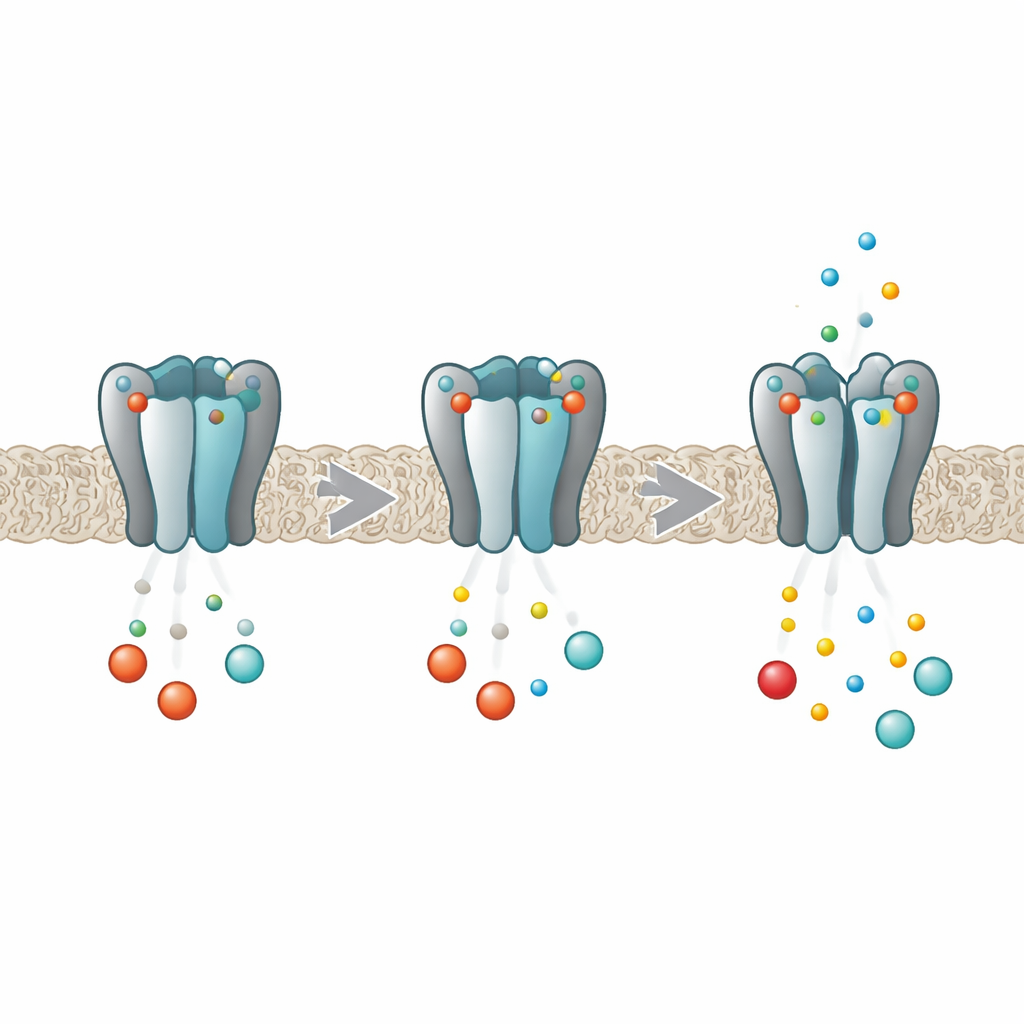
身体节律的分子调光器
HCN 通道像心脏和脑细胞电活动的调光开关。每个通道由四个相同的蛋白亚基组装而成,共同形成一个离子通过的中心孔。每个亚基深处都有一个能抓住环核苷酸(如 cAMP 和 cGMP)的口袋。当这些信使结合时,会使孔更容易打开,从而增强起搏电流。早期研究表明,在 HCN2 型中,结合并非在每个口袋独立发生;相反,四个结合位点彼此影响,使得第一个分子比后来的分子更容易结合,这种行为称为负协同。新研究旨在揭示四个亚基在这一过程中如何相互“对话”。
感知邻居的亚基
研究人员将计算机模拟与对分离的 HCN2 通道片段的实验测量相结合。通过长时间的分子动力学模拟,他们观察了通道尾部区域——包含环核苷酸口袋和连接到孔的所谓 C‑linker 的部分——在结合不同数量的 cAMP 或 cGMP 分子时如何弯曲和摆动。他们发现,当一个信使分子锁定在一个亚基时,它并不仅仅稳定该亚基本身。相反,它会微妙地改变相邻亚基的稳定性,有时使其更刚性,有时更灵活,尽管整体蛋白构型几乎没有变化。这些邻居之间的影响取决于被占据位点的数量及其在环上的位置,与负协同的预期一致。
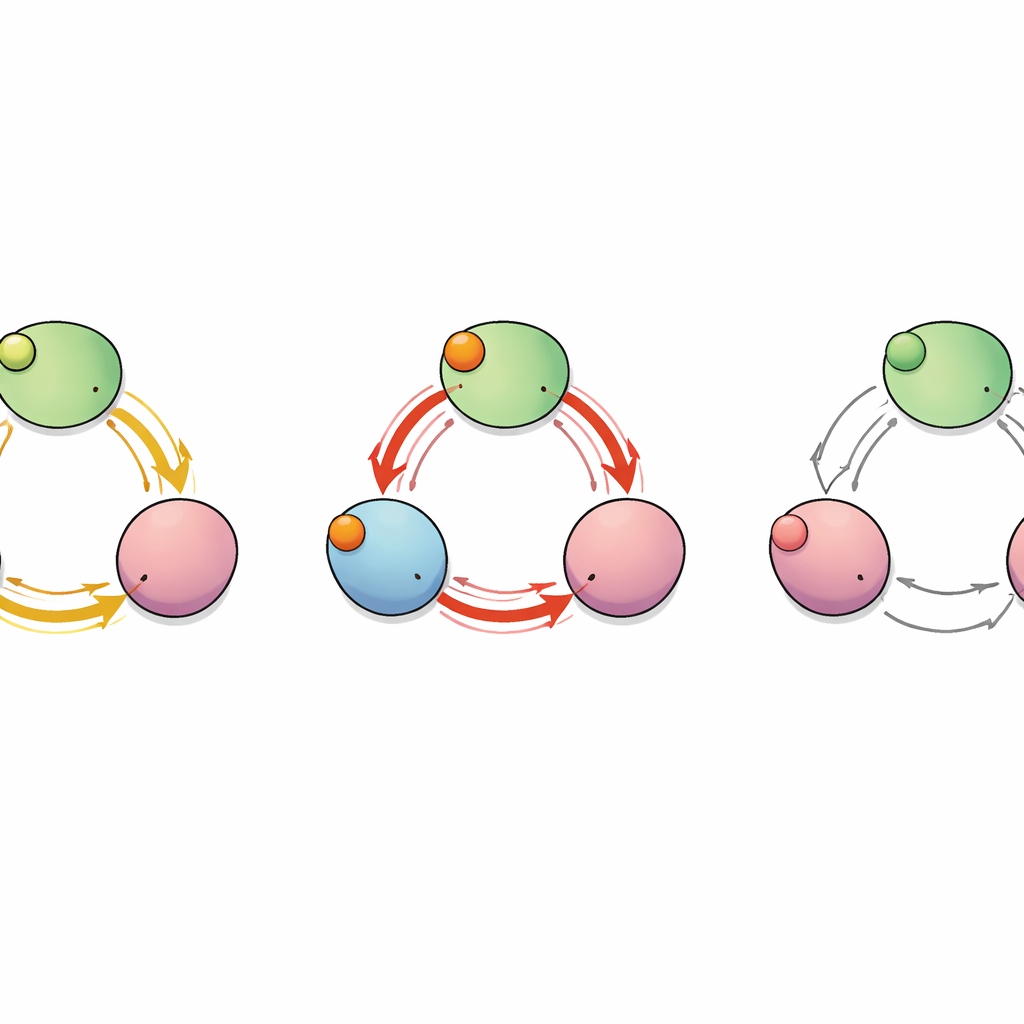
隐藏在亚基之间的通路
为了绘制结合“信号”如何在蛋白内传播,团队将通道视为一个相互作用氨基酸的网络。他们计算了在模拟过程中哪些残基以相关方式运动,并使用图论工具识别从结合口袋到控制孔的 C‑linker 段的最短且最有效的通信路径。该分析揭示了若干可能路线,但有两条尤为突出:一条局限于单个亚基内,另一条则从一亚基跳到相邻亚基。在这条亚基间路线中,一个单一残基——位于 488 位的谷氨酸(E488)——充当了关键枢纽,许多最短路径通过它,这表明它可能是协同结合的关键中继点。
打断对话的突变
作者随后转向对纯化的通道尾部进行实验以检验该通路的重要性。他们改变了 E488 以及路径到达处相邻亚基上的酪氨酸 459(Y459)。通过动态光散射,他们确认突变体蛋白仍能组装成四亚基复合体,但不再表现出正常蛋白在配体结合时亚基间出现的强烈收紧。等温滴定量热法(ITC)跟踪结合时的微小放热/吸热,显示了更大的变化:野生型 HCN2 表现为两个不同的结合事件——首先是一个由熵增加(内在运动增强)驱动的高亲和力步骤,随后是三个较低亲和力的步骤。相比之下,E488 或 Y459 的突变体仅显示出单一且亲和力温和的结合模式,缺乏有利的熵学提升,并失去了典型的负协同特征。
微妙的熵变为何重要
将这些发现拼接在一起,研究勾勒出 HCN2 通道的图景:一个由四个亚基组成的动态环,亚基间通过特定的“对话路径”相连。当第一个环核苷酸结合时,它通过 E488 和 Y459 调整环上远端部分的运动,使后续结合事件变得不那么有利,并微调孔的响应。这一效应不是由大的结构重排驱动,而是由内部柔性——即熵的变化——引起,这些变化在静态结构快照中不可见但对功能至关重要。破坏这条亚基间关键残基的突变会使对话沉默、消除负协同,并与如特发性全身性癫痫等疾病相关。对普通读者而言,结论是:心脏和大脑中维持生命的开关依赖于亚基间精妙配合的分子“低语”,理解这些低语有助于解释正常节律及其失常时的机制。
引用: Costa, F., Ng, L.C.T., Chow, S.S. et al. An inter-subunit path is required for entropically-driven and negatively cooperative binding of cyclic nucleotides in the HCN2 channel. Commun Biol 9, 362 (2026). https://doi.org/10.1038/s42003-026-09626-7
关键词: HCN2 离子通道, 环核苷酸结合, 负协同, 变构通信, 癫痫突变