Clear Sky Science · zh
一种小分子别构激活 SecA 依赖的分泌
将细菌的“装运码头”推入超速模式
细菌通过膜上的微小通道不断向外输出蛋白来维持生存。这些输出帮助它们构建细胞壁、分泌毒素并适应压力——这些过程是许多感染的核心。该研究报告了一种名为 HSI#6 的小分子,它做了一件不同寻常的事:不是抑制这种输出机器,而是将其切换为一种过度活跃、选择性降低的模式。理解这一开关如何工作既可以揭示新的抗菌策略,也可以为生物技术提供按需增强蛋白分泌的方法。
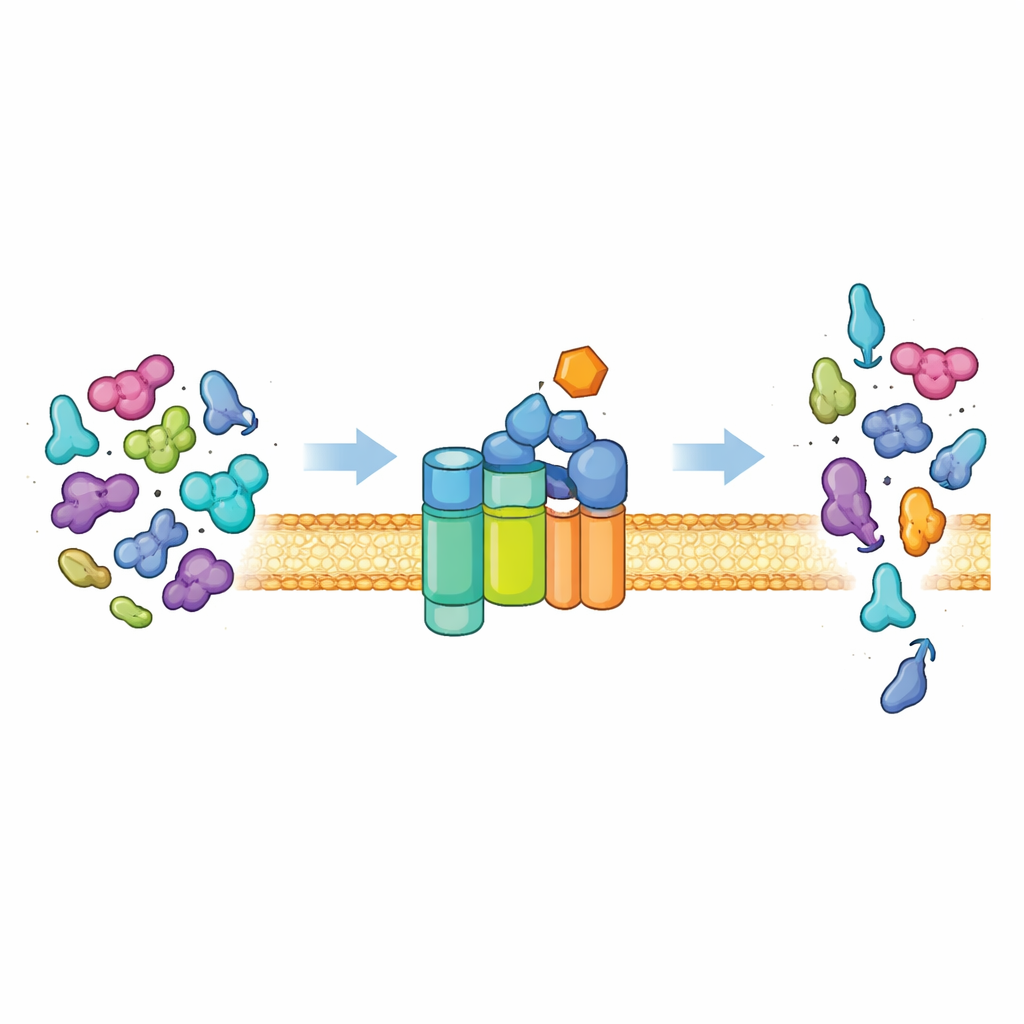
细胞的蛋白出口闸门
大多数细菌通过一种称为 Sec 系统的通用途径将蛋白运输出细胞。其核心是一个膜通道(SecYEG)和一个消耗细胞燃料(ATP)的动力蛋白 SecA,它推动未折叠的蛋白链穿过通道。在正常情况下,该系统很挑剔。它主要输出携带特殊地址标签(称为信号肽)的“前蛋白”,以及其主体中存在的额外特征。这些特征用于将 SecA 从一个安静、低活性的状态切换为强大的马达。只有呈现正确信号组合的蛋白才能解锁完整活性,从而确保细胞输出正确的货物并将普通细胞质蛋白保持在细胞内安全位置。
唤醒马达的小分子
研究人员在针对干扰细菌蛋白分泌和生长的化合物筛选中发现了 HSI#6。生化测试显示 HSI#6 以微摩尔亲和力直接结合 SecA,并改变其利用 ATP 的效率。在溶液中,它使 SecA 更紧地结合 ATP;当 SecA 结合到通道上时,HSI#6 既改善了 ATP 结合,又加快了 ATP 周转。这样的模式是别构激活剂的标志:一种在蛋白一处结合但改变远端活性的分子。与天然蛋白客户不同,HSI#6 无需作为货物来刺激马达——它只是调整 SecA 的内在动力学,使整个转位酶在催化上处于激活准备状态。
从选择性过滤器到不挑剔的纳米机器
一旦 HSI#6 结合,Sec 系统就不再坚持通常的输出标签。在试管实验中,该化合物大致使一种标准前蛋白的分泌量翻倍,并使该复合体对叠氮化钠(一种已知的 SecA 抑制剂)更具抵抗力。更引人注目的是,HSI#6 允许野生型机器移动完全缺乏信号肽的蛋白,以及那些通常位于细胞质的蛋白。在活细菌细胞中,使用基于碱性磷酸酶的报告子也观察到了相同效应:当将细胞质蛋白与分泌酶融合时,HSI#6 的存在导致分泌活性显著上升,而蛋白的表达量没有变化。换言之,HSI#6 有效地将输出与通常的客户识别检查解耦,使 Sec 系统成为针对任何足够未折叠蛋白的广泛作用输出泵。
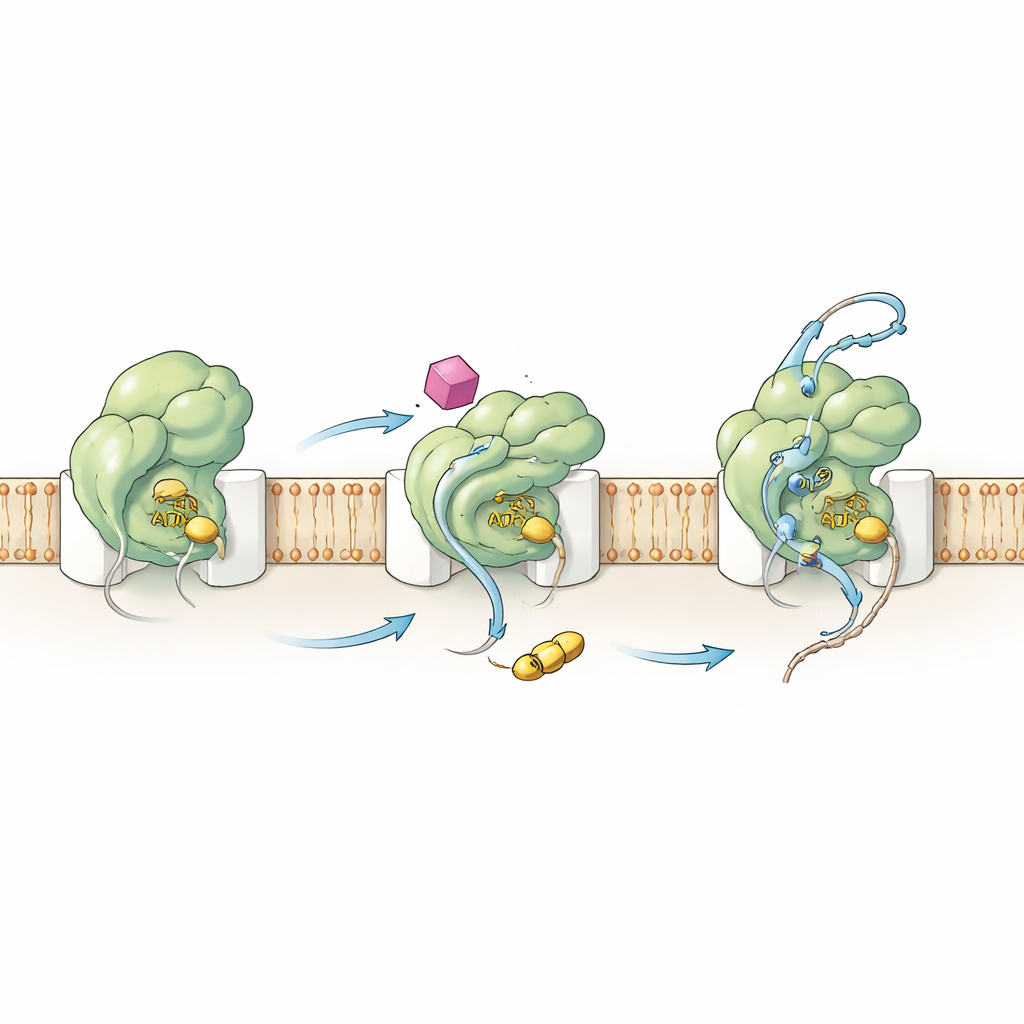
从内部改造马达
为了解 HSI#6 如何触发这种行为,团队检查了 SecA 的化学和运动学特征。动力学测量表明,该化合物将关键激活步骤上移:SecA–通道复合体在蛋白客户结合之前就变得具有催化活性。HSI#6 还帮助 SecA 释放消耗后的燃料(ADP),这通常是一个缓慢且限速的步骤,从而支持更快速的 ATP 循环。通过氢–氘交换质谱,作者绘制出 HSI#6 如何重塑 SecA 不同区域柔性的图谱。该化合物选择性地放松感知客户并与通道相连的一些区域,同时加固一个可能容纳其结合位点的支架区域。由此产生的运动模式类似于已被客户占据的“开启”状态,提示 HSI#6 稳定了一种激活形式——甚至可能偏好结合于通道的单体 SecA——而无需任何客户存在。
这对医学和生物技术的重要性
通过表明小分子可以别构激活 SecA 并剥夺其正常的客户选择性,这项工作揭示了控制这一中心细菌机器的新途径。对于传染病而言,这种被迫的、失控的分泌可能通过耗尽能量和扰乱其精细调控的输出程序来削弱病原体,使类 HSI#6 激活剂成为抗生素设计的有吸引力起点——或作为设计未来阻断相同调控特征的抑制剂的指导。对于生物技术而言,同一原理可被重新利用以增强有用重组蛋白的分泌,而无需工程化信号肽或复杂的基因改造。本质上,该研究证明了细菌的蛋白“装运码头”可以通过化学手段重新编程,为抗击微生物并将其用作微观工厂开辟了新途径。
引用: Sedky, H., Hamed, M.B., Krishnamurthy, S. et al. A small molecule allosterically activates SecA dependent secretion. Commun Biol 9, 368 (2026). https://doi.org/10.1038/s42003-026-09623-w
关键词: 细菌蛋白分泌, SecA 转位酶, 别构激活, 小分子调节剂, 抗菌药物发现