Clear Sky Science · zh
长非编码RNA P4HA2-AS1 通过 TRIM32 介导的 K63 泛素化激活 ULK1 并扰乱自噬,推动肾间质纤维化
为什么肾脏瘢痕很重要
慢性肾脏病影响全球数亿人,常常在无声无息中进展,直至透析或移植成为维持生命的唯一途径。推动这一衰退的核心过程是纤维化——正常的肾组织逐渐被僵硬且不具功能的物质所取代。本研究提出了一个简单但至关重要的问题:肾细胞内哪些分子开关会把组织推向有害的瘢痕形成,是否有办法把这些开关关闭?
肾细胞中被忽视的RNA开关
我们的肾脏通过复杂的微小小管网络来过滤血液。当这些小管因尿路梗阻、高血糖或急性缺血等损伤时,细胞间可能会沉积瘢痕组织。研究者对多种损伤小鼠肾脏与健康肾脏进行了转录组测序,以比较基因表达变化。他们发现一种鲜为人知的分子P4HA2-AS1(一种不编码蛋白质的长非编码RNA)在受损并形成瘢痕的肾脏以及实验室受压的人的肾细胞中持续升高。该RNA主要位于细胞的胞质部分,提示它可能在该处调控其他蛋白质。
下调该RNA以保护肾脏
为检验P4HA2-AS1是旁观者还是损伤的主动驱动因子,团队在小鼠和培养的人肾细胞中降低了其水平。在一个经典的一侧输尿管结扎造成长期梗阻的鼠模型中,通过靶向病毒递送降低该RNA减轻了多项纤维化特征:小管更完整、细胞间胶原及其他瘢痕蛋白减少,血液中的肾功能指标改善。在培养的人肾细胞中,降低P4HA2-AS1也减弱了强效促纤维化因子TGF‑β的作用,导致纤维连接蛋白、胶原和其他促纤维化因子的产生减少。这些实验表明该RNA不仅是损伤的标志物,而是积极促进纤维化的因素。
自噬:从家务维护到有害过程
研究者随后探查该RNA如何造成损害。基因表达和成像数据指向自噬——细胞内的回收系统,用于分解老化的蛋白质和细胞器。在正常情况下,自噬属于健康的清理与维护过程,但当长期过度激活时,会将受伤的肾脏推向不适应性的修复与纤维化。在受压的肾细胞中,P4HA2-AS1 提升了自噬通量,导致回收囊泡的积聚。当阻断该RNA时,过度活跃的自噬在细胞和梗阻小鼠的肾脏中均回落至接近正常的水平。缺失 ULK1(一种自噬启动的关键酶)的鼠也免于纤维化,并且在这些动物中过表达 P4HA2-AS1 无法再加剧损伤,明确将该RNA的作用与自噬通路联系起来。
三部分分子链条
进一步研究中,团队使用生化“捕捞”技术鉴定出与 P4HA2-AS1 实际结合的蛋白。其中一个突出的结合者是 TRIM32,一种向其他蛋白添加小分子“标签”即泛素的酶。该RNA与 TRIM32 结合并保护其免于降解,从而提高其在肾细胞内的水平。被稳定的 TRIM32 进而向 ULK1 附加特定类型的泛素链。这种泛素链并不将 ULK1 送去降解,而是像一种“强化”信号,增强 ULK1 启动自噬的能力。当科学家在小鼠中去除 TRIM32 或在肾细胞中沉默它时,纤维化和过度自噬均减少。在已被阻断 P4HA2-AS1 的细胞中重新引入 TRIM32 部分恢复了纤维化反应,表明该酶是链条中的关键中间环节。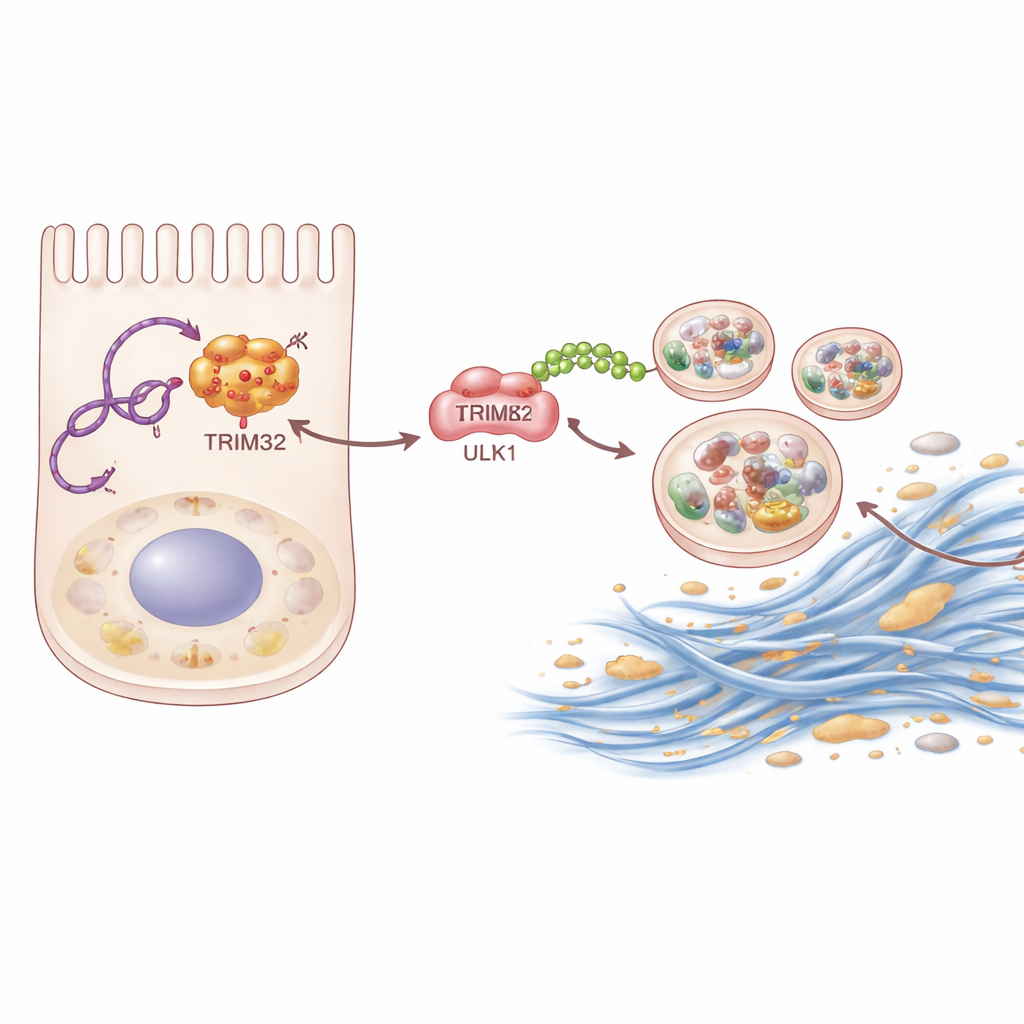
朝向更柔软肾脏的新途径
综上所述,该研究揭示了一条此前未知的分子通路,将长非编码RNA、蛋白质标记和细胞回收系统联系到肾脏瘢痕组织的积累。在受损肾脏中,P4HA2-AS1 上调,稳定 TRIM32,增强 ULK1 活性,并将自噬推向超出其有益范围的状态,最终促进促纤维化蛋白的沉积和功能丧失。对非专业读者而言,核心信息是肾脏纤维化并非不可避免的黑箱:它由可识别的开关驱动,并有望成为药物干预的目标。针对 P4HA2-AS1–TRIM32–ULK1 轴——降低异常 RNA、抑制 TRIM32 或微调 ULK1 活性——未来或许可以开发出减缓或阻止慢性肾脏病进展的新疗法。
引用: Pan, Z., Xiao, F., Hu, W. et al. LncRNA P4HA2-AS1 drives renal interstitial fibrosis via trim32-mediated k63 ubiquitination of ULK1 and autophagic dysregulation. Commun Biol 9, 339 (2026). https://doi.org/10.1038/s42003-026-09618-7
关键词: 慢性肾脏病, 肾脏纤维化, 自噬, 长链非编码RNA, 肾小管