Clear Sky Science · zh
逆转录酶抑制剂使胎鼠睾丸在体外产生具有生育能力的精子细胞
将早期生殖细胞转化为能工作的精子
不孕症治疗和基础研究都依赖于弄清睾丸中未成熟生殖细胞如何转变为精子。这项研究表明,现在可以促使在胚胎性别刚确定后采集的非常早期胎鼠睾丸,在培养皿中完成这一转变。通过精细调整化学环境和氧气水平,研究者不仅产生了成熟的类似精子细胞,而且还用这些细胞创造了健康、有生育能力的后代。
为何早期睾丸发育难以复制
在体外生长精子以前已用新生或更大龄小鼠的睾丸组织取得过进展,但效率低下,使用更早期胎儿组织的尝试大多失败。在这一早期阶段,睾丸仍在搭建其内部结构,生殖细胞在DNA包装与表观标记方面发生剧烈变化。在培养皿中重现这种复杂的时序极具挑战,从胚胎发育第12.5天左右采集的睾丸(性别刚确定不久)出发的培养往往只能走到早期步骤,难以继续进展。
借用抗病毒药保护正在发育的细胞
团队关注了一个被忽视的障碍:称为逆转转座子的可移动DNA元件,它们能复制并插入基因组中新位点。在体内的正常睾丸中,这些元件受到严格控制,尤其是在生殖细胞中。然而在培养中,作者发现逆转转座子的活性明显升高,而细胞自身的防御基因表达减弱。这种失衡与精子发育不良相关。由于逆转转座子依赖一种类似某些病毒的逆转录酶,研究者测试了几种原本设计用于抑制逆转录酶的药物。一种由三种药物组成的特定混合物,称为AEC,大致将精子发生细胞的比例提高了一倍,并使新生睾丸培养中单倍体、类似精子的细胞比例增加了三倍以上,与未处理对照相比有显著提升。
从微小的胎儿睾丸到功能性精子
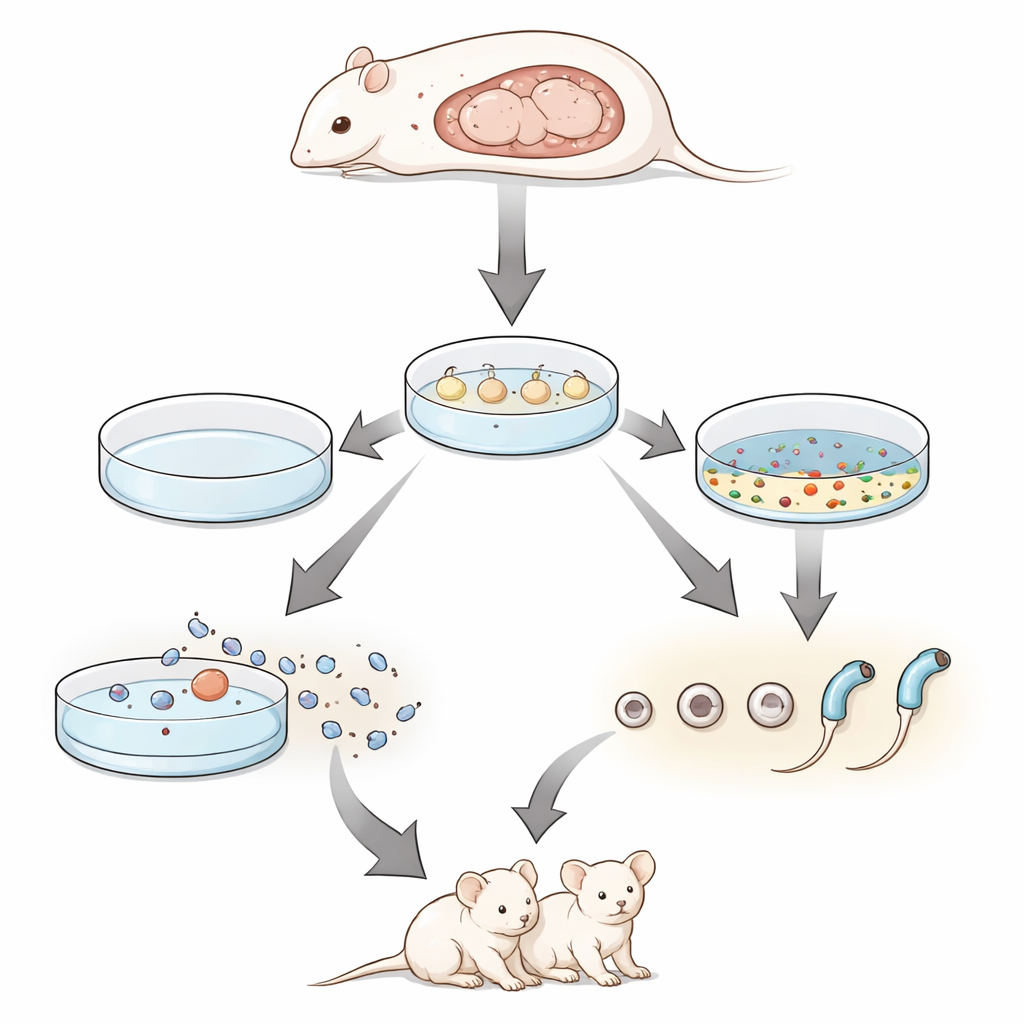
在这套药物组合的帮助下,科学家们转向胎儿睾丸。在接近出生的组织中,抑制剂促进了高级精子细胞的出现。更引人注目的是,当他们培养发育到第12.5天的胚胎睾丸——此前从未在体外完成整个精子发生的阶段——现在能够生成圆形和延长的精子细胞。最大收益来自将抑制剂混合物与更接近体内发育环境的低氧气氛结合。在这些低氧条件下,大约三分之一的组织区域显示出高级生殖细胞发育的标志,并且可以从培养物中回收带有尾部的精子。
检验实验室制备的精子细胞是否真正有效
为确定这些体外产生的细胞是否真正具备功能,团队采用了一种称为圆形精子细胞注射的技术。他们从培养的胎儿睾丸中分离出圆形精子细胞,并将其注入经轻度激活的鼠卵中。得到的胚胎被移植到代孕母鼠体内。从仅两块培养的睾丸组织碎片中,该程序产生了多只活仔,其中许多携带表明其培养来源的荧光标记基因。当这些第一代动物被允许交配时,它们生育了正常规模的、健康的第二代后代,证明实验室来源的精子细胞不仅能支持出生发育,还能维持完全的生育能力。
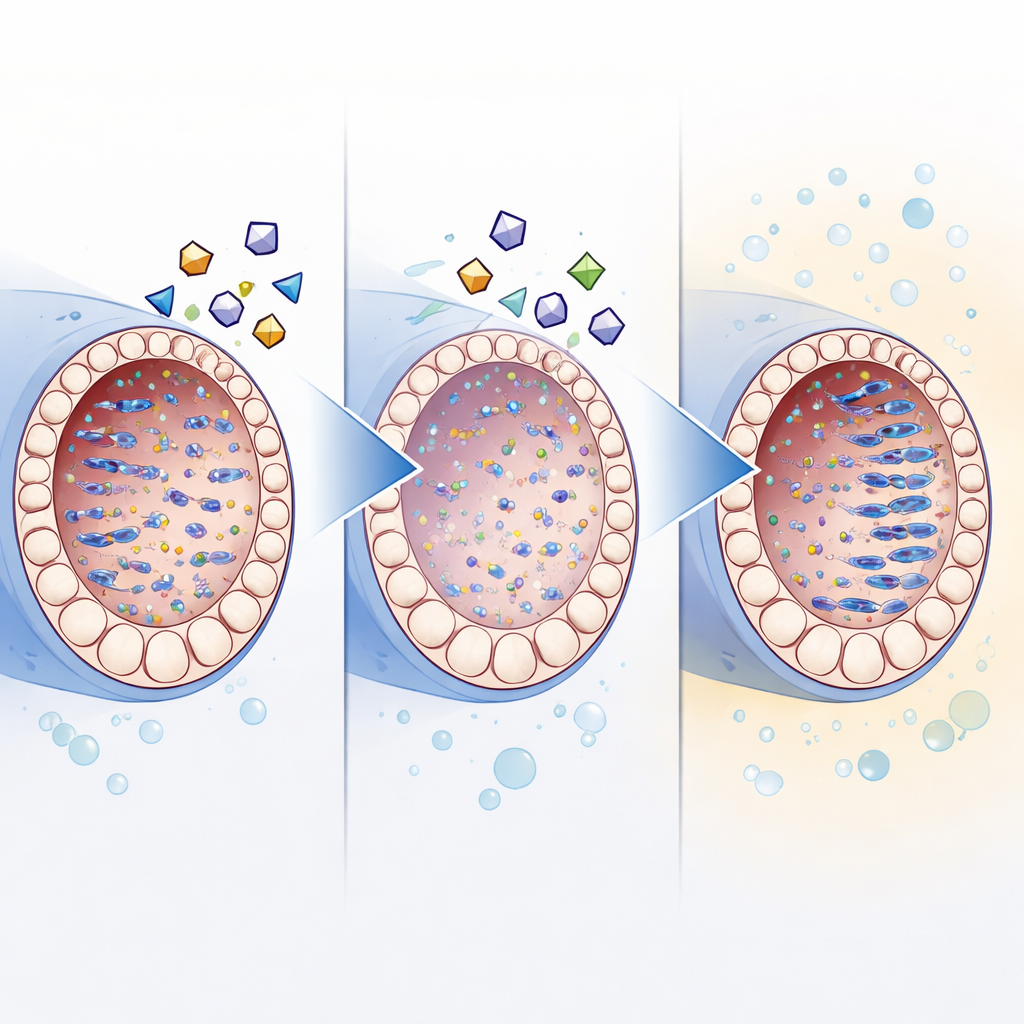
阻断可移动DNA可能如何助力未来疗法
进一步实验支持了逆转录酶抑制剂主要通过抑制可移动DNA发挥作用的观点。与同龄在体睾丸相比,培养睾丸显示出更高水平的逆转转座子蛋白和其DNA的额外拷贝,同时细胞天然的沉默机制表达下降。加入抑制剂鸡尾酒减少了这种积累,并同时改善了生殖细胞的成熟。尽管这些药物稍微减慢了整体组织生长,但用血清类添加物试图抵消这一点并未提高精子产量,表明生长与正确分化之间必须谨慎平衡。
这对生殖科学意味着什么
这项工作表明,即便是非常未成熟的胎儿睾丸,只要环境保护其基因组并模拟子宫内的重要条件,就已具备构建功能性精子工厂的所有成分。通过将类抗病毒药物与低氧结合,研究者建立了一种能够从迄今测试的最早阶段之一重现完整精子发生的培养系统,并产生出能够正常生长和繁殖的后代。尽管该研究在小鼠中进行,离临床应用还很遥远,但它为研究雄性生殖细胞发育的最早步骤打开了一个强有力的窗口,并提供了可能在未来帮助保存或恢复那些在生命早期受损的生殖细胞的生育能力的线索。
引用: Nishida, M., Ono-Sunagare, Y., Kato, S. et al. Reverse transcriptase inhibitors enable the generation of fertile spermatids from fetal mouse testes in vitro. Commun Biol 9, 329 (2026). https://doi.org/10.1038/s42003-026-09613-y
关键词: 体外精子发生, 胎儿睾丸培养, 逆转录酶抑制剂, 逆转转座子, 男性生育力