Clear Sky Science · zh
肥胖通过肝源外泌体miR-122-5p诱导的Leydig细胞铁死亡损害精子发生
体重与生育力为何有关联
人们谈论肥胖时通常关注心脏病和糖尿病,但肥胖也会悄然损害男性生育力。这项在小鼠身上的研究揭示了一种令人意外的机制:高脂饮食可以降低睾酮并破坏精子生成——肝脏将微小的“信息泡”释放入血,触发睾丸中生成激素的细胞发生一种特殊的细胞死亡。理解这种隐秘的肝—睾通讯有助于解释为何超重男性常出现低睾酮和不育,并可能指出新的治疗靶点。
器官间的隐秘通信
我们的器官通过激素和其他化学信使不断交流。其中一种通信方式是外泌体——细胞释放的纳米级小泡,携带脂类、蛋白质和遗传物质。研究人员用正常饮食或导致肥胖、胰岛素抵抗和血糖控制不良的高脂饮食喂养小鼠。肥胖小鼠的睾丸较小且活性下降:精子数量、睾酮水平以及产生精子的曲细精管的大小和数量均减少。检测睾丸中的关键细胞标记显示,生成睾酮的Leydig细胞减少,早期和晚期精子细胞也减少,证实整个造精“流水线”受损。 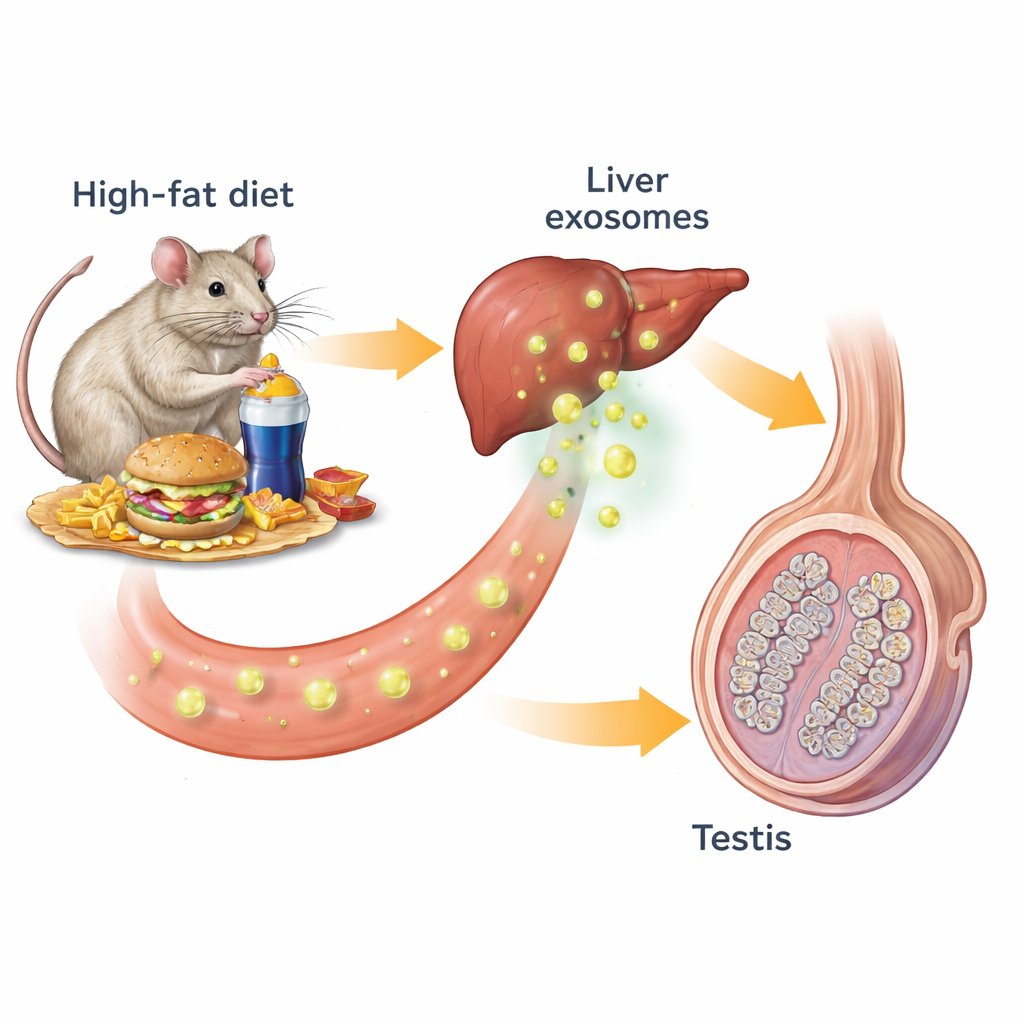
外泌体扩散损伤
为检验循环外泌体是否参与驱动这种损伤,科学家们从肥胖和瘦小鼠的血液中分离外泌体。将来自肥胖小鼠的外泌体注入健康瘦小鼠,便足以复现许多问题:受体出现代谢异常的迹象,睾酮下降,精子数和睾丸结构恶化。用一种名为GW4869的药物抑制肥胖小鼠的外泌体释放,能够在很大程度上逆转这些变化,恢复精子数、睾酮水平和正常的睾丸结构。这些结果表明,血液中的外泌体并非旁观者;它们积极携带来自肥胖的有害信号到生殖系统。
一种有毒的细胞死亡形式
研究团队随后探究外泌体对Leydig细胞究竟做了什么。他们关注铁死亡,这是一种由铁驱动的细胞死亡形式,特征为铁积聚、脂类的氧化损伤和线粒体——细胞的能量工厂——受损。在肥胖小鼠及给予肥胖来源外泌体的健康小鼠中,睾丸显示较高水平的铁和丙二醛(脂类损伤的副产物),并在电子显微镜下见到明显的线粒体损伤。用阻断铁死亡的化合物Ferrostatin-1处理肥胖小鼠,可以保存Leydig细胞、提高睾酮和精子数量,并改善线粒体健康。在细胞培养中,同样的药物保护分离的Leydig细胞免受肥胖动物外泌体诱导的死亡和氧化应激。总体上,这些实验揭示铁死亡是肥胖与睾酮生成失败之间的关键联系。
肝脏的信息与SCD2开关
为追踪外泌体内部的信息,研究人员对其小RNA货物进行测序,发现一种特定的微小RNA——miR-122-5p,在肥胖小鼠的外泌体中显著升高。这种microRNA在肝脏及肝源外泌体中尤为丰富,且这些肝源外泌体可以被追踪到睾丸。当在外泌体中实验性降低miR-122-5p水平时,Leydig细胞对铁死亡的易感性降低,睾酮生成改善,尽管动物在代谢上仍然不健康。进一步测试表明,miR-122-5p直接抑制一个名为Scd2的基因,该基因有助于将某些脂肪转化为能保护细胞免受氧化损伤的形式。在Leydig细胞中降低Scd2使其更易发生铁死亡并降低睾酮,而在肥胖小鼠中提高Scd2则部分恢复了激素水平、精子生成和线粒体结构。 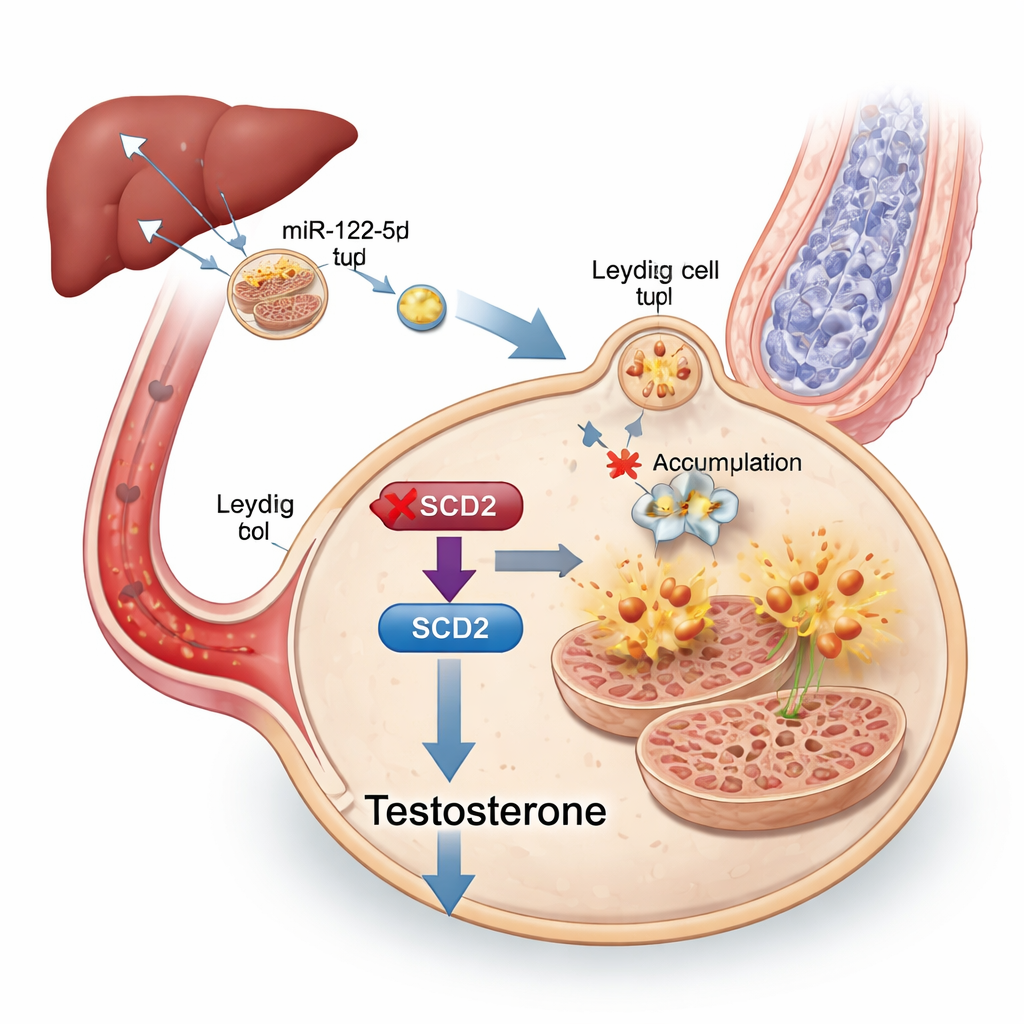
对人类健康的意义
简而言之,这项工作表明高脂饮食可促使肝脏将过量的miR-122-5p装入外泌体。这些外泌体通过血液到达睾丸,在那里该microRNA关闭Leydig细胞中负责“脂类处理”的Scd2开关。没有Scd2,这些细胞累积铁驱动的氧化损伤,发生铁死亡,产生更少的睾酮,最终无法支持同样数量的健康精子。尽管这项研究在小鼠中进行,仍需在人类中得到证实,但它将肝源外泌体、miR-122-5p、铁死亡和Scd2确定为有前景的生物标志物和潜在药物靶点,用于治疗与肥胖相关的男性不育——并再次强调长期高脂饮食会悄然侵蚀生殖健康的另一原因。
引用: Wang, N., Zhang, B., Chen, T. et al. Obesity impairs spermatogenesis via Leydig cell ferroptosis induced by liver-derived exosomal miR-122-5p. Commun Biol 9, 318 (2026). https://doi.org/10.1038/s42003-026-09612-z
关键词: 肥胖与男性生育力, 睾酮, 外泌体, Leydig细胞, 铁死亡