Clear Sky Science · zh
组蛋白去甲基化酶 KDM7A 负向调控促纤维化巨噬细胞极化及肺纤维化进展
为什么肺部瘢痕与每个人都有关
当肺部形成顽固的瘢痕,呼吸就会成为日常的挣扎。该疾病被称为肺纤维化,影响数以百万计的人,目前尚无治愈方法——只有能减缓损伤进展的药物。在这项研究中,研究者发现了存在于一种称为巨噬细胞的免疫细胞内、此前被隐藏的分子“刹车”,它有助于抑制肺部瘢痕的形成。理解这一刹车机制可能为新的治疗方案打开大门,不仅针对肺纤维化,也可能对其他伴随有有害瘢痕和失控炎症的疾病带来启示。
一个会变形的免疫细胞的故事
巨噬细胞是巡逻组织、清除碎屑并帮助修复损伤的一线免疫细胞。但它们也是“变形者”:在某些情形下它们成为促炎战士,而在另一些情形下则变为促进伤口愈合的细胞,可能会驱动瘢痕形成。一类特定的促瘢痕细胞,被称为促纤维化巨噬细胞(Fib-Mac),与肺纤维化密切相关。这些细胞产生能激活成纤维细胞的分子,后者随后沉积过量的胶原和其他基质成分,逐步使肺变硬。作者想弄清楚巨噬细胞内部的基因“设定”如何决定它们是成为这种危险的 Fib-Mac,还是保持更为平衡、具有保护性的状态。
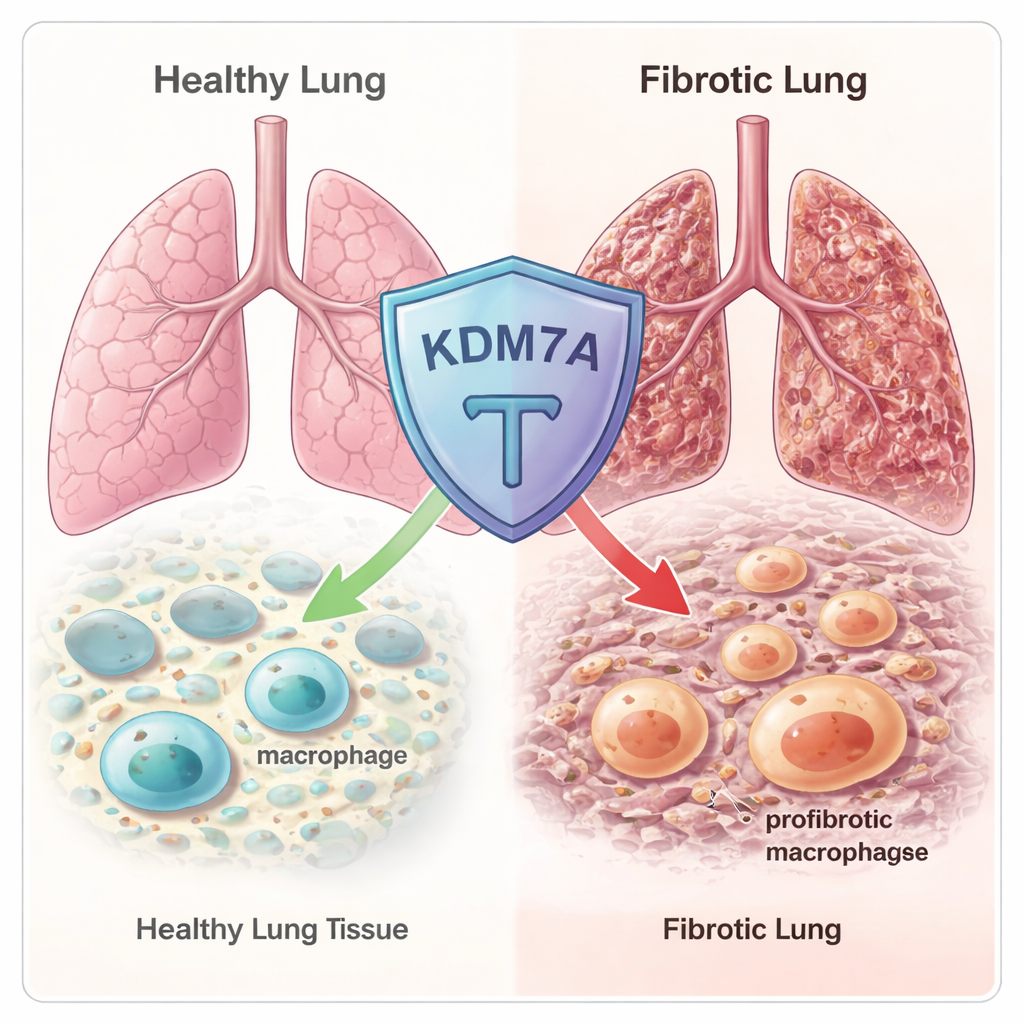
隐藏在基因组中的表观遗传刹车
团队首先扫描了数百种已知的表观遗传调控因子——这些蛋白微调 DNA 的包装紧密程度以及哪些基因被打开或关闭。通过在人和小鼠巨噬细胞中进行 RNA 测序,他们发现当巨噬细胞被推动向促纤维化、伤口修复状态时,一种名为 KDM7A 的酶被强烈激活。KDM7A 是一种“组蛋白去甲基化酶”:它从缠绕 DNA 的组蛋白上去除某些化学标记。这一模式提示 KDM7A 可能充当内在的反馈刹车,正是在巨噬细胞开始偏向促瘢痕身份时被激活。
为验证这一点,研究者使用缺失 Kdm7a 基因的小鼠,并用化疗药物博来霉素诱导肺损伤,这是研究肺纤维化的常用模型。损伤早期,正常与缺失 Kdm7a 的动物肺组织看起来相似。但到第三周,缺乏 Kdm7a 的小鼠显示出更广泛的瘢痕形成、细小气囊塌陷以及更高的 Ashcroft 评分(用于量化纤维化)。与纤维化相关的胶原生成等通路相关基因在这些敲除小鼠中更为活跃,证实了失去 Kdm7a 会使肺更易于形成持久且有害的瘢痕。
KDM7A 如何引导巨噬细胞远离促瘢痕命运
作者使用单细胞 RNA 测序放大观察受损小鼠的单个肺细胞。他们发现,在缺失 Kdm7a 的情况下,肺基质中的一个特定巨噬细胞亚群显著扩增并呈现出强烈的 Fib-Mac 特征,表达诸如 Arg1、Spp1 和 Trem2 等基因。进一步在培养巨噬细胞中的实验显示,去除 Kdm7a 提升了 Fib-Mac 标志基因并重编程细胞代谢,朝向支持胶原生成和持续活化的通路。换言之,KDM7A 通常抑制驱动巨噬细胞进入促纤维化状态的基因与代谢程序。
深入研究时,研究者识别出该刹车系统的一个关键伙伴:名为 TLR8 的感受蛋白,它能探测免疫细胞内的 RNA 片段。他们发现 KDM7A 通过从 Tlr8 附近的增强子区域去除抑制性化学标记(H3K27me2)来帮助维持 Tlr8 基因的开启状态。当 Kdm7a 被禁用时,该抑制性标记积累,Tlr8 水平下降,Fib-Mac 特征增强。直接降低巨噬细胞中的 Tlr8 也会推动它们走向促纤维化身份,而激活或过表达 TLR8 即使在缺乏 Kdm7a 时也能将它们拉回。这将 KDM7A–TLR8 通路置于保护肺部免受过度瘢痕形成的分子电路中心。
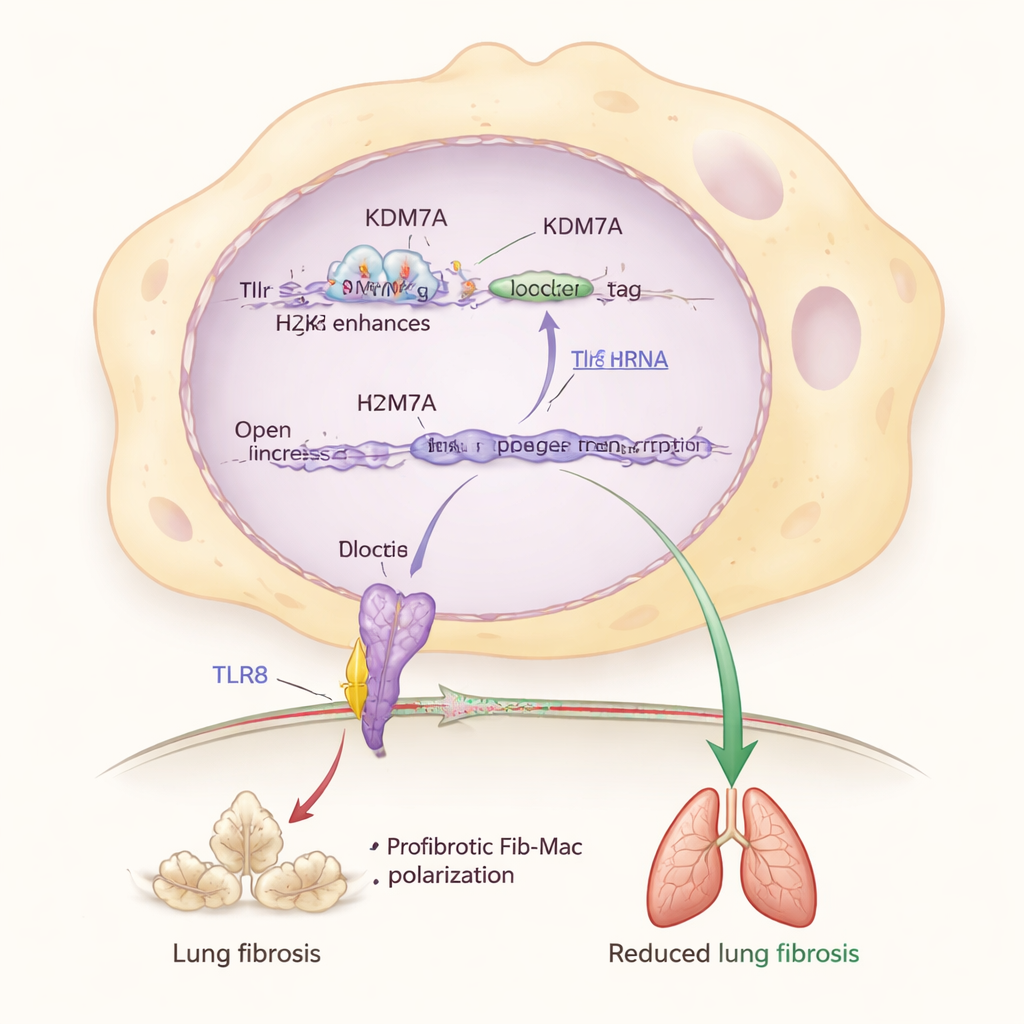
从老化的肺到人类疾病
为将这些发现与人类联系起来,团队检查了患有纤维性肺病患者的肺组织。与无疾病的对照组织相比,纤维化肺含有更多带有 Fib-Mac 标志的巨噬细胞,但这些细胞的 KDM7A 和 TLR8 水平明显降低。对特发性肺纤维化患者现有单细胞数据集的再分析证实了这一模式:随着 Fib-Mac 特征上升,KDM7A 表达下降。研究者还挖掘了大型小鼠图谱,发现雄性小鼠巨噬细胞中 Kdm7a 和 Tlr8 的表达随年龄下降,反映出年长男性肺纤维化风险更高的现象。这提示年龄和性别相关的 KDM7A–TLR8 刹车减弱可能部分解释谁更易受严重肺部瘢痕的影响。
这对未来治疗意味着什么
简言之,这项工作表明我们的免疫系统自身携带一种内在的安全机制,可防止有益的修复细胞过度活跃并转变为导致永久瘢痕的推动者。KDM7A 通过 TLR8 抑制巨噬细胞锁定为促纤维化模式,从而有助于在损伤后维持肺组织灵活且功能性的状态。当该系统因基因缺失、衰老或其他因素失效时,巨噬细胞更容易成为“瘢痕放大器”,加重纤维化。通过揭示这一表观遗传刹车,研究指向了新的治疗策略:未来或可开发增强 KDM7A 活性、模拟其作用或谨慎激活 TLR8 的药物,以补充现有的抗纤维化治疗,提供更好的保护,防止进行性、危及生命的肺部瘢痕。
引用: Funagura, N., Koga, T., Etoh, K. et al. Histone demethylase KDM7A negatively regulates fibrotic macrophage polarization and lung fibrosis progression. Commun Biol 9, 309 (2026). https://doi.org/10.1038/s42003-026-09610-1
关键词: 肺纤维化, 巨噬细胞, 表观遗传学, KDM7A, TLR8