Clear Sky Science · zh
通过抑制AAV诱导的凋亡通路活化,ATM抑制提高敲入效率
让基因编辑更有效
CRISPR 基因编辑有望用于治疗遗传病、培育更强壮的作物并提供强大的研究工具。但它最有价值的技能之一——在基因组的特定位点精确插入新 DNA,称为“敲入”——仍然效率不高。本研究探讨了为何某些细胞比其他细胞更容易接受新 DNA,并揭示了一种促使细胞更频繁执行精确编辑的方法,尤其是在使用腺相关病毒(AAV)这一领先的基因治疗载体时。
实时观察 DNA 修复
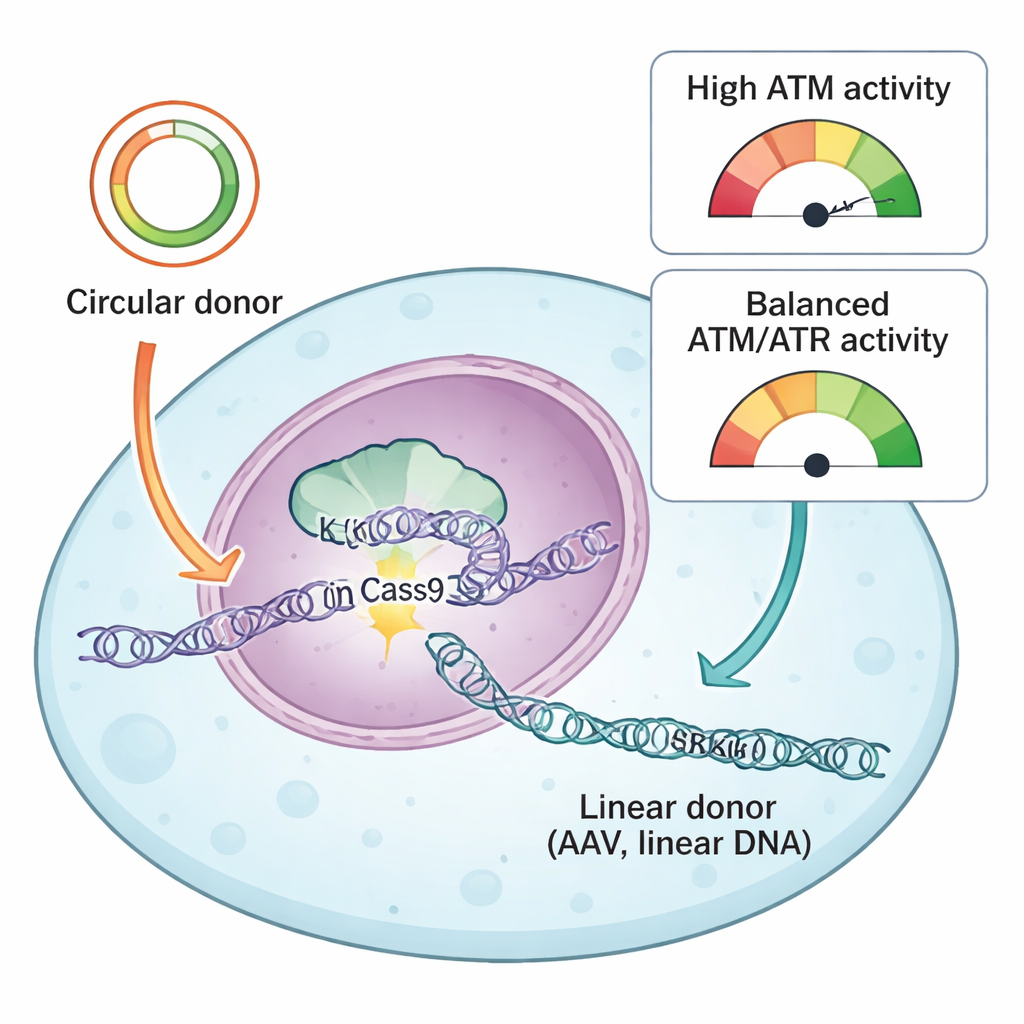
为了解什么有助于或阻碍精确基因插入,研究人员在小鼠胚胎干细胞内构建了一个精密的“仪表盘”。这个三重报告系统使用三种荧光标记在同一细胞中追踪 CRISPR 是否切割了 DNA、是否发生了精确敲入、以及细胞是否通过一种更粗糙的修复方式将供体 DNA 粘接进位点。通过用流式细胞术读取不同颜色组合,他们可以将基于模板的干净编辑与易出错的插入和未编辑细胞区分开来。这种并列跟踪使他们能够比旧的基于 PCR 的检测更高分辨率地描绘不同 DNA 修复通路对每种结果的贡献。
两种供体 DNA,两种迥异的反应
团队比较了两种常用的用于指导 CRISPR 修复的供体 DNA 类型:环状质粒和线性来源于 AAV 的 DNA。两者都带有匹配的“同源臂”,告诉细胞在哪里插入新序列,但它们以不同的物理形态进入细胞。环状质粒是闭合的双链 DNA 环,而 AAV 供体通常以单链线性分子到达。借助他们的报告系统和一个针对 DNA 损伤反应蛋白的药物库,作者发现一个关键蛋白 ATR 对两种供体的成功敲入都普遍必需。抑制 ATR 会显著减少精确插入,而通过 KEAP1–NRF2 途径温和增强 ATR 活性则使敲入更高效,尤其是在使用 AAV 供体时。
当 DNA 保护机制适得其反
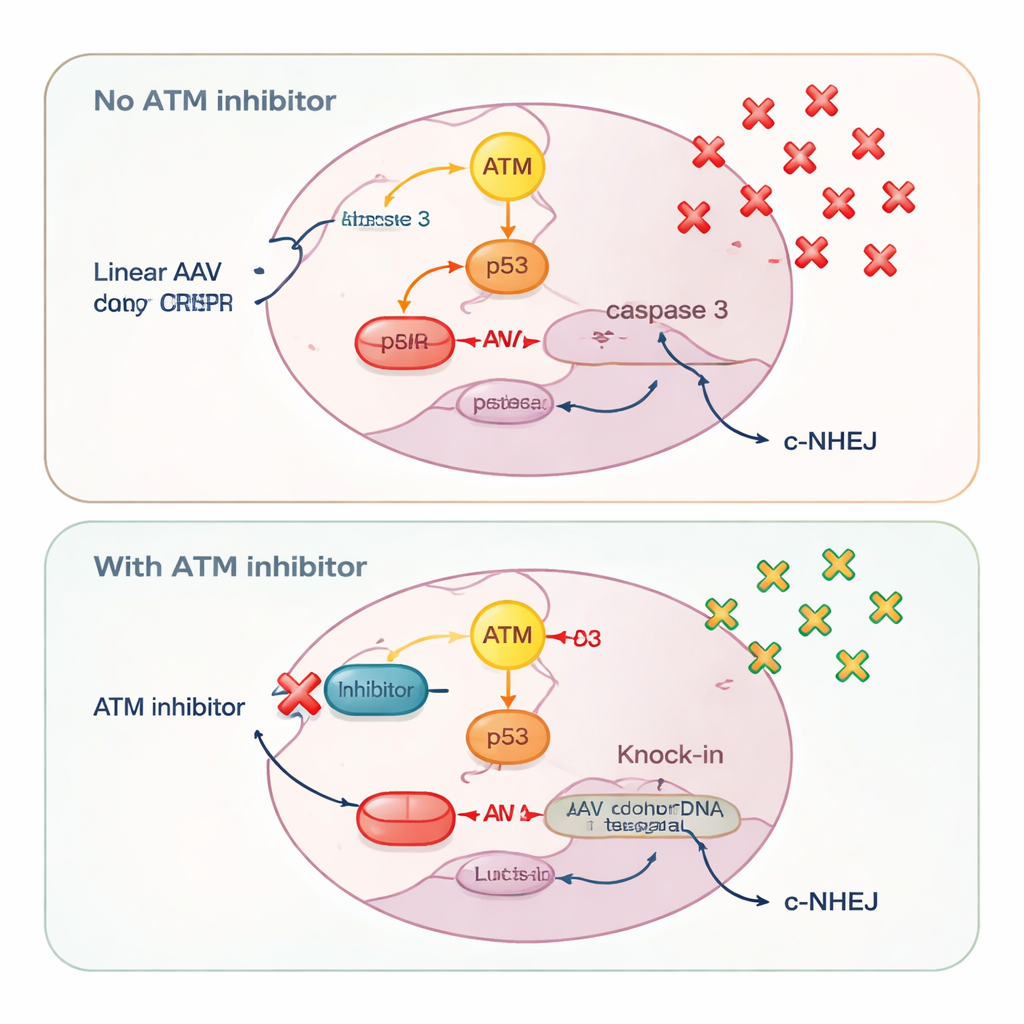
另一个 DNA 损伤传感器 ATM 表现出显著的供体依赖性。对于环状质粒供体,抑制 ATM 会减少精确敲入和经端连接介导的插入,这符合其在协助细胞修复双链断裂方面的经典作用。但对于线性 DNA——无论来自 AAV、自互补 AAV,还是被切成直段的质粒——ATM 抑制则产生相反效果:它提高了敲入效率。研究人员将该效应追溯到细胞如何解读大量线性 DNA 的冲击。高剂量 AAV 强烈激活 ATM,进而启动 p53 和半胱天冬酶 3,这些是程序性细胞死亡的核心执行者。摄取大量供体 DNA 的细胞(因此最有可能完成成功敲入)也是最可能被这一报警系统清除的细胞。
拯救最有条件的细胞
通过加入 ATM 抑制剂,科学家们抑制了 ATM–p53–半胱天冬酶 3 的死亡通路。这保护了携带大量供体 DNA 的细胞,使更多此类细胞存活足够长的时间以完成精确敲入。对病毒基因组拷贝数的测量证实,ATM 抑制增加了细胞内保留的 AAV 分子数量。与此同时,ATM 阻断略微减弱了一条快速且钝性的修复途径——经典非同源末端连接(c-NHEJ),这可通过 DNA-PK(该通路的核心酶)激活的降低看出。削弱这一竞争性修复选项促使更多 CRISPR 切割朝向同源依赖的敲入而不是忽略供体模板的快速修补。
这对未来基因治疗意味着什么
对非专业读者而言,信息是:那些保护我们免受 DNA 损伤的细胞防护机制在使用大量病毒供体 DNA 时可能会无意中破坏精确的基因编辑。本研究表明,温和调整这些防护机制——在存在像 AAV 这样的线性供体时保持 ATR 活性同时暂时抑制 ATM——可以使 CRISPR 敲入更可靠、更高效。这种策略可通过帮助更多细胞接受预期的改变并避免不必要的细胞丧失,从而改进基因疗法、细胞工程和疾病模型的构建。
引用: Natsagdorj, ME., Hara, H., Uosaki, H. et al. ATM Inhibition Enhances Knock-in Efficiency by Suppressing AAV-Induced Activation of Apoptotic Pathways. Commun Biol 9, 177 (2026). https://doi.org/10.1038/s42003-026-09604-z
关键词: CRISPR 敲入, AAV 基因编辑, DNA 损伤反应, ATM 抑制, 基因组工程