Clear Sky Science · zh
STING 控制糖酵解与组蛋白乳酸化,驱动术后肠功能性麻痹中巨噬细胞的代谢重编程
当手术让肠道按下暂停键
腹部手术后,许多患者会发现肠道迟迟难以恢复活动。这种减慢被称为术后肠功能性麻痹,可能导致数日的恶心、腹胀和康复延迟。本文所述研究提出了一个看似简单的问题:为什么肠道中的某些免疫细胞会使肠道停滞不前?是否通过关闭一个分子开关就能让肠道重新启动?
常规手术如何引发肠道炎症
腹部手术不可避免地扰动肠道。在小鼠中,仅对肠管的轻柔操作就足以引起肿胀、液体潴留以及小肠内容物的堵塞。当研究者追踪一种无害荧光染料在肠道中的移动距离时,发现手术显著减缓了染料的前进,这表明蠕动受损。对肠壁的显微检查显示,负责推动食物前进的肌层出现炎症,并被大量进入的免疫细胞,尤以巨噬细胞和中性粒细胞为主,所充斥。这些发现提示:手术后,肠道的肌层变成了一个局部炎症的战场,而这种局部炎症与肠道的瘫痪密切相关。
巨噬细胞改变能量来源并助长炎症
为弄清这些渗入的巨噬细胞在做什么,研究团队从肠肌层中挖掘了大规模转录组和单细胞测序数据。他们发现,手术动物体内的巨噬细胞显著增强了一条快速的糖类燃烧通路——糖酵解。与同一组织中的其他免疫细胞相比,浸润性巨噬细胞显示出最高的糖酵解评分,并表达更高水平的关键糖酵解酶。一类独特的细胞亚群对糖酵解依赖性强,具有明显的炎症特征,并对细菌成分如脂多糖反应强烈。实质上,巨噬细胞切换到一种高糖、高炎症的状态,似乎加剧了肌层炎症,从而维持肠道运动的停滞。
将危险感应与糖类燃烧耦合的分子开关
研究者随后将注意力集中在 STING 上——一种以检测外来 DNA 为人所知的报警蛋白,但越来越被认识到具有代谢调节作用。在发炎的肠肌层中,那些高度糖酵解的巨噬细胞亚群表现出明显更高的 STING 水平,这一模式也在组织染色中得到证实。在细胞培养中,暴露于细菌脂多糖会同时提高 STING 活性和促进将葡萄糖转化为能量与乳酸的糖酵解酶水平。当研究者敲除 STING 基因时,这种糖类燃烧激增便坍塌:糖酵解中间产物下降,培养基酸化减弱,产生的活性氧减少。STING 缺失的细胞也产生更少的乳酸,表明该报警通路与代谢引擎紧密耦合。
从糖代谢产物到表观遗传记忆
乳酸常被视为代谢废物,但在这里它发挥了更微妙的作用。团队表明,在正常巨噬细胞中,大量产生的乳酸被用于通过一种称为乳酸化的化学修饰作用于组蛋白——包装 DNA 的蛋白质。这种修饰在靠近 HK2 基因的组蛋白位点 H4K8 上尤其明显,HK2 是糖酵解的门控酶。在 STING 缺失的细胞中,组蛋白乳酸化和 HK2 启动子处的染色质可及性均减少,专门的测序方法证实这些改变抑制了 HK2 的激活。与此同时,一个下游转录因子 IRF3 被发现更容易直接结合到带有这种组蛋白乳酸化标记的 HK2 启动子上。合在一起,这些步骤形成了一个自我强化的回路:STING 稳定那些增强糖酵解的因子,糖酵解产生乳酸,乳酸修饰组蛋白以打开 HK2 基因,IRF3 提升 HK2 表达,进而进一步推动糖酵解和炎症。
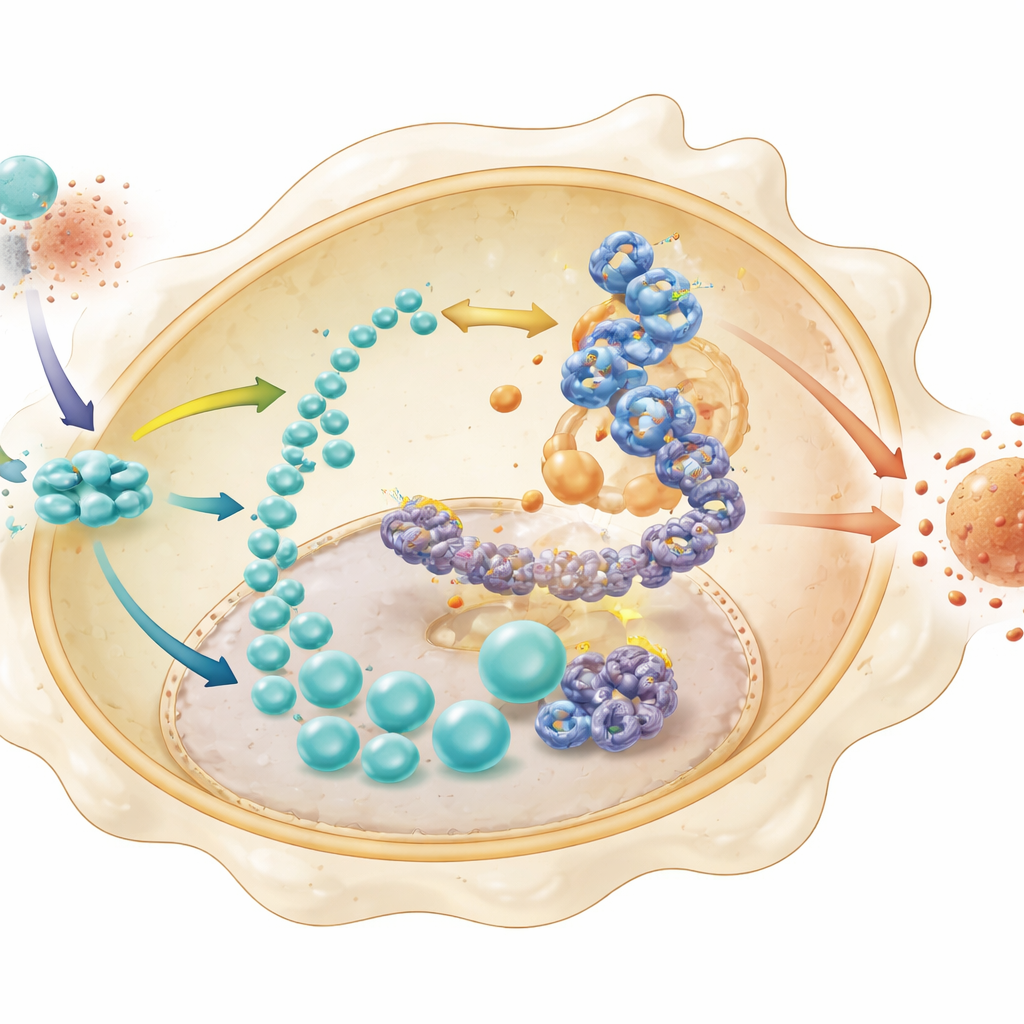
打破回路让肠道恢复
最后,研究团队探问:打破这一回路是否真的能帮助动物从术后肠功能性麻痹中恢复。在缺乏 STING 的小鼠中,肠肌组织表达的糖酵解酶更少,炎性巨噬细胞数量下降,且巨噬细胞状态从具有攻击性的促炎型向更倾向于解决炎症的表型转变。中性粒细胞的浸润也减少,肠道通过性得到改善。在正常小鼠中药理学抑制 STING 也产生了类似的益处,而在 STING 缺失动物中重新激活 HK2 酶则部分恢复了炎症和运动障碍。对普通读者而言,结论很明确:肠道巨噬细胞中的一个单一危险感应开关能够重塑它们的代谢,使肠道在手术后陷入长期的暂停。针对 STING——或其控制的糖酵解与乳酸标记反馈回路——为加速康复并缓解腹部手术的这一顽固并发症提供了有希望的途径。
引用: Chen, K., Li, G., Cheng, Y. et al. STING controls glycolysis and histone lactylation to drive macrophage metabolic reprogramming in postoperative ileus. Commun Biol 9, 358 (2026). https://doi.org/10.1038/s42003-026-09602-1
关键词: 术后肠功能性麻痹, 巨噬细胞代谢, STING 通路, 糖酵解, 肠道炎症