Clear Sky Science · zh
犬类癌瘤中的上皮-间质可塑性和免疫抑制揭示跨物种上调的CD109
藏在狗身上的癌症线索
许多家庭犬会出现与人类乳腺癌惊人相似的乳腺肿瘤。本研究利用这些自然发生的犬类癌症来回答肿瘤学中的一个紧迫问题:为何某些肿瘤能够成功关闭免疫系统的攻击,而另一些仍然脆弱。通过观察犬瘤如何改变细胞形态和行为,以及免疫细胞如何响应,研究者揭示了一种跨物种共享的癌症免疫规避机制,对人类患者具有直接启示。
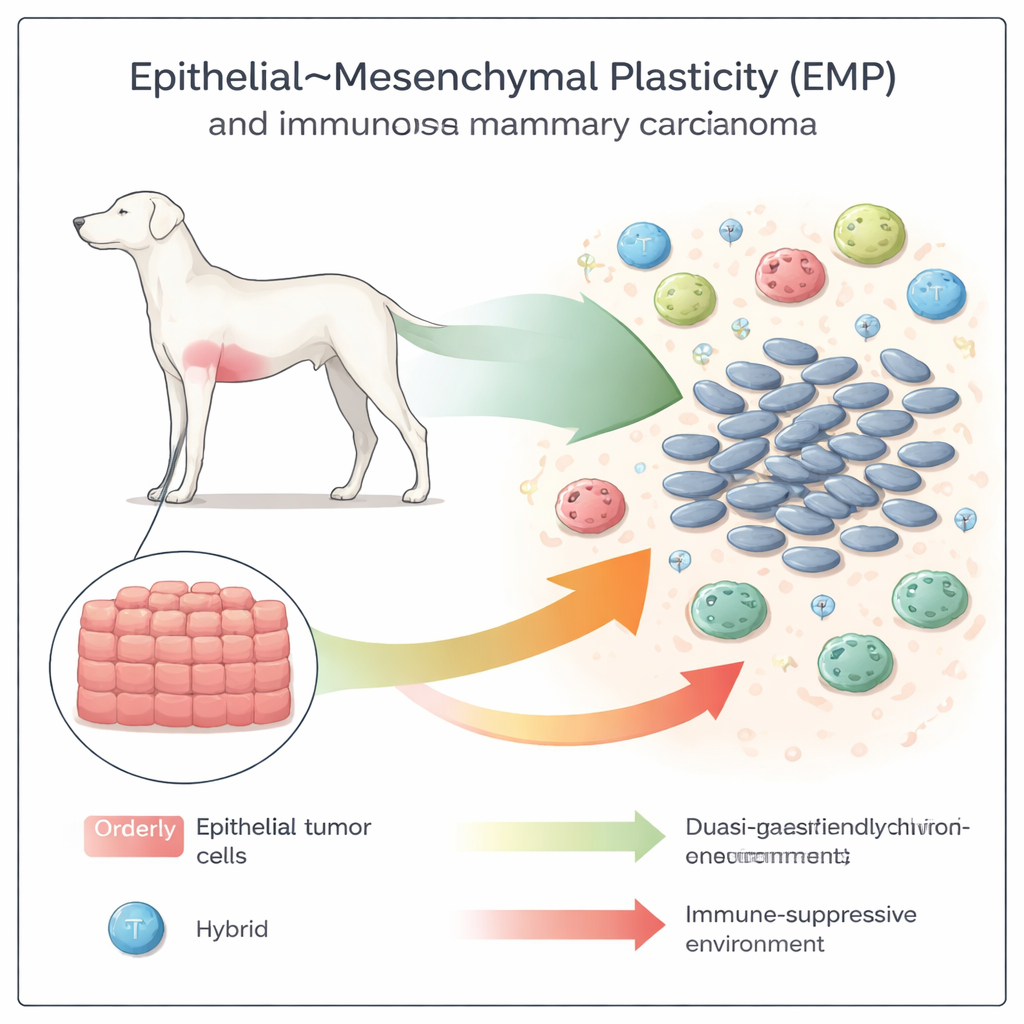
会变形的肿瘤细胞
癌细胞并非固定不变。它们可以从整齐、砖块状的“上皮”形态转变为更松散、可移动的“间质”形态,且常常停留在两者之间的中间状态。这种被称为上皮—间质可塑性(EMP)的连续谱已知有助于癌症侵袭和转移。在犬乳腺癌中,研究团队检查了50多例肿瘤,发现高级别、更具危险性的癌症显示出更强的这种变形程序:丧失有序结构,出现纺锤样细胞,并改变了通常维持细胞黏附的关键表面蛋白。
肿瘤如何关闭免疫攻击
接着,研究者询问这种细胞改造是否伴随肿瘤“邻里”免疫环境的变化。在低级别、更上皮化的肿瘤中,T细胞——尤其是能破坏癌细胞的杀伤型T细胞——相对丰富。随着肿瘤向准间质状态和更高组织学分级转变,总体T细胞数量下降,而调节性T细胞和促肿瘤的M2样巨噬细胞比例上升。换言之,随着细胞变得更具可塑性和侵袭性,周围微环境从有利免疫转向免疫抑制,这与此前仅在小鼠模型中观察到的模式相呼应。
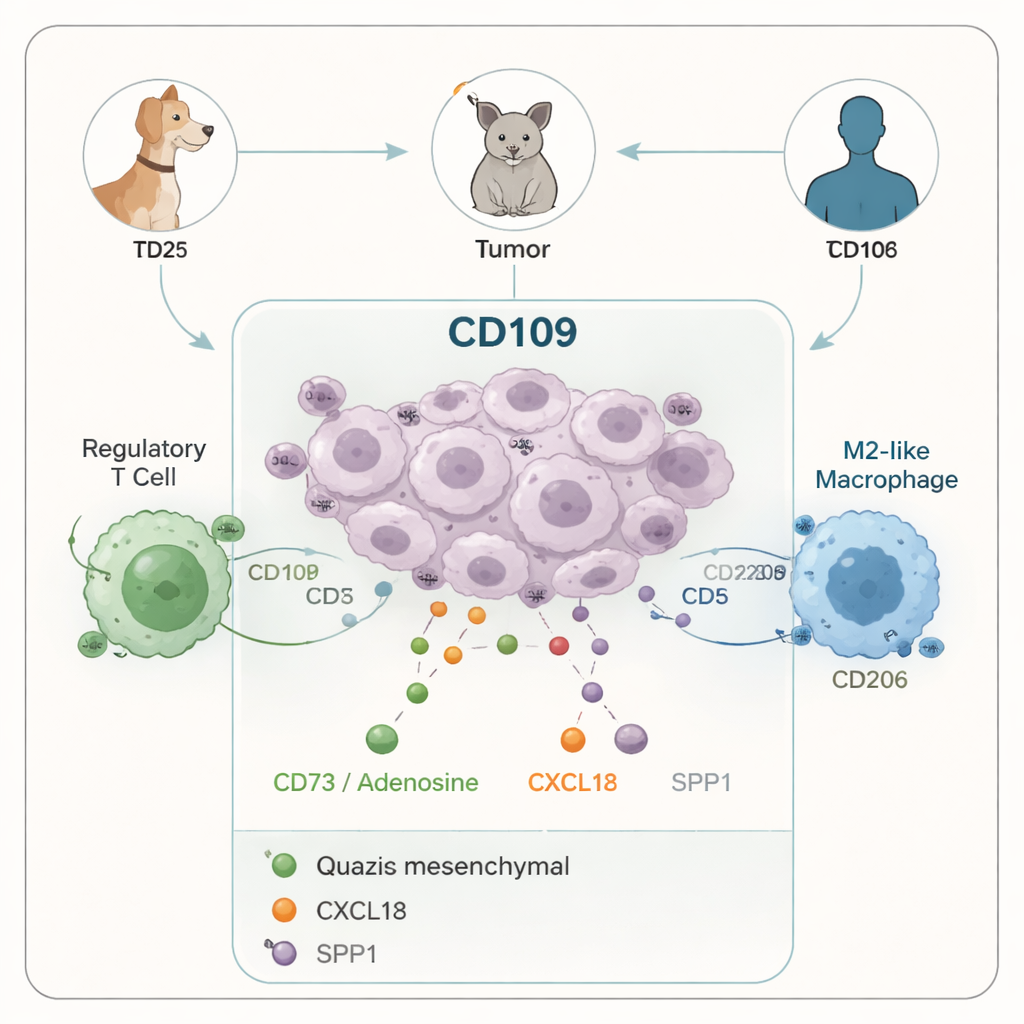
招来“错误援助”的信号
为揭示这些肿瘤如何重编程其周围环境,团队对一组覆盖上皮、混合和准间质状态的犬瘤进行了RNA测序。异质性和准间质肿瘤开启了一套已知可抑制免疫反应并招募抑制性细胞的分泌因子。这些因子包括能产生腺苷并使免疫细胞“沉睡”的CD73,以及像CXCL12和SPP1这样的趋化因子,它们有助于招募巨噬细胞和其他最终支持肿瘤生长的细胞。值得注意的是,即便只有一小部分准间质细胞的肿瘤也显示出强烈的免疫抑制基因表达,表明少数侵袭性亚群就能决定整个肿瘤的行为。
一个新参与者:犬、鼠与人中的CD109
在随EMP上升的众多分子中,有一个特别突出:一种名为CD109的表面糖蛋白。在犬乳腺肿瘤中,CD109水平在更趋间质化的、高级别和基底样癌中更高,并倾向于与更差的预后相关。通过挖掘现有的小鼠和人类数据集,作者显示CD109在准间质小鼠乳腺肿瘤以及侵袭性基底样人类乳腺癌细胞中也升高。作为细胞状态转变的关键调控因子,转录因子Snail直接结合在CD109基因附近,将其机械性地连接到EMP程序。单细胞分析确认CD109表达集中在最像间质的癌细胞中,并与其他免疫抑制信号共同出现。
多种癌症中共享的免疫逃逸策略
为检验这些模式的普适性,团队重新分析了数种来源于上皮的犬类其他癌症的RNA数据,包括口腔鳞状细胞癌、侵袭性尿路上皮癌和肺癌。在这些肿瘤类型中,EMP标志物与免疫抑制旁分泌因子的更高表达持续相关——尤其是CD73、SPP1和CXCL12——尽管CD109与EMP的关联在乳腺癌中表现得最强且最具特异性。这提示了一个共同的剧本:当肿瘤采取更具可塑性、侵袭性的状态时,它们同时开启化学信号以重塑有利于自身的免疫景观。
对犬与人的意义
对普通读者的结论是:当犬类的癌细胞学会改变形态和身份时,它们也学会了压制免疫系统并对现代免疫疗法产生抵抗。由于犬瘤与人类疾病高度相似,这些发现指向了共享的靶点——如CD73和新提出的CD109——可能通过阻断这些分子来重新唤醒两种物种的免疫攻击。未来,检测这些分子可能有助于识别高风险肿瘤并指导组合治疗,不仅直接攻击癌细胞本身,还拆解它们周围构建的保护屏障。
引用: Bakhle, K., Nelissen, S., Li, L. et al. Epithelial-mesenchymal plasticity and immunosuppression in canine carcinomas reveals cross-species upregulation of CD109. Commun Biol 9, 303 (2026). https://doi.org/10.1038/s42003-026-09587-x
关键词: 犬类乳腺癌, 上皮-间质可塑性, 肿瘤免疫微环境, CD109, 癌症免疫疗法耐受性