Clear Sky Science · zh
对WRN解旋酶的结构洞见揭示构象状态并为MSI‑H癌症药物发现提供机会
这对癌症治疗为何重要
某些癌症有一个内在的弱点:它们难以修复DNA中的错误。一种称为WRN解旋酶的蛋白质像分子修复工具,维持这些脆弱肿瘤的存活。本研究以原子级细节揭示了WRN如何沿DNA移动,以及实验性药物如何阻断其运动——为开发选择性杀死这些易感癌细胞同时尽量不伤害健康组织的新疗法提供了路线图。
显微镜下的DNA修护工
WRN解旋酶是细胞维护队伍的一员,帮助解开DNA以便发现并修补损伤。先天缺失功能性WRN的人会患上维纳综合征(Werner syndrome),这是一种以过早衰老为特征的罕见疾病,表明该蛋白对基因组维护至关重要。携带“高微卫星不稳定性”(MSI‑H)——这种在结直肠癌和某些其他癌症中常见的缺陷——的肿瘤尤其依赖WRN。当在这些细胞中关闭WRN时,它们本就脆弱的DNA会迅速崩溃,癌细胞死亡。因此WRN成为一个有吸引力的药物靶点,但此前科学家尚未清晰了解该蛋白在抓取DNA、消耗化学能量并沿基因物质移动时如何变化构象。
观察WRN的伸展与呼吸
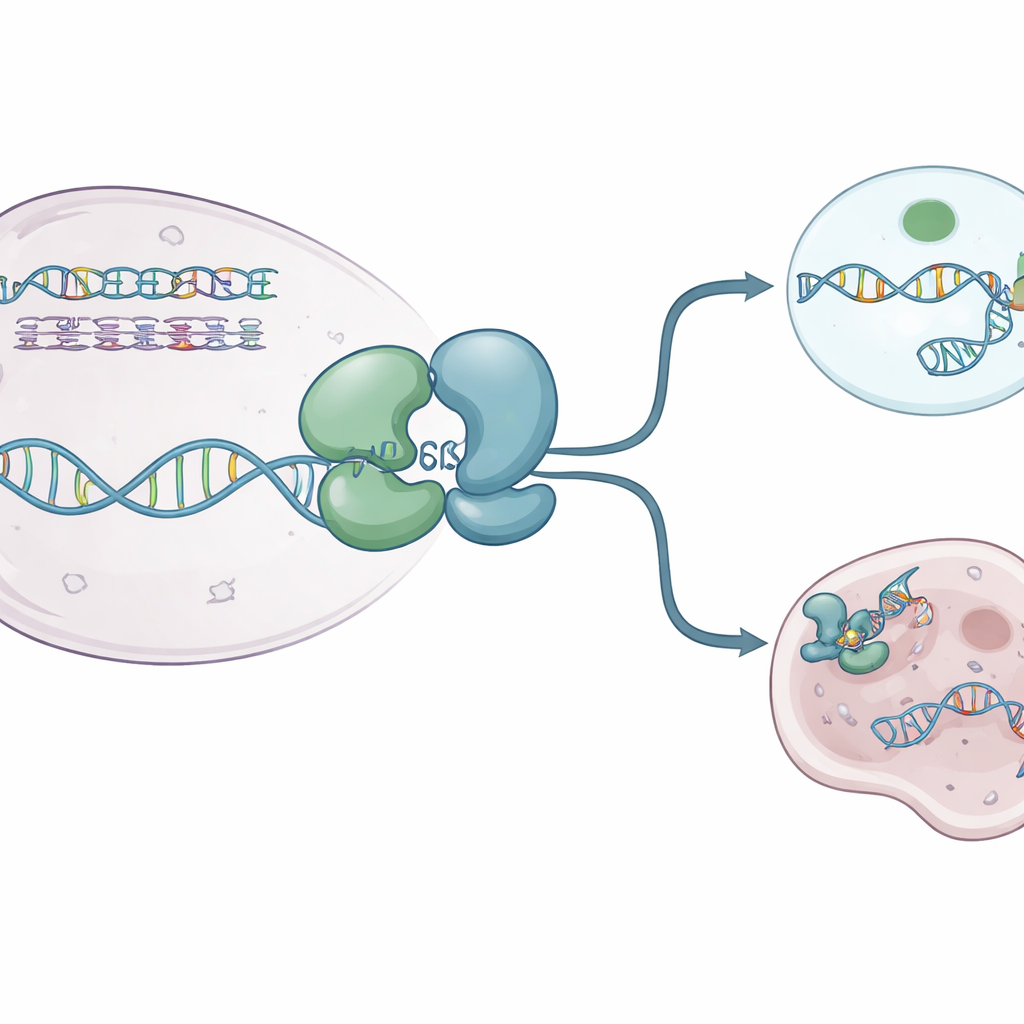
作者使用X射线晶体学捕获了人类WRN解旋酶核心的多个高分辨率“快照”。他们解析了孤立WRN以及与单链DNA和不可裂解的类ATP供能分子结合的结构。这些视图揭示,该蛋白由两个主叶组成,通过一个柔性的铰链相连,像一个会“呼吸”的关节。在静息、无能量分子状态下,WRN采用紧凑的“闭合”构象,两叶靠得很近。当类ATP供能分子和DNA存在时,两叶分开,呈更“开放”的构型,可以在一个带正电的槽中容纳DNA。WRN内一个小的芳香族环变形成一段短螺旋并楔入DNA碱基之间,像棘轮一样帮助蛋白向前迈步而不向后滑动。
当前药物如何关闭WRN
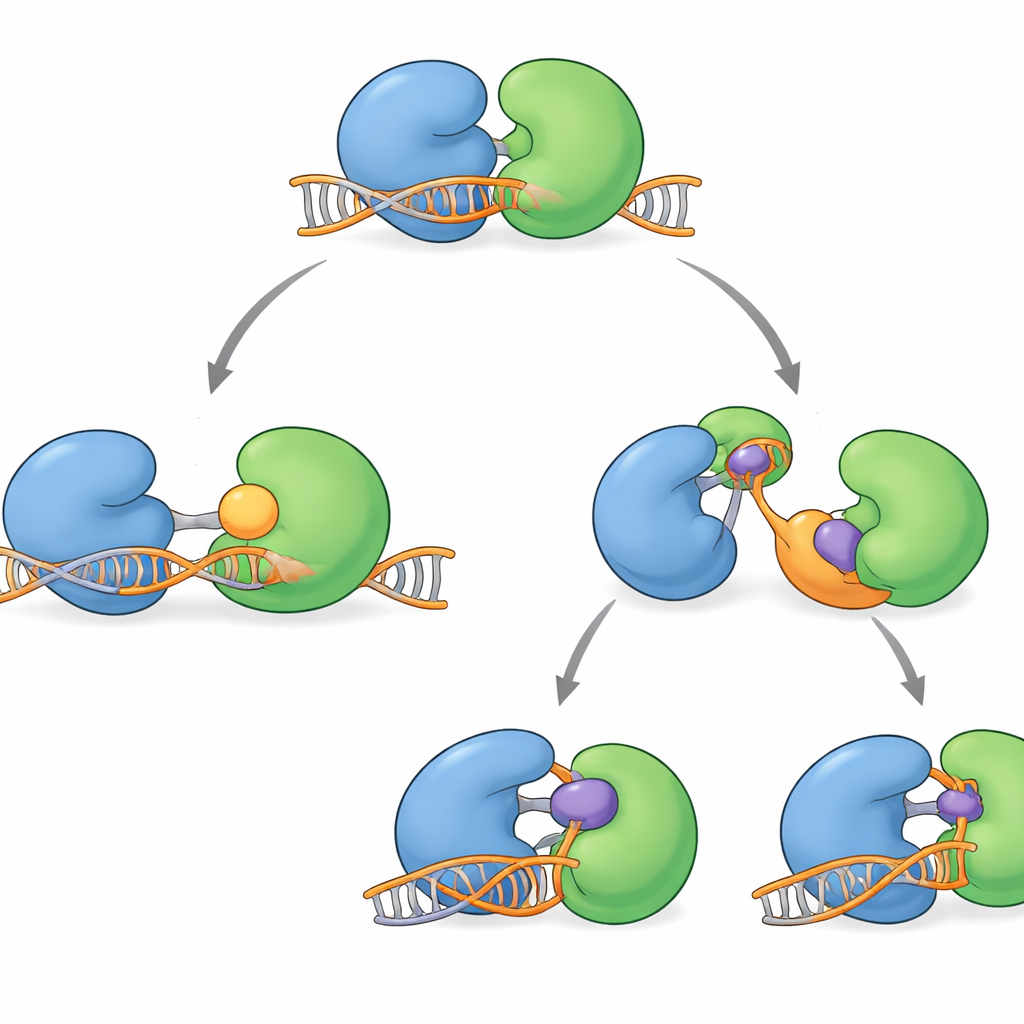
若干阻断WRN的化合物最近进入临床试验。它们并不直接堵塞蛋白的活性槽,而是在远处作用,抓住铰链区域并将WRN锁定在无法正常结合DNA的构象中。一些分子,如HRO761及葛兰素史克(GSK)的一种相关临床候选药,使一个叶相对于另一个叶大约旋转180度,形成一种“扭曲”的显著构型,无法与DNA接触。其他分子,包括VVD‑133214及本研究中考察的一个密切相关化合物,则将WRN钉在紧密的“闭合”构型,不能暴露关键的DNA抓取表面。生物物理实验证实,当这些药物结合时,WRN不再能与单链DNA形成稳定复合体,有效切断了ATP消耗与DNA解旋之间的联系。
癌细胞如何学会逃避
为了解肿瘤可能如何规避这些药物,研究团队在WRN抑制剂存在的条件下培养MSI‑H结直肠癌细胞数周到数月。耐药群体迅速出现。遗传学分析显示,在每个案例中,细胞在靠近药物结合铰链的WRN基因处获得了一个单一且精确的改变。一种突变削弱了对“扭曲态”抑制剂HRO761的作用,而另一种突变降低了对偏好闭合态的VVD‑133214的敏感性。此外,许多耐药细胞提高了WRN的表达,增加了靶点拷贝数,从而部分稀释了药物的效应。这些发现与其他靶向癌症药物观察到的耐药模式相呼应:靶蛋白的小结构调整或过表达可削弱治疗效果。
展望更聪明的WRN抑制剂
综合来看,新解析的结构描绘出WRN抓住DNA、前进并重置的完整工作循环。它们还表明,当今的临床化合物主要稳定蛋白的“脱离DNA”构象。对普通读者而言,关键点是我们现在理解了WRN的脆弱之处以及肿瘤可能如何适应。这提示下一代抑制剂可在WRN被锁定在DNA上时结合它,可能将其困在有毒状态——类似于能诱捕其他DNA修复酶的成功药物。此类“在DNA上”WRN抑制剂,单独使用或与现有药物联合使用,可能为更持久地利用MSI‑H癌症的隐性弱点提供新的途径。
引用: Fletcher, C.T., Mornement, A.A., Barrett, C. et al. Structural insights into WRN helicase reveal conformational states and opportunities for MSI-H cancer drug discovery. Commun Biol 9, 334 (2026). https://doi.org/10.1038/s42003-026-09584-0
关键词: WRN解旋酶, 微卫星不稳定性, DNA修复, 变构抑制剂, 药物耐受性