Clear Sky Science · zh
PiR48444通过靶向METTL7A/eIF4E介导的BMP2 m6A甲基化抑制MSC成骨分化和骨再生
为何微小分子对骨折修复至关重要
骨折和与年龄相关的骨量流失是常见问题,医生希望利用干细胞帮助机体重建受损的骨骼。然而,这些干细胞并不总能像我们期望的那样高效形成新骨,尤其是在老年人或炎症组织中。本研究发现了一种名为piR48444的微小RNA分子,它像分子制动器一样抑制成骨干细胞。研究者表明,通过解除这一制动,有望促进骨修复并防止骨量流失。
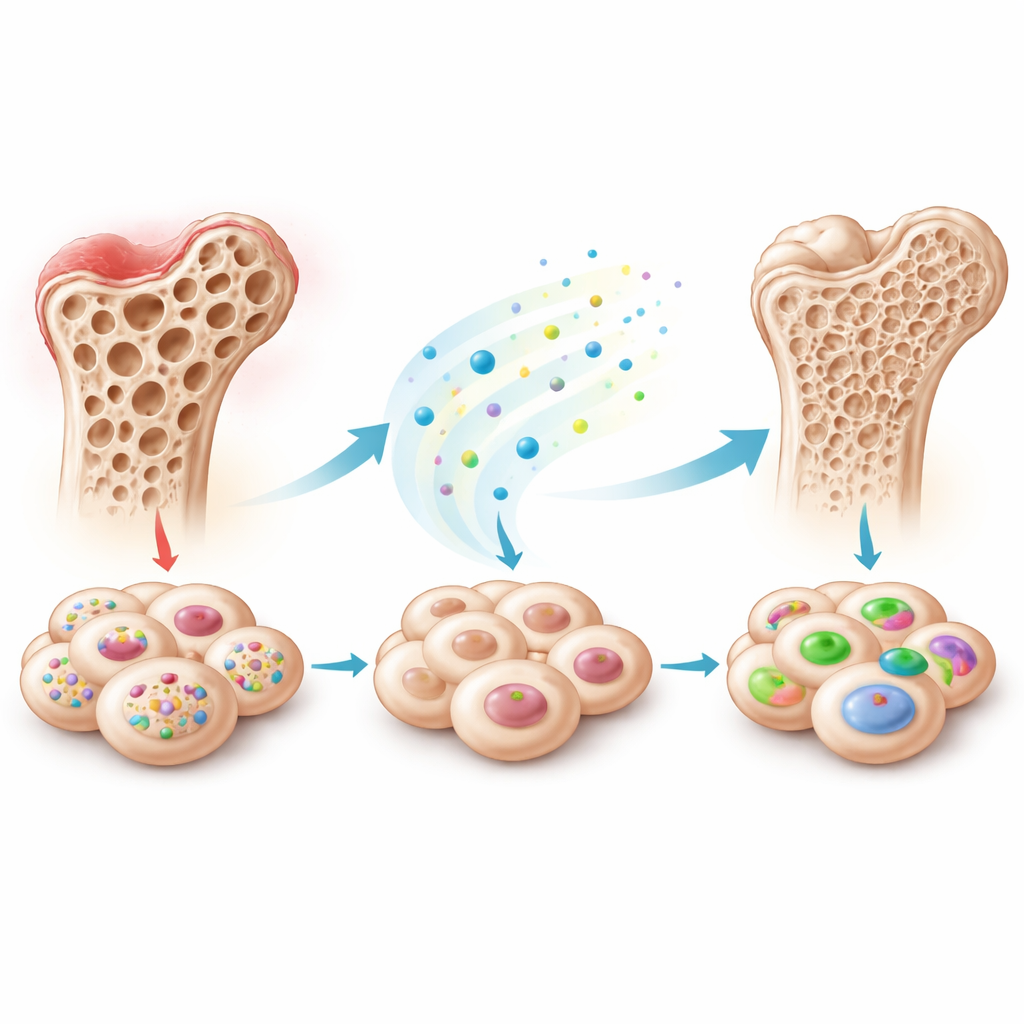
存在于多种干细胞中的隐性制动器
团队把研究重点放在间充质干细胞上——这类多能细胞可分化为骨、软骨、脂肪等,并可从骨髓、乳牙、脂肪等多种组织中分离出来。当在体外诱导这些细胞成骨时,数千个基因和小RNA的活性发生变化。通过对来自脱落乳牙的干细胞测序,研究者发现一种特定的小RNA piR48444在细胞向成骨方向转变过程中持续下降。随后他们在其他类型的干细胞中也观察到相同模式:成骨活性更高的细胞中piR48444含量更低,这暗示该分子可能在生理上抑制它们的成骨能力。
从培养皿到活体骨组织
为验证这一假设,科学家在多种干细胞类型中调节了piR48444的水平。降低piR48444时,细胞沉积更多钙质,激活与成骨相关的基因,显微镜下表现出更像未成熟骨组织的形态。强制表达额外piR48444则产生相反效果:成骨相关活性下降。随后团队进入动物模型研究。将关闭piR48444的干细胞用于填补小鼠颅骨缺损,这些经改造的细胞产生的新骨远多于对照细胞,3D X射线扫描和组织染色均显示出明显差异,表明抑制piR48444可实质性改善活体中的骨修复。
在疾病与衰老中保护脆弱骨组织
骨量流失不仅由损伤引起,也受炎症和衰老驱动。在暴露于细菌毒素的骨髓干细胞以及来自年老动物的干细胞中,piR48444水平异常升高,而成骨标志物下降。研究者构建了一种“抗小干扰寡核苷酸”(antagomir)——一种用于在血液中中和piR48444的短分子,并将其注射到炎症所致骨丢失的小鼠或自然衰老的小鼠中。在两种模型中,接受处理的动物保留了更多松质骨,骨小梁更致密且数量更多,而骨外层的致密骨未见显著变化。这表明阻断piR48444可以选择性保护在衰老和慢性炎症时最易受损的代谢活跃型骨组织。
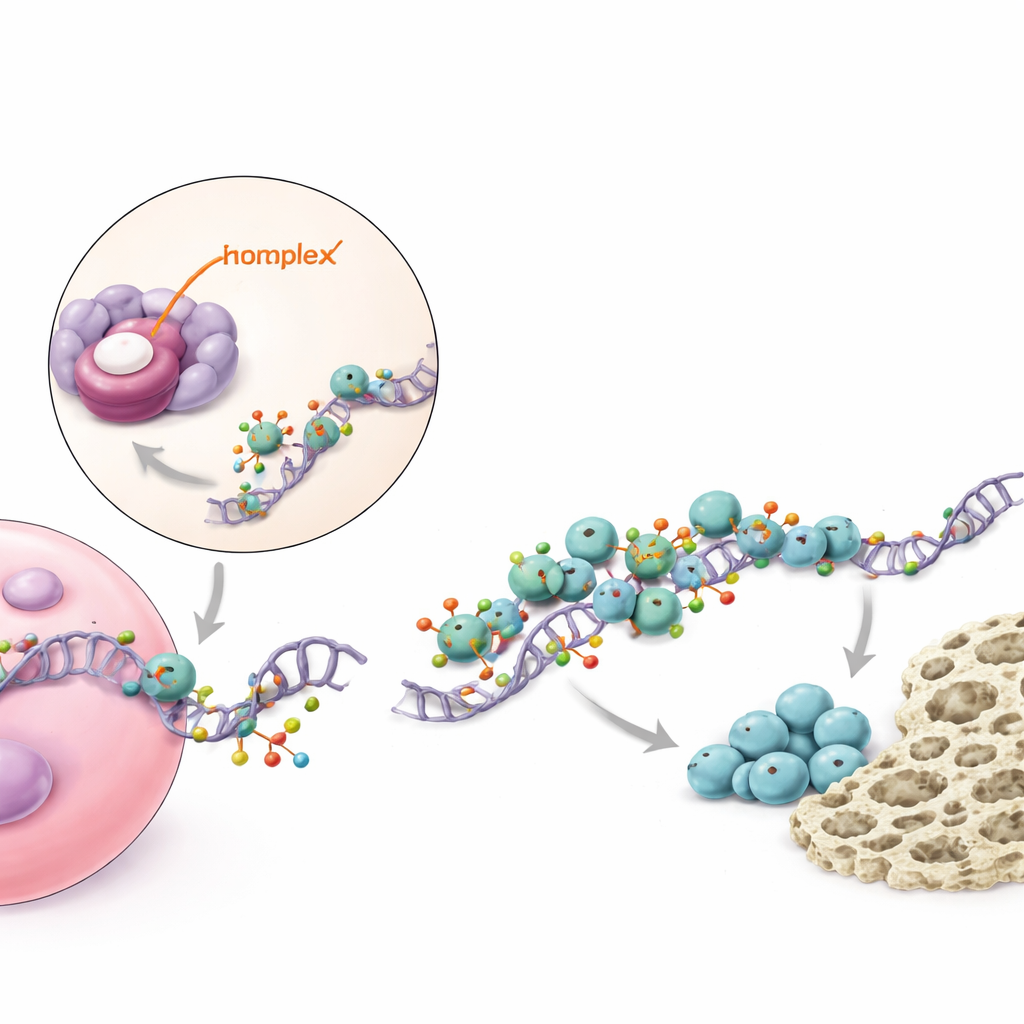
增强关键成骨信号的分子接力
深入研究显示了piR48444在细胞内发挥作用的途径。该小RNA与并抑制一种名为METTL7A的蛋白结合,后者作为酶对携带BMP2蓝图的信使RNA进行修饰。METTL7A在BMP2信使RNA上添加小的化学标记,使这些信息更稳定、更易被细胞的蛋白质合成机器利用。METTL7A还与另一种帮助启动蛋白合成的蛋白eIF4E协同工作。当piR48444含量高时,METTL7A受抑,标记并被翻译的BMP2信息减少,BMP2蛋白产量下降,因而干细胞更不易分化为骨。当阻断piR48444时,METTL7A和BMP2水平上升,推动细胞向成骨方向发展。
对未来骨修复的意义
简而言之,作者揭示了一条控制链:微小RNA(piR48444)抑制辅助酶(METTL7A),进而限制强有力的成骨信号(BMP2)。在piR48444水平处切断这条链,可以增强多种干细胞的成骨能力,并减轻小鼠的骨量流失。尽管安全性、脱靶效应和长期结果仍需谨慎评估,该工作将piR48444指出为潜在的骨质疏松血液标志物与有望用于临床促进干细胞骨再生的药物靶点。
引用: Zheng, Z., Li, X., Qin, W. et al. PiR48444 inhibits MSC osteogenic differentiation and bone regeneration via targeting METTL7A/eIF4E-mediated BMP2 m6A methylation. Commun Biol 9, 337 (2026). https://doi.org/10.1038/s42003-026-09583-1
关键词: 骨再生, 间充质干细胞, 骨质疏松, 非编码RNA, BMP2信号