Clear Sky Science · zh
局部阳离子夹持使RNA双链扭曲并变软
为什么这微小的RNA扭转很重要
在每个细胞内,DNA和RNA不断地被弯曲、拉伸和扭转,以便储存和使用遗传信息。这些运动不仅仅是机械细节——它们控制基因如何被读取、病毒如何复制自身,以及基于RNA的新药物和纳米器件将如何工作。本研究表明,由正负离子组成的简单盐类可以显著改变RNA的刚性或柔韧性,并且RNA对此的响应与DNA大不相同。理解这种微妙的“变软与变硬”变化,有助于科学家更好地设计RNA药物、疫苗和分子工具。
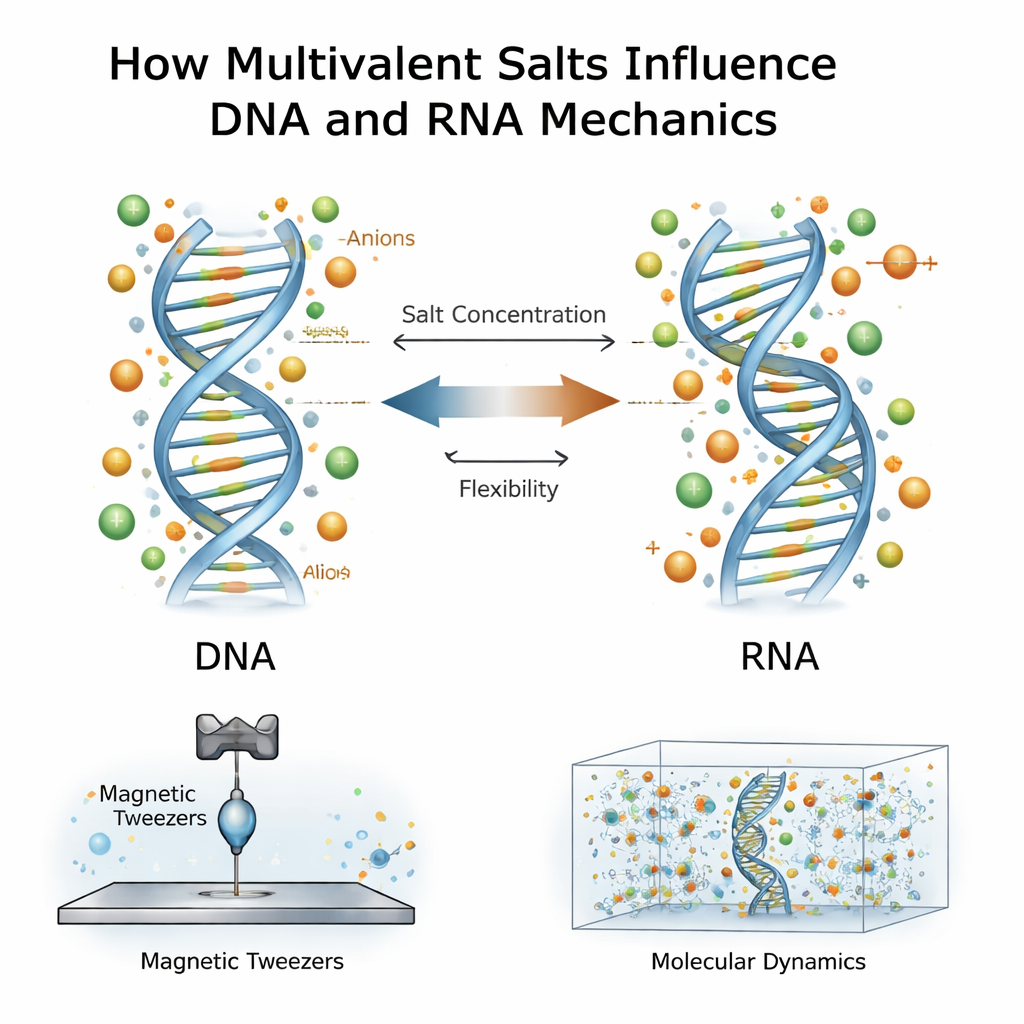
含盐环境与遗传分子
DNA和RNA带有强烈的负电荷,因此在水中被相反电荷的离子云包围。早期大多数研究主要关注正电离子,尤其是携带两价或三价电荷的多价离子,如镁离子或精胺。这些离子已知能把DNA链拉拢在一起、使其凝聚或改变其弯曲难易度。尽管RNA在化学上与DNA相似,但表现不同:它通常更难弯曲但更容易拉伸。新研究提出了一个更深入的问题:当正离子及其伴随的负离子——称为阴离子——在非常高的盐浓度下(远高于典型细胞内水平)与DNA和RNA相互作用时,会发生什么?
拉伸单分子以测量刚性
研究者使用一种称为磁镊的技术逐一拉伸单个DNA或RNA双螺旋分子。每个分子一端固定在玻璃表面,另一端连接到一个微小的磁珠。通过在样品上方移动磁铁,他们可以施加受控力并记录每个分子伸长的距离以及它在拉力下的扭转情况。从这些力—伸长曲线中,他们提取出四项关键机械特性:分子的弯曲难度、拉伸难度、每个碱基对的有效长度以及扭转如何改变其长度。他们在多种盐(包括精胺和氯化钙)和广泛的多价盐浓度范围内重复了这些测量。
DNA再次变硬,但RNA突然变软
对于DNA,其行为大体符合预期。随着多价正离子浓度的增加,DNA先变得更易弯曲——其刚性下降——因为这些离子中和了其负电荷。在更高浓度下,过量的正离子会过度补偿,实际上逆转了DNA的净电荷。这种“电荷反转”使DNA再次变得难以弯曲,从而刚性上升。令人意外的是,RNA表现出相反且更剧烈的模式。在低到中等盐浓度下,其弯曲刚性增加:RNA双链变得更笔直、更僵硬。但在非常高的浓度下,RNA的弯曲刚性下降了超过一半,其他性质如其拉伸性和扭转—拉伸行为也以出乎意料的方式发生了变化。
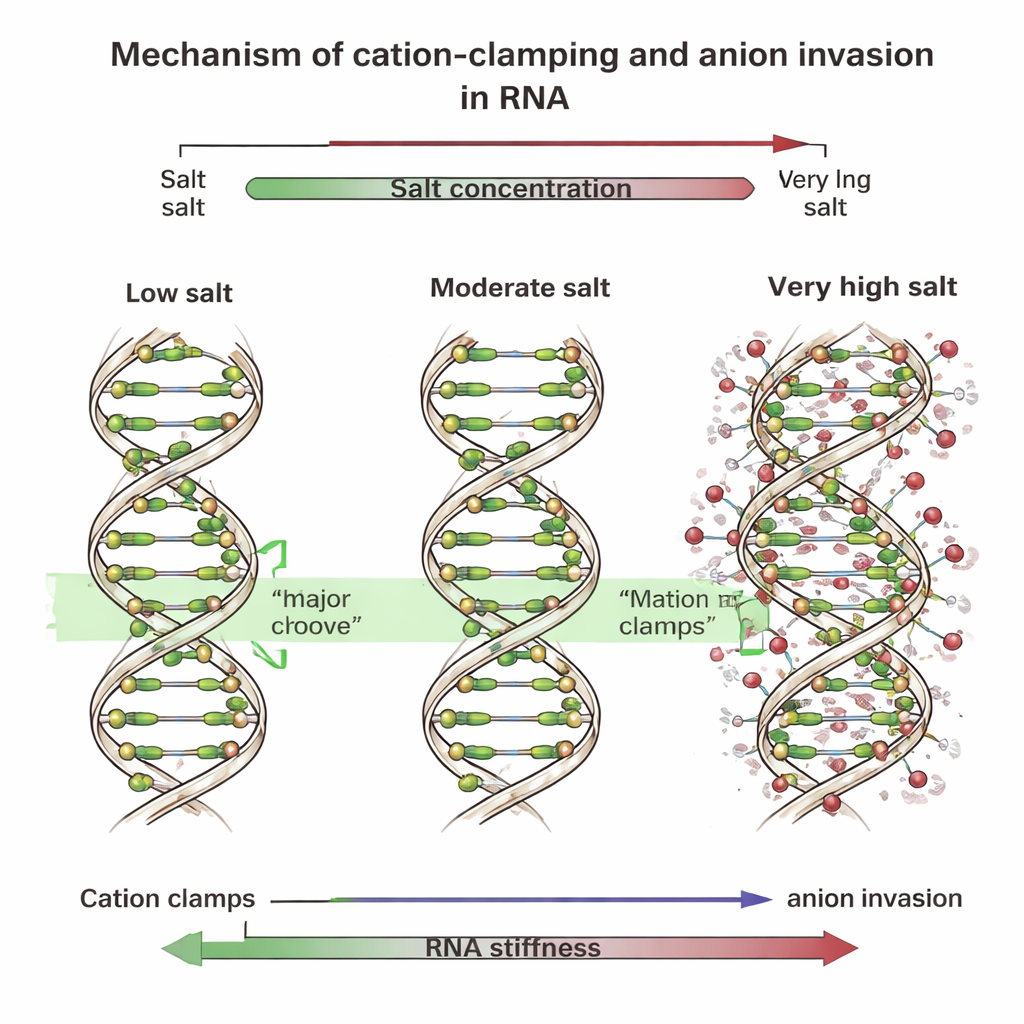
夹持、槽道与入侵的离子
为查明原因,团队进行了详尽的计算机模拟,追踪短DNA和RNA片段在盐水中每个原子的行为。这些模拟显示,在低到中等浓度时,多价正离子会定居在RNA的一处宽阔表面,称为大沟(major groove)。在那里它们形成“阳离子夹持”,跨越沟槽桥接两侧,将其拉拢在一起,使螺旋变直并变刚硬。DNA的沟槽形状不同,主要是在其外部骨架上结合这些离子。然 而,在非常高的盐浓度下,许多阴离子——例如氯离子——会逼近RNA骨架甚至进入大沟。它们的出现破坏了有序的夹持,将其打散成不规则、斑驳的“局部夹持”,导致螺旋变形。当研究者在模拟中通过添加人工弹簧或在RNA附近锁定额外阴离子来模仿这一效应时,RNA骨架弯曲增加、整体刚性骤降,这与实验观察一致。
这对未来RNA技术意味着什么
简单来说,研究表明仅通过改变周围盐类的类型和浓度,就可以使RNA变得更笔直、更刚硬,或更加折角、更柔软。在适度水平的多价离子下,正电荷有序地夹持RNA的外表面并支撑它;在极高水平下,入侵的阴离子破坏了这种均匀支撑,产生扭曲、较软的区域。DNA没有出现这种明显的软化,因为它以不同方式结合离子并经历净电荷反转。这些见解强调了不仅正离子而且其负电伴侣对于控制RNA形状的重要性。这一知识将帮助研究人员在实验室中有目的地调节RNA力学——例如稳定RNA药物、控制生物传感器中RNA的折叠,或设计更可靠的基于RNA的纳米结构。
引用: Zhang, C., Dong, HL., Zhang, JH. et al. Local cation-clamping distorts and softens RNA duplex. Commun Biol 9, 308 (2026). https://doi.org/10.1038/s42003-026-09580-4
关键词: RNA 力学, 多价离子, 阳离子夹持, DNA 与 RNA 的区别, 盐的效应