Clear Sky Science · zh
α-SNAP 的致病突变通过掩蔽关键疏水环降低膜脂结合
一个微小蛋白变化如何扰乱大脑发育
我们的脑细胞不断通过名为囊泡的小气泡运输货物,而一种名为 alpha-SNAP 的辅助蛋白在这些运输过程中起着核心作用。来自称为“hyh”的小鼠系的一种罕见 alpha-SNAP 突变会导致严重的脑形成和液体平衡问题。本研究提出了一个看似简单但后果重大的问题:alpha-SNAP 中的这个单字母替换是否阻止了它附着到细胞膜上,而这是否可能是大脑出现异常的关键原因?
一位承担多重任务的细胞码头工人
Alpha-SNAP 通常充当囊泡的“码头工人”,帮助它们与细胞膜融合,从而释放或回收货物。它与一组称为 SNARE 的蛋白及利用能量的机器 NSF 协同工作,将膜拉拢在一起,然后重置系统以进行下一轮融合。除了这一经典角色外,alpha-SNAP 还参与调控自噬、细胞凋亡、钙通道以及能量感应等过程。这些功能在某种程度上都依赖于 alpha-SNAP 与膜的接触以及部分插入膜脂的能力。
一个隐蔽的环与一个麻烦的突变
早期工作表明,alpha-SNAP 在蛋白的一端附近使用一段短小的疏油“环”来钩住膜。在健康蛋白中,这个环会突出并能够插入膜的外层。在 hyh 小鼠中,位置 105 的单个氨基酸被置换,产生了 M105I 突变。作者使用计算模拟来观察这一改变如何影响蛋白构象。他们发现突变体蛋白变得略微更紧凑并发生扭曲,使疏水环向内折叠,远离水和膜。因此,突变蛋白接近膜时呈更平的角度,并倾向于用一个粘性较差的区域贴压膜面,从而减少了接触时间和插入深度。结合能计算支持了这一点:野生型蛋白进入了低能量、强结合的状态,而突变体更倾向于较弱、较浅的接触。
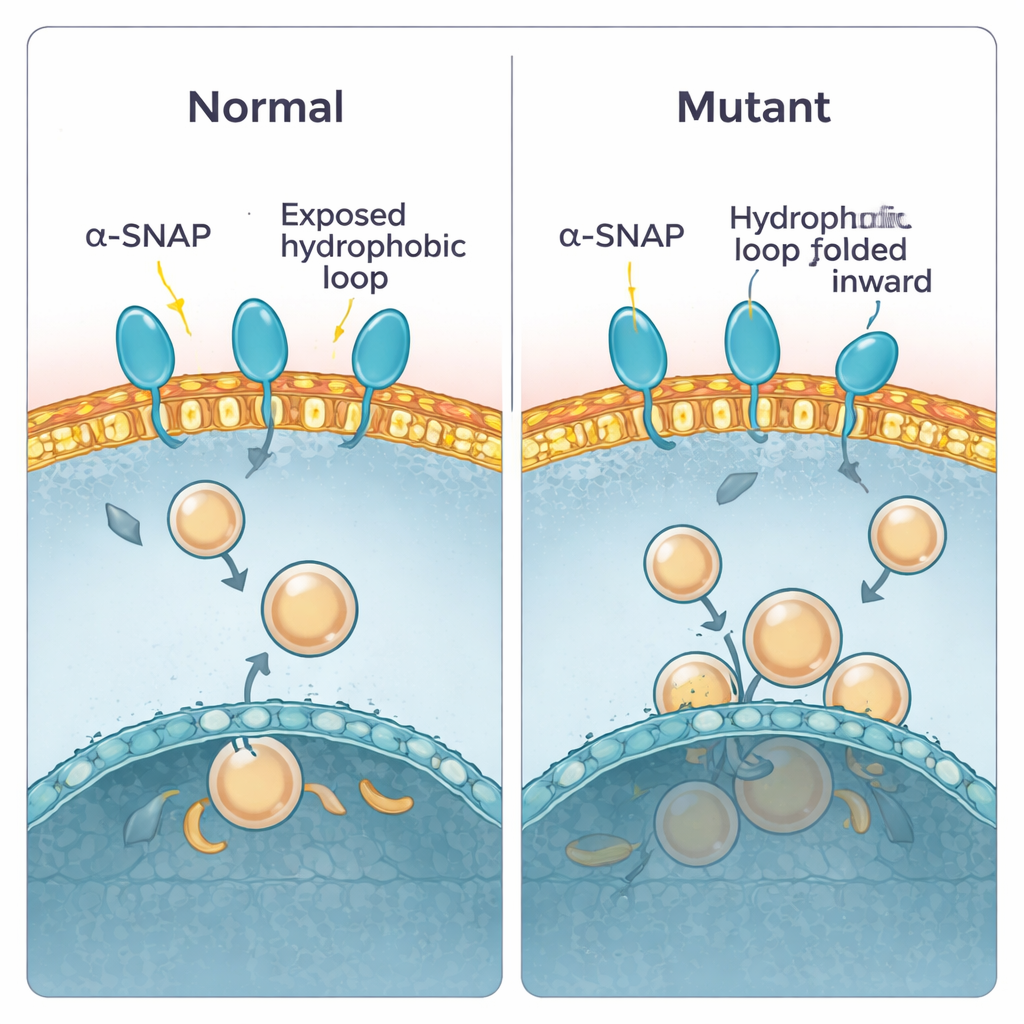
在实验室中验证预测
为了检验这些预测,团队纯化了正常和突变的 alpha-SNAP 并在不同实验体系中测试它们的行为。首先,他们使用一种能分离成水相和油相的去污剂,以模拟在水与膜之间的取舍。正常的 alpha-SNAP 在两相间均匀分布,表明具有平衡的、部分疏油表面。突变体不太愿意进入油相,提示其疏油片段确实更多被埋藏。接着,他们让这些蛋白与从细胞制备的平面质膜“片”相互作用,并成像观察结合斑点的数量。结果再次显示,正常的 alpha-SNAP 在膜上呈点状分布,而突变体的结合明显减少。最后,他们将用脑脂质制成的人工膜泡(脂质体)通过糖梯度进行浮选。野生型 alpha-SNAP 随着富含质膜脂质的囊泡上浮,而突变体则滞后,除非囊泡由较内层膜成分制成,否则其结合很差。
在发育中大脑中的后果
研究者随后转向发育中小鼠胚胎的大脑,关注新神经元生成的时期。通过将细胞内容物分离为可溶与膜结合两部分,他们证明 hyh 大脑中 alpha-SNAP 的总量已经降低,但更重要的是,与正常小鼠相比,附着于膜上的那一部分比例明显偏低。当他们进一步分离不同类型的膜时,发现损失最大的是质膜——细胞的外表面,而内膜的影响要小得多。显微镜结果也印证了这一点:在正常组织中,alpha-SNAP 在细胞边缘呈现蜂巢状轮廓,与已知的表面标记相吻合。在 hyh 大脑中,这种清晰的边界染色变得模糊并转为更弥散的内部荧光,表明突变蛋白无法停留在细胞边缘——那里是囊泡融合和信号传导最活跃的区域。
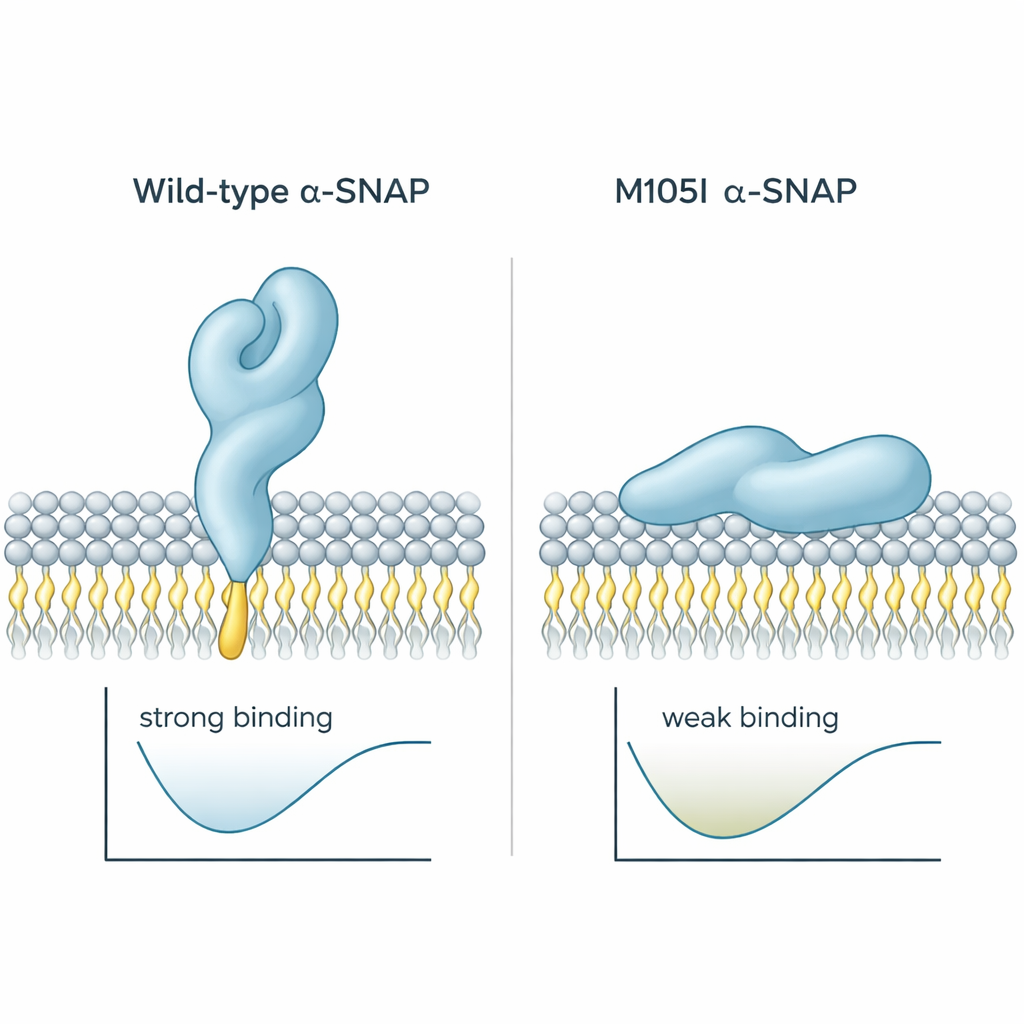
此发现对疾病研究的意义
综上所述,这项工作表明 M105I 突变不仅仅降低了 alpha-SNAP 的量;它改变了蛋白的折叠,使其关键的膜抓取环被掩蔽。这使 alpha-SNAP 更难抓住质膜并采取组织融合机器所需的适当方向。在发育中的大脑里,细胞表面精准递送信号和构建材料至关重要,这一微妙的结构缺陷很可能促成了 hyh 小鼠出现的脑积水、皮层连线错误及其他缺陷。对非专业读者而言,结论很明确:即便是单个蛋白形状的微小变化,也能改变细胞的沟通方式,进而影响大脑的构建。」
引用: Méndez-Ruette, M., Bedoya, M., Hinrichsen, B. et al. A pathogenic mutation in α-SNAP impairs membrane lipid binding by concealing a critical hydrophobic loop. Commun Biol 9, 294 (2026). https://doi.org/10.1038/s42003-026-09578-y
关键词: alpha-SNAP, 膜结合, 蛋白质突变, 脑发育, 囊泡融合