Clear Sky Science · zh
穿通束通路与CA3–Schaffer侧枝输入协同调控空间学习
为何找路如此重要
无论是寻找隐蔽平台的老鼠,还是在新城市中导航的人类,大脑都会不断将视觉、听觉和自我运动信息转化为内部地图。本研究探究了两个关键脑区——内嗅皮层与海马体——如何协同支持这一能力。通过在极细的神经纤维中实时观察活动,并在小鼠中精确地激活或抑制特定通路,研究者揭示了这些区域如何配合以形成并稳定空间记忆——这些见解最终可能有助于我们理解和治疗记忆紊乱。
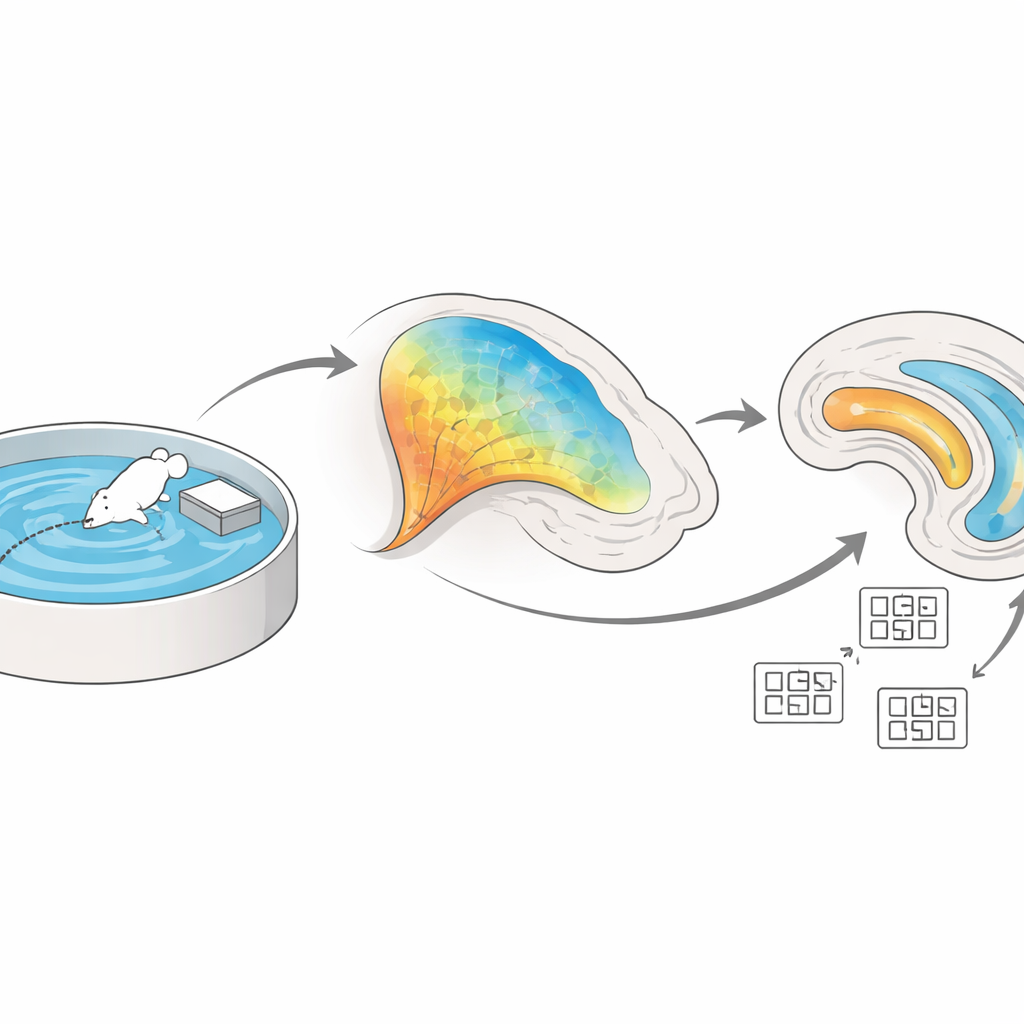
大脑“内置GPS”的两个关键枢纽
海马体及其邻近的内嗅皮层位于大脑颞叶深部,构成我们的导航系统核心。在海马体内部,一个称为CA3的区域通过称为Schaffer侧枝的纤维与另一个称为CA1的区域相连。与此同时,内嗅皮层通过所谓的穿通束将另一股信息流直接投射到CA1。作者旨在确定当动物学习空间布局时,这两条输入通路如何协作,以及它们连接处的改变——通常称为“可塑性”——如何支持稳定空间地图的建立。
逐纤维观察学习的展开
为了在行为动物中追踪这一过程,团队使用了光纤光度法,这是一种通过荧光闪光报告神经活动的技术。他们基因工程化小鼠,使投射到CA1的CA3神经元在活跃时发光,然后在莫里斯水迷宫上训练这些动物,这是一种经典测试,要求小鼠学习水池中隐蔽小平台的位置。在早期试验中,CA3–CA1纤维在动物搜索时活动强烈;随着小鼠熟练并更快找到平台,这种活动逐渐减弱。该模式表明,这些连接在大脑最初编码环境布局时特别活跃;一旦记忆建立,它们就会进入更高效、更稳定的表征状态。
上游输入如何促进或削弱学习
研究人员接着探问内嗅皮层的信号如何影响这一海马回路。利用光敏蛋白激活内嗅神经元并同时记录CA3–CA1纤维的活动,他们发现驱动来自内侧内嗅皮层的输入会可靠地增强这些海马连接的活动。相反,当在水迷宫训练期间化学遗传学地抑制到达CA1的内嗅信号时,CA3–CA1活动减弱,小鼠学会平台位置的速度更慢且不够精确。在一组互补实验中,作者直接记录投射到CA1的内嗅神经元,观察到它们的活动随着训练天数上升,这与动物表现的改善相呼应。综上,这些结果表明,强烈且时序恰当的内嗅信号对于适当地调节用于导航的海马回路是必要的。
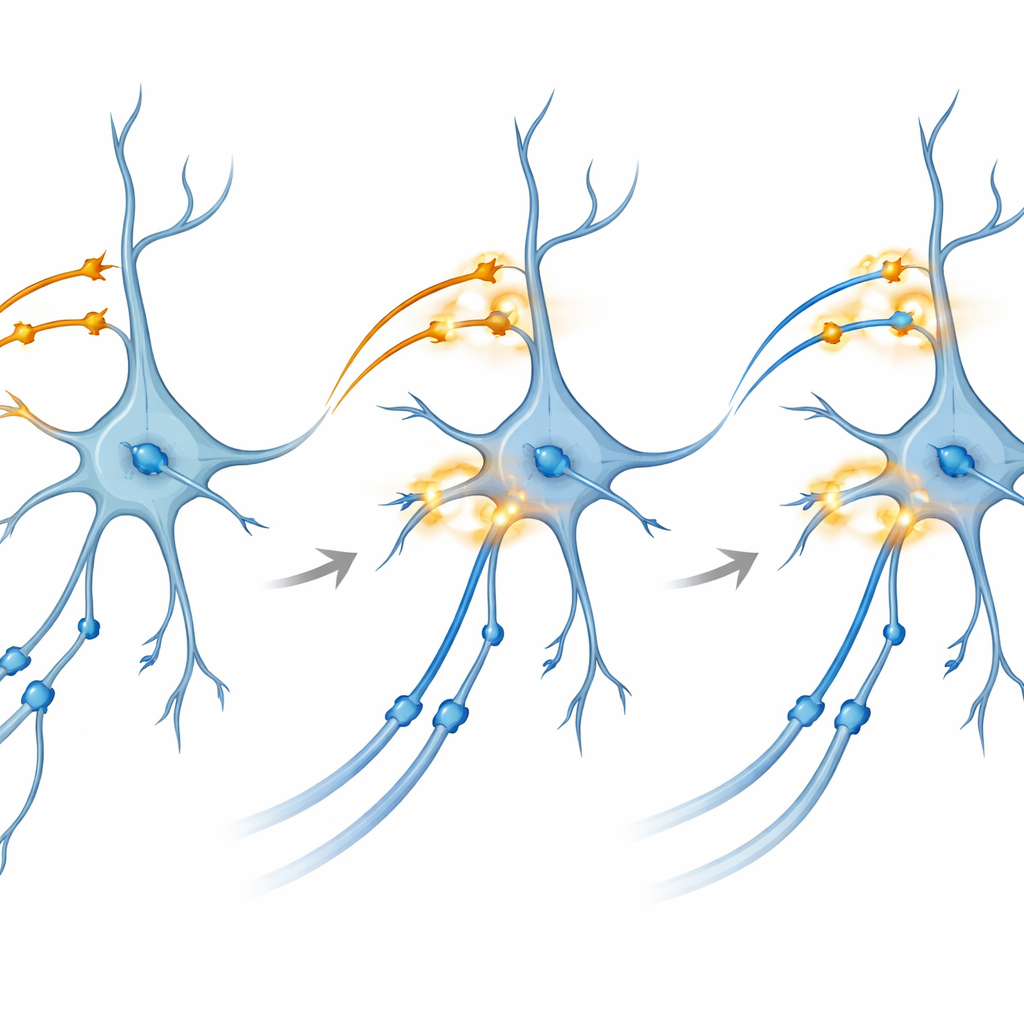
聚焦连接如何增强
为探究潜在机制,团队转而使用保持活性的脑切片。在这里他们可以分别控制CA3和投射到CA1的内嗅输入中的光激活蛋白。令人意外的是,单独对任一路径施加theta爆发式光刺激——模拟自然节律放电的模式——并不能可靠地产生长期增强(LTP),即被认为是记忆基础的突触持久增强。然而,当他们施加精确时序的双色爆发,使两条通路同时共同激活CA1时,CA3–CA1连接呈现出强大且持久的增强。阻断NMDA受体或特定的钙通道——两条众所周知的可塑性分子门控——会阻止这一效应,将该现象与经典的记忆形成生化通路联系起来。
这对记忆与疾病意味着什么
总体而言,这项研究描绘了空间学习为内嗅输入与海马内部连线之间的一种协调舞蹈。内嗅输入不仅携带有关位置与情境的信息;它们还充当一个强有力的调节旋钮,能够放大或抑制CA3–CA1纤维的活动,并在共同激活时驱动这些突触的长期增强。对非专业读者来说,关键结论是大脑的“GPS”并不依赖单一脑区,而是依靠一种伙伴关系:一个区域设定场景,另一个区域锁定细节。无论是衰老、损伤还是神经退行性疾病,对这种伙伴关系的破坏都可能解释为何人们在熟悉地点迷失方向,针对这些通路的干预或许为保护或恢复空间记忆提供新的途径。
引用: Huang, F., Temitayo Bello, S., Lau, S.H. et al. The perforant pathway and CA3-Schaffer collateral afferents coordinate to regulate spatial learning. Commun Biol 9, 364 (2026). https://doi.org/10.1038/s42003-026-09577-z
关键词: 空间记忆, 海马体, 内嗅皮层, 突触可塑性, 导航