Clear Sky Science · zh
ZFP42通过CRY1维持人类表皮干/祖细胞的干性与节律性转录
为什么皮肤的内部时钟很重要
每当你在夜间睡眠时,皮肤并不真正休息——它在修复、更新并为第二天的日晒和磨损做准备。本研究探讨了位于皮肤干细胞内的小型生物钟如何让这一更新过程按时进行,以及一种较少为人所知的因子ZFP42如何与钟蛋白CRY1协作,保持这些干细胞的青春性和功能性。理解时间调控与皮肤更新之间的这种联系,未来或可为衰老皮肤、伤口愈合和皮肤疾病的更好治疗提供线索。
皮肤的计时器
类似于响应光线的大脑主时钟,几乎每种组织都有自己的“外周”时钟。在表皮这一最外层皮肤中,基底层的干细胞和祖细胞不断分裂、向上推移并形成我们所依赖的保护性屏障。作者研究了来源于胎儿和成人的人类表皮干/祖细胞(EPSCs),以观察有多少基因以大约24小时的节律周期开关。他们发现大约十分之一的活跃基因在这些细胞中呈现日节律,并且许多关键基因的时序在胎儿与成人皮肤之间发生变化,表明随着我们衰老,皮肤细胞的生物钟也在变化。
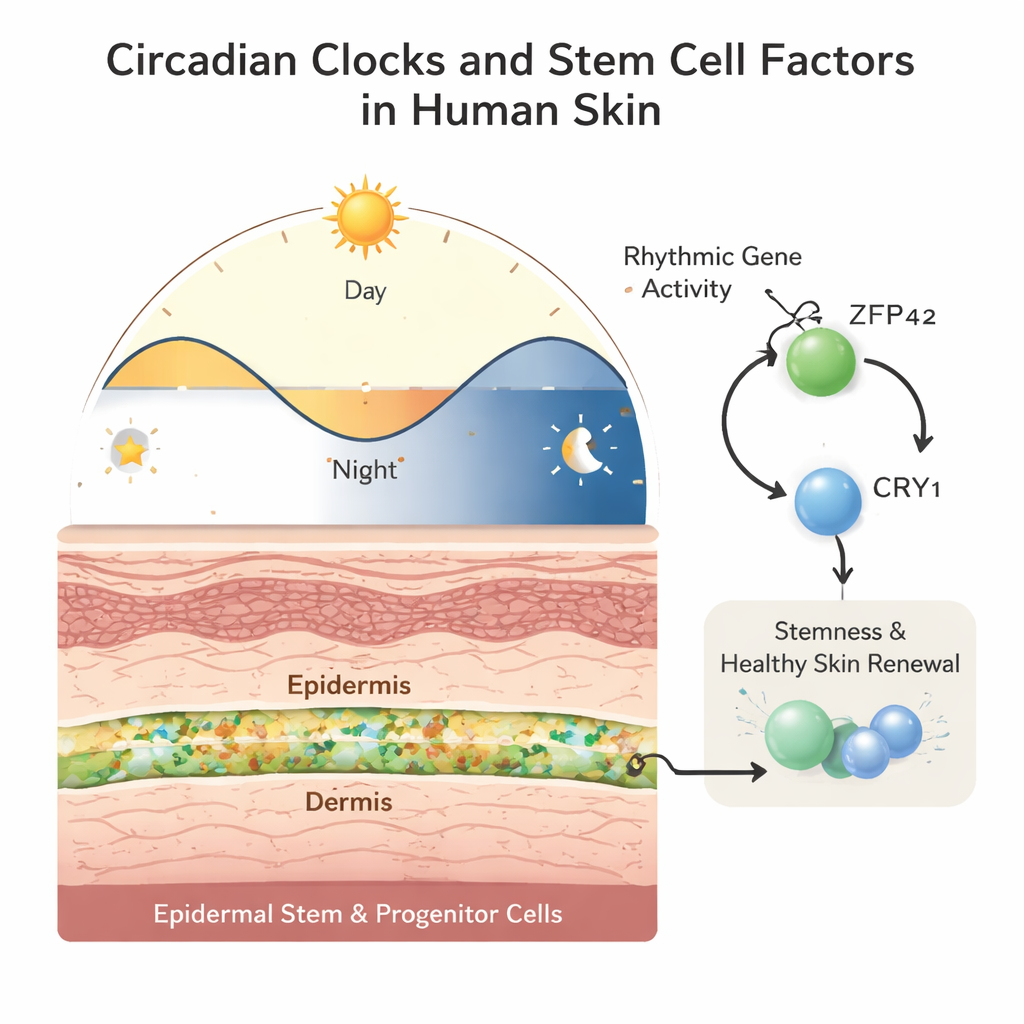
胎儿与成人皮肤:青年期节律更强
通过在培养皿中同步EPSCs并每三小时测量基因活性,研究团队发现核心钟基因——如BMAL1、PER1和CRY1——在胎儿和成人细胞中都呈现强烈的周期性。然而,节律性基因活动的整体“响度”(即振幅)在胎儿细胞中更高,而在成人细胞中则被削弱。许多共有的节律基因与DNA复制、细胞分裂和修复相关,这些过程对于维持干细胞健康至关重要。基因表达峰值的时序也发生了转移:成人细胞显示出延迟和改变的节律,尤其是在与抗病毒、防衰老和程序性细胞死亡相关的基因中,这暗示着随着皮肤成熟和老化,保护与更新的每日程序被重新调优。
生长与成熟的日常时序
当研究者查看仅在胎儿或仅在成人中呈节律的基因时,发现了显著差异。在胎儿EPSCs中,参与伤口反应、代谢和剧烈细胞分裂的基因波往往在日周期的较早时间达到峰值,这与其快速生长和再生能力相符。在成人EPSCs中,与构建皮肤屏障和驱动细胞完成分化相关的基因往往比控制DNA复制和分裂的基因更早达到峰值。这种分离表明,成体皮肤干细胞可能利用一天中的时间在使细胞准备形成保护性表面与在随后促进细胞增殖之间交替,以在保持屏障功能与抵御白天如紫外线等压力间取得平衡。
ZFP42与CRY1:维持干细胞青春性
进一步挖掘时,研究团队寻找可能位于这些节律性基因上游的调控分子。他们鉴定出ZFP42——更常被视为非常早期干细胞的标志——在胎儿EPSCs中高度活跃,并与胎儿节律基因的启动子强相关。当在年轻的EPSCs中降低ZFP42水平时,细胞分裂减少,积聚在细胞周期的早期阶段,并表现出更多分化和细胞死亡的迹象。相反地,在年长成人的EPSCs中提高ZFP42能改善其克隆形成能力,使其表现得更像年轻的干细胞。关键的是,ZFP42直接激活钟基因CRY1并且对其正常节律性是必需的。单独降低CRY1可模拟ZFP42缺失的许多效应——增殖变慢并且分化增加——而恢复CRY1能部分挽救生长缺陷,这表明ZFP42–CRY1轴对维持干细胞样行为至关重要。
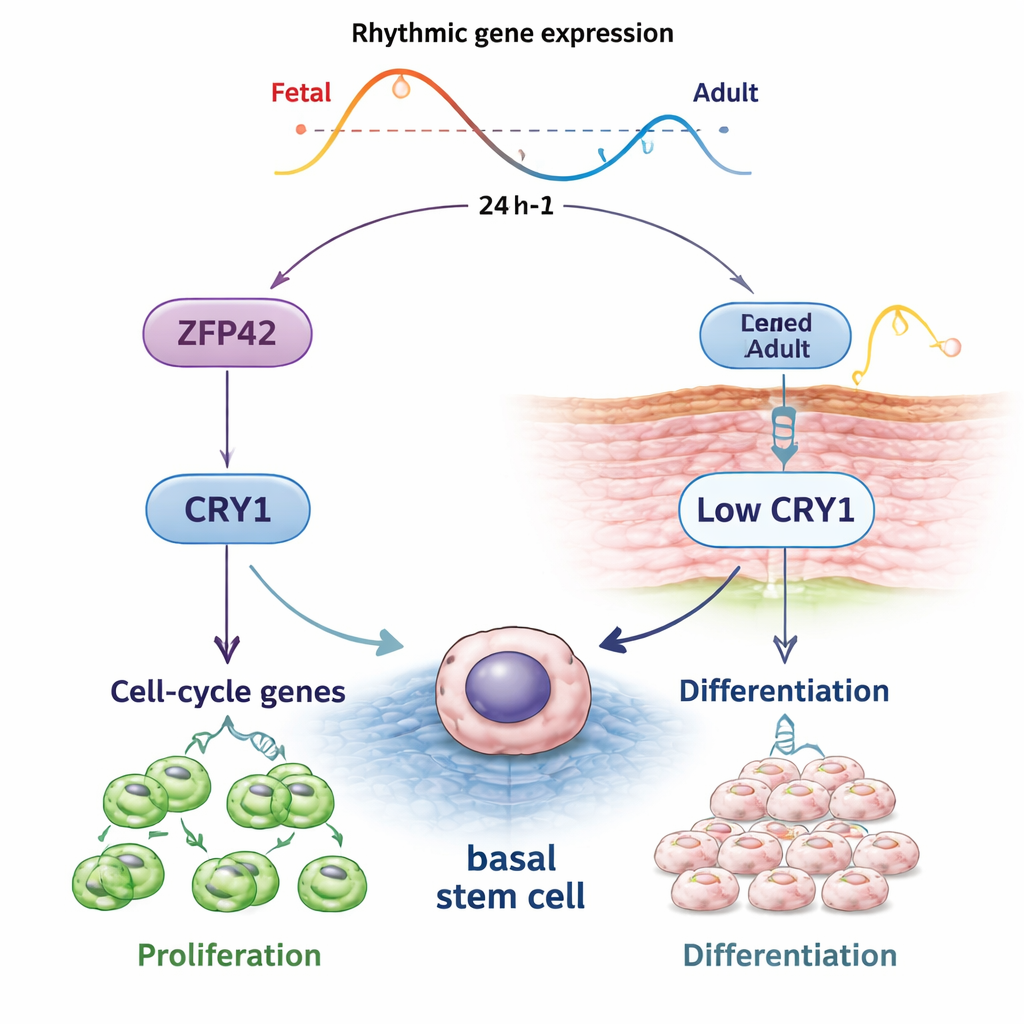
这对皮肤健康意味着什么
对非专业读者来说,结论是皮肤干细胞并非被动地对损伤和衰老作出反应——它们遵循由分子时钟编排的日常时间表,并且这一时间表会随生命过程发生变化。ZFP42充当与青年相关的开关,保持钟基因CRY1的活性与节律性,帮助表皮干细胞自我更新并防止过早成熟。随着与ZFP42相关程序随年龄衰弱,皮肤中受时钟控制的更新循环也似乎减弱。尽管这项工作是在培养细胞中完成的,尚需在活体组织中验证,但它提示通过调节ZFP42–CRY1通路或将治疗与皮肤内部时间对齐,未来有可能改善衰老皮肤、慢性伤口和其他这一最大器官疾病的治疗效果。
引用: Gao, S., Tan, H., Xu, S. et al. ZFP42 maintains stemness and rhythmic transcription in human epidermal stem and progenitor cells via CRY1. Commun Biol 9, 291 (2026). https://doi.org/10.1038/s42003-026-09576-0
关键词: 昼夜节律, 皮肤干细胞, 表皮, CRY1, ZFP42