Clear Sky Science · zh
负载脱水淫羊藿苷的间充质干细胞外泌体通过ACSL4介导的铁死亡改善小鼠银屑病
为何一种皮肤病会牵动全身健康
银屑病常被简化为“仅仅是皮肤问题”,但对于全世界大约6000万名患者来说,这种疾病可能伴随疼痛、瘙痒和情绪上的困扰。现有治疗方法虽然有效,但可能带来严重副作用或随时间失去疗效。本研究探索了一种有前景的新策略:基于传统中药中长期使用的植物成分,并借助由干细胞产生的微小生物“递送囊泡”,旨在抑制皮肤炎症的同时避免使用强效药物。
一种潜力未被充分发掘的植物成分
研究者聚焦于脱水淫羊藿苷(ANH),这是一种存在于淫羊藿中的天然分子,该药草数百年来用于增强活力和保健。ANH具有抗氧化和抗炎特性,已经被添加到一些保健产品中。然而,其在治疗银屑病方面的潜在作用尚未被明确检验。研究团队利用基于计算的“网络药理学”工具,绘制了ANH可能与驱动银屑病的蛋白质之间的相互作用网络。分析将ANH与若干部已被现代银屑病药物靶向的主要炎症和免疫通路联系起来,提示这种植物来源的化合物可能在降低疾病活动度方面具有实质性作用。
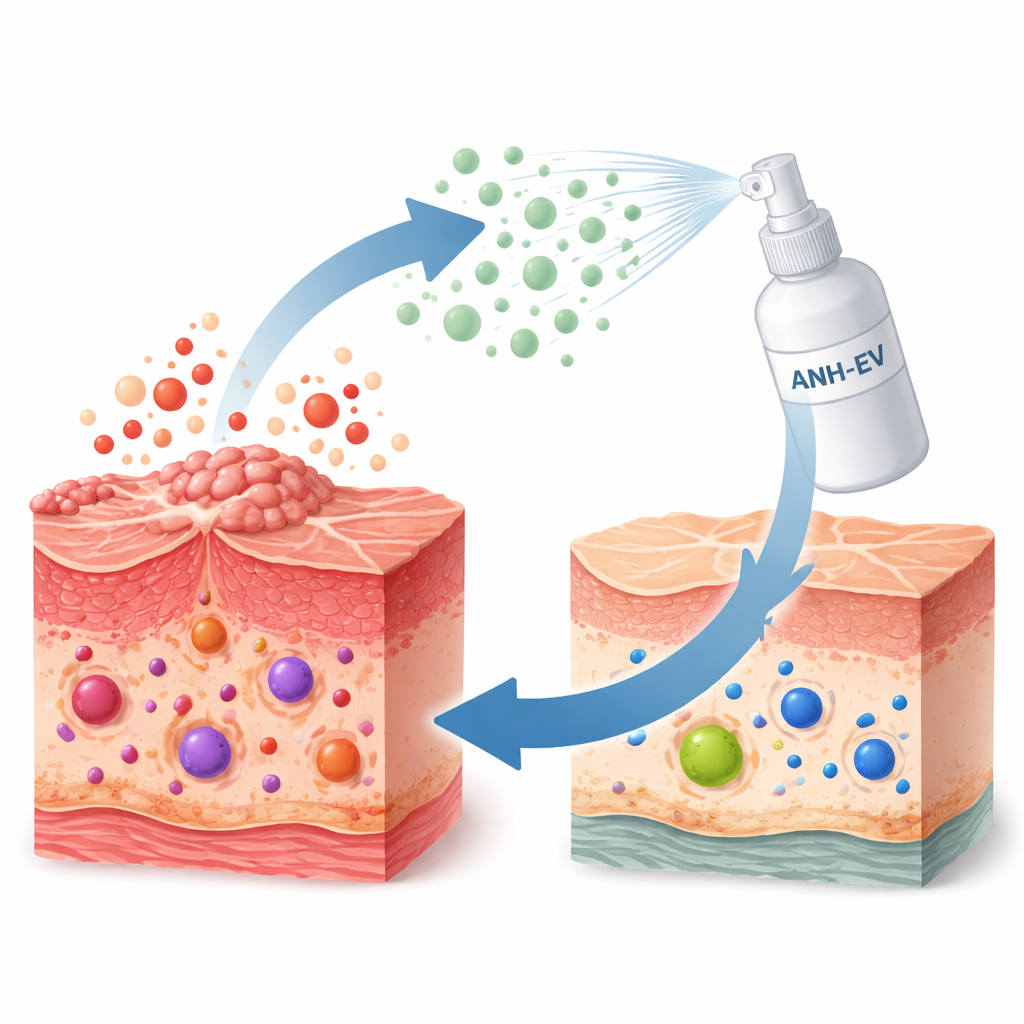
从培养皿到鼠皮
科学家首先在实验室培养的人类皮肤细胞上测试了ANH,这些细胞被诱导为过度活跃、处于炎症状态。ANH抑制了它们的异常增生并降低了关键的炎性介质,如白细胞介素-6和肿瘤坏死因子。随后,他们转向一种成熟的银屑病小鼠模型:含有免疫刺激剂伊马木喹莫德的外用霜会诱发与人类斑块相似的红、厚、鳞屑状皮损。当研究者将ANH喷涂于患处皮肤时,小鼠出现了更轻的病变,表皮更薄、鳞屑和发红减少,侵入皮肤和脾脏的过度活跃免疫细胞也更少。表征外层皮肤细胞过度增生的标志物也下降,指向疾病过程的真实缓解,而非仅仅是表面伪装。
将药物送到需要处的纳米囊泡
像许多植物化合物一样,ANH存在缺点:它在水中溶解性差,而且作为一种黄酮类化合物,理论上可能增加皮肤对阳光的敏感性。为了解决这些问题,团队将ANH封装在由间充质干细胞释放的细胞外囊泡中——这些天然的纳米级囊泡可以与其他细胞融合并高效递送货物,同时被机体良好耐受。研究者确认了囊泡的大小、形态与纯度,然后加载ANH。在实验室培养的皮肤细胞中,载有ANH的囊泡(EV-ANH)比单独的ANH或空囊泡更有效地抑制了炎性过度增生。在小鼠实验中,EV-ANH处理产生了更平滑的皮肤、更少的发红与增厚,以及较小的脾脏,表明对局部和全身炎症的控制都有所改善。
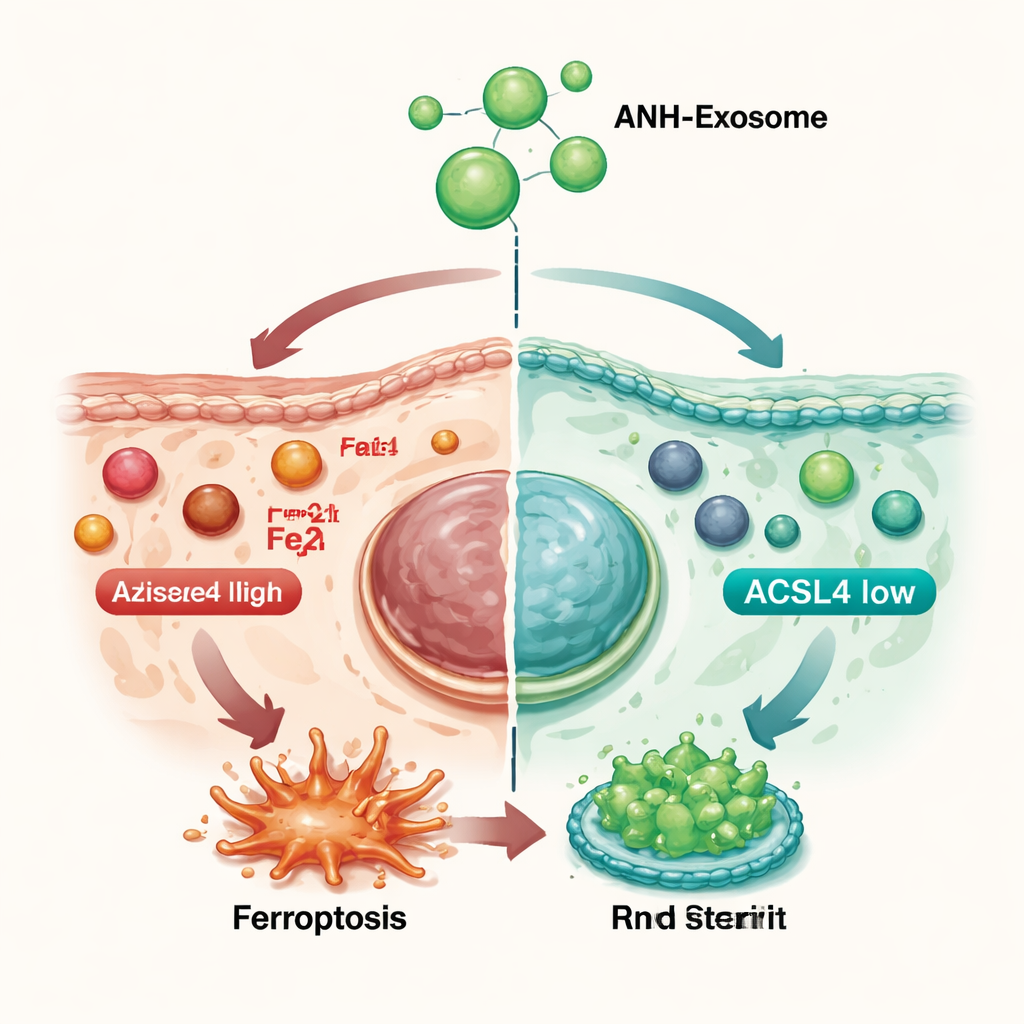
关闭一种类似“生物生锈”的细胞损伤方式
该研究的一个关键发现涉及铁死亡,这是一种新近被认识的细胞死亡形式,由铁和脂质氧化驱动——有点像生物学上的“生锈”。银屑病皮肤显示出铁死亡增强的迹象,这会进一步加剧组织炎症。通过分析小鼠皮肤中的基因表达,研究团队发现ANH强烈抑制与该过程相关的基因,尤其是名为ACSL4的基因,后者有助于合成促成铁死亡的不稳定脂质分子。在小鼠皮肤和人体皮肤细胞中,ANH降低了ACSL4水平和氧化损伤的标志物。当研究者使用已知的铁死亡抑制剂时,其对小鼠银屑病的改善效果与ANH相当。而当他们直接人为降低ACSL4时,ANH带来的额外益处缩小——这表明ANH在很大程度上通过关闭这一铁死亡开关发挥作用。
这对银屑病患者可能意味着什么
这项工作尚不能直接提供可供患者使用的现成治疗方案,但奠定了重要的基础。研究显示,一种传统植物成分可以被改良并通过干细胞来源的囊泡递送,以在小鼠中缓解类似银屑病的疾病,作用于免疫过度活化和由铁与脂质驱动的特定细胞损伤形式。如果在人类中证实有类似效果,负载ANH的囊泡未来可能成为一种外用疗法,通过恢复皮肤免疫与氧化环境的平衡来减轻斑块,且潜在副作用可能少于许多现有药物。
引用: Gao, Y., Ma, B., Jin, R. et al. Anhydroicaritin-loaded mesenchymal stem cell exosomes ameliorate psoriasis via ACSL4-mediated ferroptosis in mice. Commun Biol 9, 306 (2026). https://doi.org/10.1038/s42003-026-09575-1
关键词: 银屑病, 铁死亡, 脱水淫羊藿苷, 细胞外囊泡, 间充质干细胞