Clear Sky Science · zh
重新评估GPCR信号传导中Gα蛋白与反应元件的特异性
为什么微小的细胞开关对医学很重要
当今许多药物通过翻转位于细胞表面的分子“开关”来发挥作用,这些开关称为G蛋白偶联受体(GPCR)。这些开关通过称为G蛋白的辅助蛋白向细胞内部传递信息,最终开闭基因表达。几十年来,研究人员一直依赖简单的发光检测来判断某种药物或受体正在使用哪些G蛋白。本研究提出了一个基础但关键的问题:这些测试真能如我们想象地反映实际情况吗?在设计下一代精确药物时,我们还能信任这些测试吗?
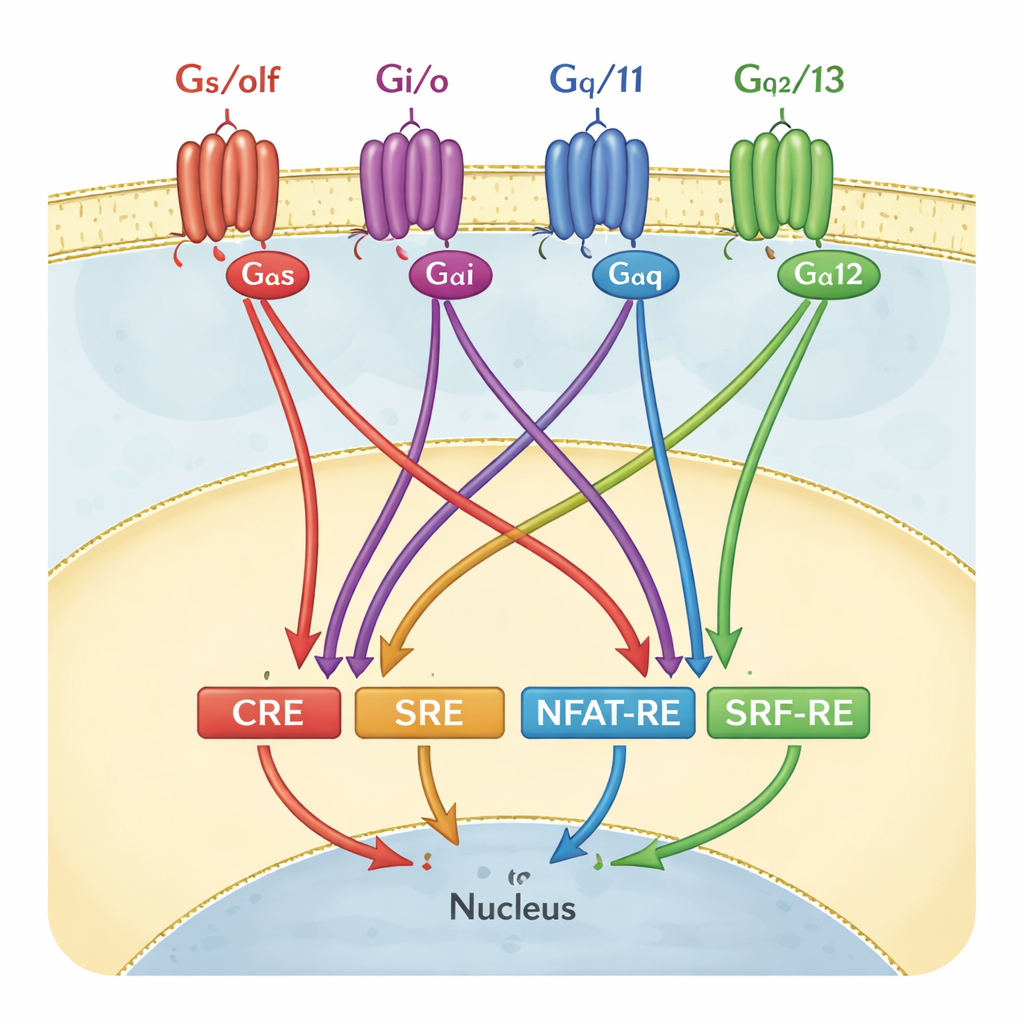
科学家通常如何解读GPCR信号
为了追踪GPCR活性,许多实验室使用报告基因测定。在这些实验中,细胞被工程化,使得当某个基因开关或“反应元件”被激活时,细胞会发光。其中有四种开关尤其常用:CRE、SRE、NFAT‑RE和SRF‑RE。长期以来,每一种通常被视为G蛋白某一分支的代表——例如CRE代表Gαs/olf家族,或SRF‑RE代表Gα12/13。在教科书和筛选流程中,这些配对常被近似画成一对一的接线图:激活特定G蛋白,只有对应的报告器发光。
将旧的接线图付诸检验
作者系统性地挑战了这一图景,使用通过基因编辑去除特定G蛋白家族——甚至全部G蛋白——的人源HEK293细胞。然后他们逐一重新引入单一的G蛋白类型。在这些细胞中,他们表达了九种不同的GPCR,代表既有高度选择性信号转导的受体,也有通过多种G蛋白伙伴传递信号的受体。通过测量四种报告器在不同药物浓度下的发光强度,研究人员可以看出哪些G蛋白对每个反应元件是真正必需的,哪些则能间接提供帮助。
重叠的通路,而非清晰的通道
结果推翻了整洁的一受体一报告器模型。尽管CRE仍主要依赖于Gαs/olf蛋白——经典的升高cAMP通路——其他G蛋白家族在Gαs/olf存在时亦能显著影响CRE活性。对于其余三种报告器SRE、NFAT‑RE和SRF‑RE,Gαq/11家族成为主要驱动者,尽管传统上SRE和SRF‑RE被关联到其他G蛋白分支。SRE和SRF‑RE的表现尤为相似,表明它们利用的是共享的下游机器而非截然分离的路径。在许多情况下,诸如Gα12/13和Gαi/o等额外G蛋白提供了额外推动或背景活性,突显出的是交叉对话的网络而非独立通道。
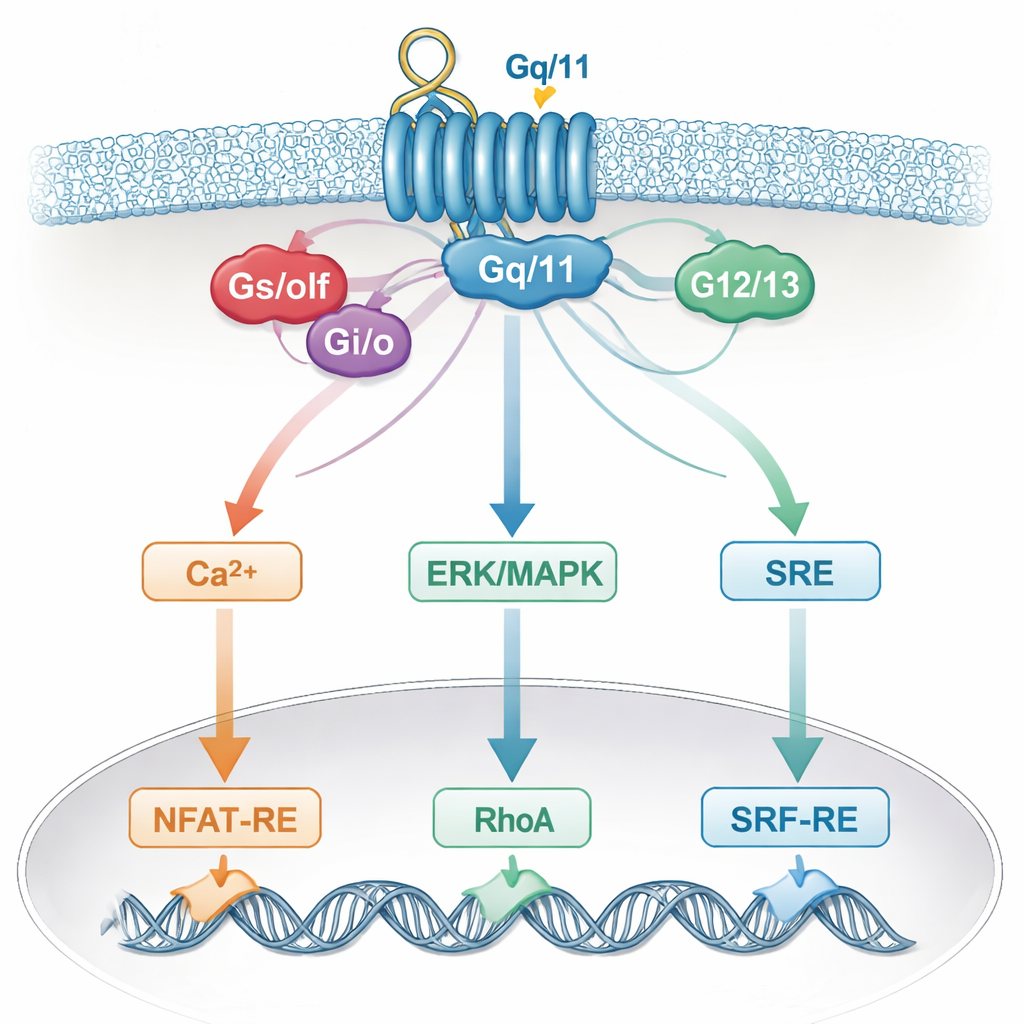
为何细胞网络会模糊我们的读数
这种特异性模糊很可能反映了真实细胞如何整合信号。单个受体可以激活多种G蛋白,这些G蛋白随后会汇聚到共同的信使分子,如钙、ERK/MAPK、RhoA或cAMP,以及共享的辅助因子如Gβγ亚基。这些共享通路又会作用于细胞核内相同的基因开关。因此,原本被认为仅响应某一G蛋白家族的报告器,实际上“监听”着多种信号。细胞类型特异性因素和存在的受体组合进一步增加了复杂性,这意味着从一种细胞体系得出的结论在另一种体系中可能并不成立。
这对药物发现意味着什么
对非专业读者来说,关键结论是:许多广泛使用的发光GPCR检测比标签所暗示的要不那么特异。它们仍能告诉我们受体是否被激活以及大致哪些广义通路被牵涉,但不能作为某一特定G蛋白家族——且仅该家族——被参与的可靠证据。作者认为,研究人员和药物开发者应将这些报告器视为粗略指示,并辅以能实时观察蛋白相互作用的更直接方法。这样可以更真实地描绘潜在药物如何引导细胞信号,避免在追寻更安全、更有针对性的疗法时走入误导性的捷径。
引用: Saito, A., Kise, R., Yamaguchi, S. et al. Re-evaluating Gα protein–response element specificity in GPCR signaling. Commun Biol 9, 288 (2026). https://doi.org/10.1038/s42003-026-09569-z
关键词: GPCR信号传导, G蛋白, 报告基因测定, 细胞信号网络, 药物发现