Clear Sky Science · zh
基于细胞且同种型选择性的G蛋白偶联受体激酶测定用于全面评估抑制剂
为何“调低细胞音量旋钮”很重要
我们的许多药物通过调高或调低位于细胞表面的受体活性来发挥作用,这些受体可感知激素、神经递质和药物。为了避免细胞持续过度刺激,这些受体必须被精确地关闭,部分由称为GRK的酶来控制。当GRK过度活跃时(如心力衰竭和某些癌症中所见),信号传导会出现紊乱。本研究开发了实用的基于细胞的测试,用以测量实验分子阻断特定GRK的能力,帮助科学家设计能更精细调控这些关键细胞“音量旋钮”的更聪明药物。
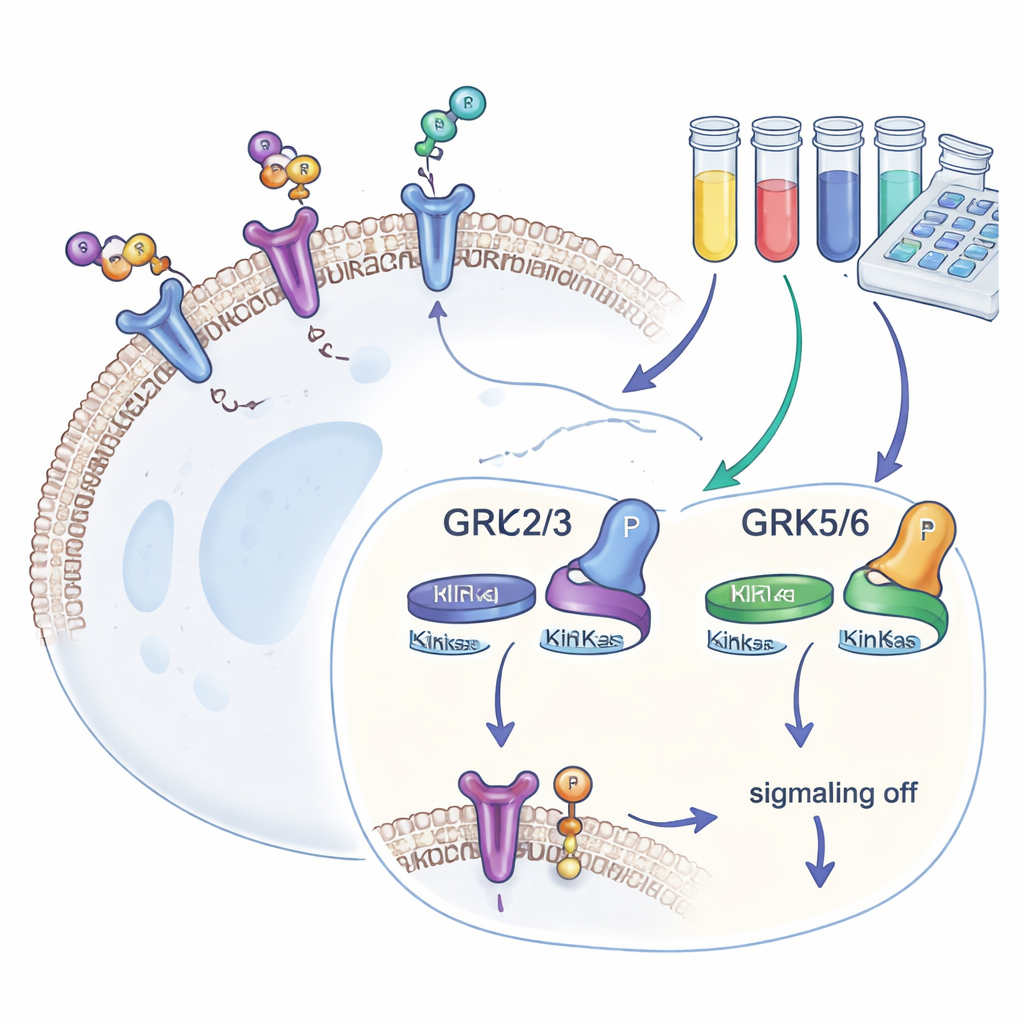
细胞表面的门卫
我们的细胞携带数百种G蛋白偶联受体(GPCR),它们检测外界信号并将其转化为细胞内反应。当GPCR被激活后,GRK会在其尾部附加小的磷酸“标记”。这些标记吸引另一种蛋白——β- arrestin(β-逮捕素),它停止进一步信号传导并常常将受体内吞。四种常见的GRK同种型——GRK2、GRK3、GRK5和GRK6——分布在许多组织中。因为它们决定了GPCR响应的强度,而且在心力衰竭、癌症和成瘾等疾病中其水平会改变,药物开发者热衷于寻找既有效又具有选择性的GRK抑制剂。
在细胞内构建干净的测试平台
以前的大多数GRK研究依赖计算建模或试管化学,这些方法可以揭示抑制剂结合的紧密程度,但不能反映其在拥挤的活细胞内部的表现。为填补这一空白,作者改造了人源HEK293细胞,去除了四种常见GRK,然后每次仅重新引入一种GRK同种型。每个细胞系还携带一种研究充分的受体——β2-肾上腺素能受体,并对其进行了标记,以便通过灵敏的抗体测定读出其在特定位点(称为T360/S364)上的磷酸化。因为该位点仅被GRK修饰,所检测到的磷酸量就成为在活细胞内定量衡量每种GRK同种型活性的直接指标。
分辨优、劣与非特异性抑制剂
利用这一工具包,团队测试了一组市售的GRK抑制剂。首先他们将化合物分为主要靶向GRK2/3的一组和靶向GRK5/6的另一组。通过比较每种分子在仅表达单一GRK亚型的细胞中降低受体磷酸化的程度,研究者能绘制出其在真实细胞环境下的选择性图谱。一种名为8h的化合物被确定为对GRK2/3最有效的抑制剂,而化合物18在选择性抑制GRK5/6方面最为突出。一些广泛使用的分子在测试剂量下效果甚微,可能是因为它们难以进入细胞;而一种强效的共价抑制剂则破坏了细胞健康,使其不适合用于成像实验。
从化学特征到受体行为
为证明这些抑制剂影响的不仅仅是单一测试受体,而是更广泛的GPCR生物学,作者还检查了几种医学上重要的受体,包括μ-阿片受体和加压素V2受体。他们通过显微镜同时测量了磷酸化和受体内吞。单独使用8h或18可部分减少许多靶点的磷酸化和受体内移,但同时使用8h和18几乎完全阻止了这些变化,使受体保持在细胞表面。进一步追踪β-逮捕素募集的实验证实,同样的化合物可在由重叠GRK集合调控的其他受体上调节信号传导。
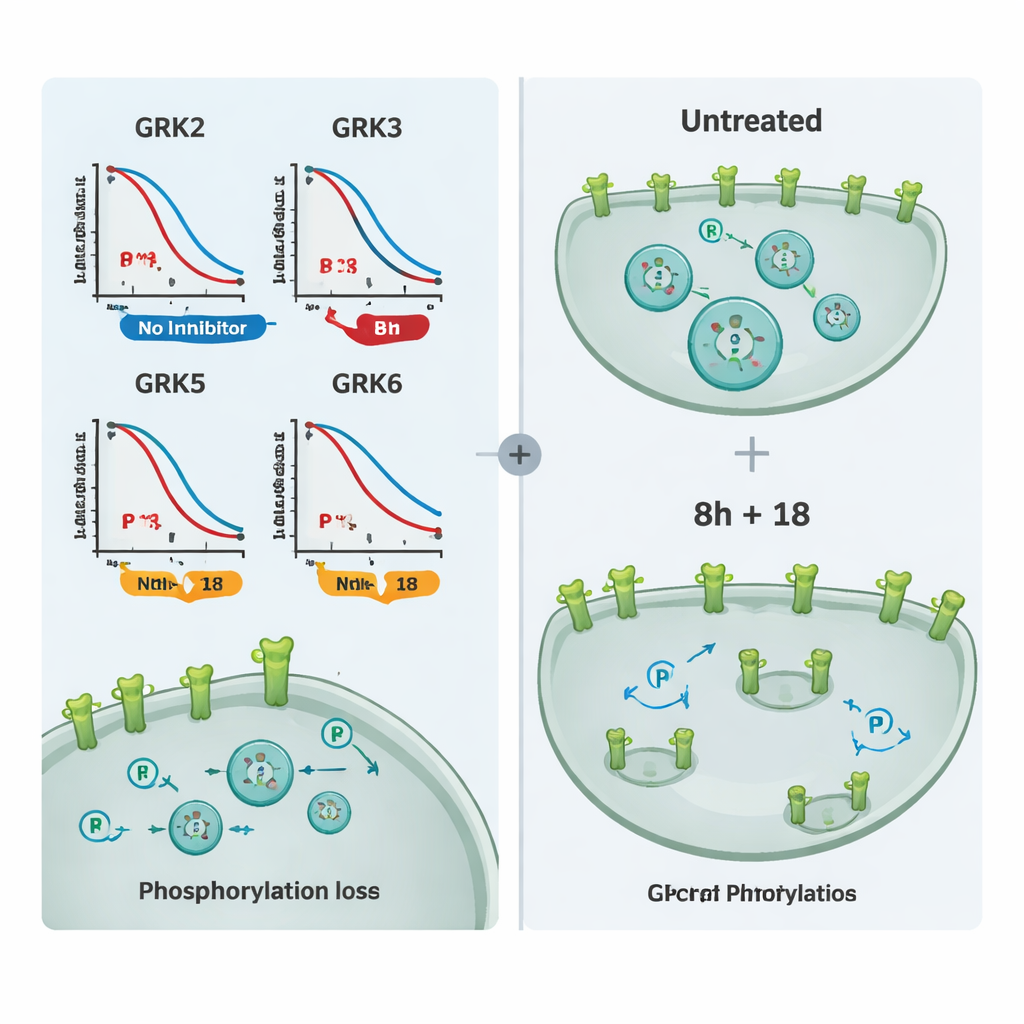
这对未来药物意味着什么
对非专业读者来说,关键结论是该研究提供了一套可靠的基于细胞的测试工具——以及两种特别有用的工具化合物8h和18——使研究人员能够在活细胞中直接观察不同GRK同种型是如何被调低的。研究人员不再需要依赖简化的试管数据进行推测,而可以并排比较候选抑制剂,判断它们主要影响GRK2/3、GRK5/6还是同时影响这四种同种型。这种清晰度应有助于加速开发能更精确调节GPCR信号传导的药物,可能为治疗心脏病、癌症、疼痛障碍及其他与信号平衡失调相关的疾病带来益处。
引用: Blum, N.K., Kiefer, M.C., Decker, A. et al. Cell-based and isoform-selective G protein-coupled receptor kinase assays for comprehensive inhibitor evaluation. Commun Biol 9, 287 (2026). https://doi.org/10.1038/s42003-026-09568-0
关键词: GPCR 信号传导, GRK 抑制剂, β-肾上腺素能受体, 基于细胞的测定, 药物发现