Clear Sky Science · zh
HBP1增强黄体酮受体活性并上调IGFBP1表达,驱动子宫内膜蜕膜化
这对生育意味着什么
妊娠开始时,胚胎只有在子宫内膜完成一种称为蜕膜化的重要改造后才能着床。许多不孕和反复胚胎移植失败的病例仍无法解释,越来越多的证据表明问题常常出在子宫内膜的这次改造而非胚胎本身。本研究揭示了一个此前被低估的分子“开关”——转录因子HBP1,它有助于为胚胎着床准备子宫内膜,可能为诊断和治疗着床问题提供新的思路。
子宫内膜中的隐秘开关
子宫的内膜随月经周期有节律性变化。在雌激素作用下它增殖,而在孕激素作用下成熟为对胚胎具有接受性的基质。研究者将注意力集中在人类子宫内膜基质细胞上,这些结构性细胞在着床时转变为更大、分泌性更强的蜕膜细胞。通过挖掘既有的基因表达数据并开展新实验,他们发现随着这些基质细胞开始蜕膜化,HBP1水平显著上升,提示HBP1是准备子宫的内在时序系统的一部分。
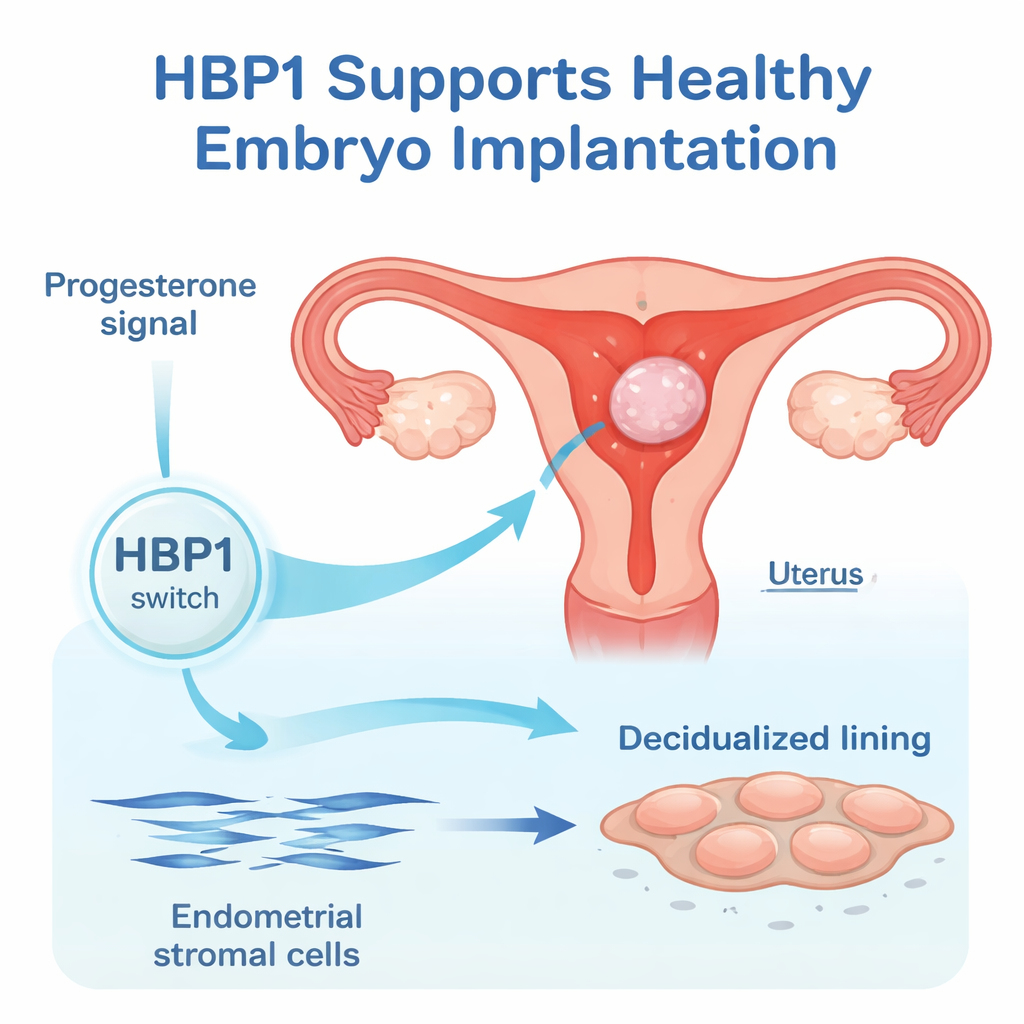
帮助细胞改变形态并减缓增殖
为了检验HBP1是仅仅存在还是确实必需,研究团队在培养的人类子宫内膜基质细胞中调节了其表达水平。当降低HBP1时,经典的蜕膜化标志物如IGFBP1、FOXO1和催乳素在RNA和蛋白水平上均下降。细胞也未能经历从纤细梭形向更宽、更多边形形态的典型形变,而是持续增殖。相反,当提高HBP1时,IGFBP1水平上升,细胞分裂减缓。这些发现共同表明,HBP1有助于细胞退出生长模式,进入支持早期妊娠的特化蜕膜状态。
在细胞内微调激素信号
孕激素及其受体对子宫准备至关重要,但并非所有组织对激素的反应都一样强。研究者发现孕激素信号本身会提升HBP1水平,形成一个正反馈环。值得注意的是,降低HBP1并未改变细胞制造的孕激素受体数量,但却削弱了若干重要孕激素响应基因的活性,包括FKBP4、FKBP5、FOSL2和辅助激活因子SRC1。通过全基因组方法,他们显示HBP1与这些基因附近结合,并伴随特定组蛋白修饰H3K4me3的增加,该修饰标志着DNA区域的转录活性。本质上,HBP1并不直接开关受体,而是使受体的靶基因更容易被读取。
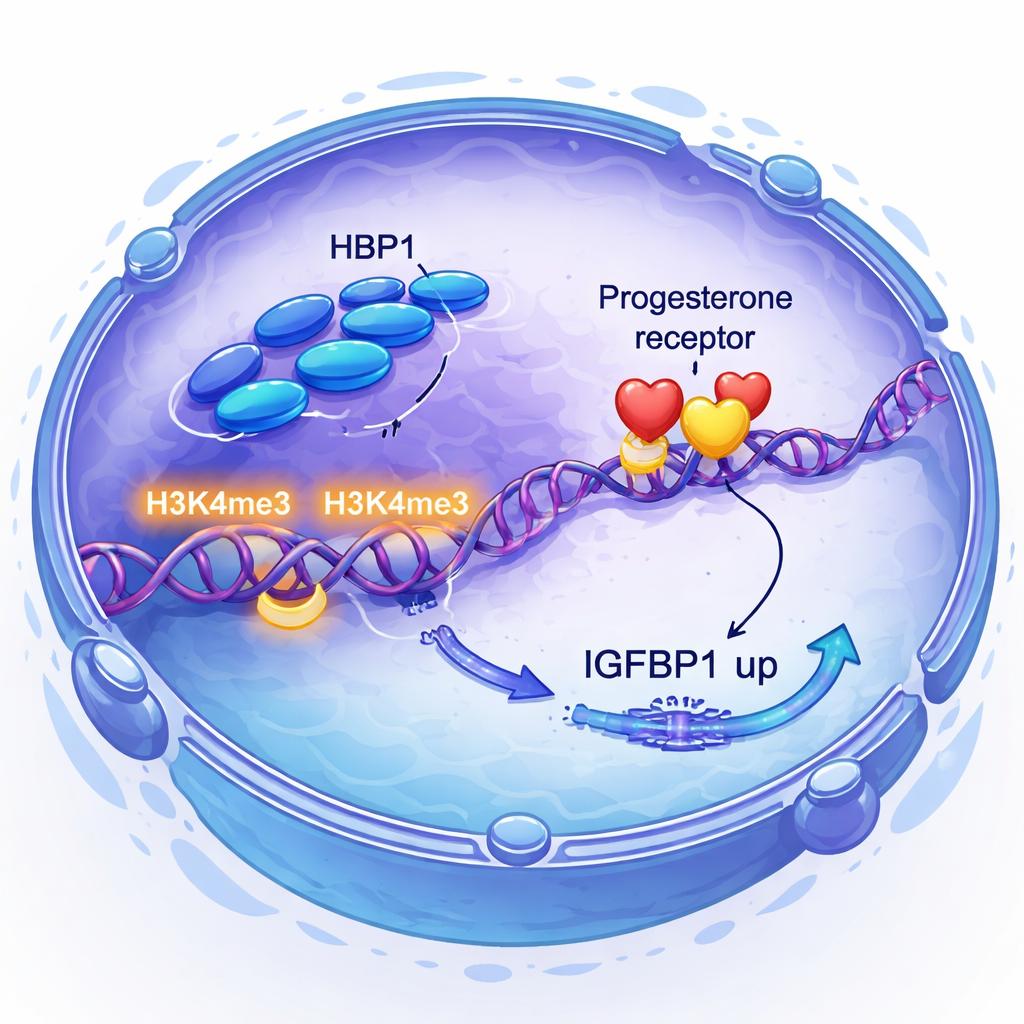
对关键着床信号的直接控制
接着团队探查HBP1如何与IGFBP1相连。IGFBP1长期被用作健康蜕膜化的标志物,并被认为影响胚胎与子宫的通讯。通过结合RNA测序与染色质免疫沉淀测序,他们显示HBP1直接结合在IGFBP1的启动子区域,并在那里增加H3K4me3,从而驱动IGFBP1产量上升。他们还发现,降低HBP1会激活PI3K–AKT通路——一种与生长相关的信号通路,当其过度活跃时会抑制IGFBP1。抑制该通路可以恢复IGFBP1水平。因此,HBP1通过两条途径支持蜕膜化:直接启动IGFBP1,以及抑制会遏制蜕膜基因表达的生长信号。
将分子缺陷与着床失败联系起来
最后,研究者比较了反复移植失败女性的子宫内膜样本与在中分泌期(着床准备期)采集的生育良好对照组组织。反复失败的女性其HBP1及下游分子IGFBP1、FKBP5和FOSL2的水平明显偏低,尽管两组间孕激素受体水平相近。这一模式契合“孕激素抵抗”的概念——激素存在,但组织无法做出充分反应,因为像HBP1这样的关键支持因子缺失。
对患者的意义
通俗地说,这项研究表明HBP1像子宫内膜控制面板上的一个主控开关。适当开启时,它帮助放大孕激素信号,促使细胞停止增殖并分化特化,并提升诸如IGFBP1等有利于着床分子的产生。当HBP1过低时,内膜在显微镜下可能看起来正常,但功能上表现不佳,导致胚胎无法扎根。未来了解并检测HBP1及其网络,或可帮助医生识别有着床问题风险的女性,并激发恢复子宫受容性的新的治疗策略。
引用: Guo, Y., Tian, W., Nie, C. et al. HBP1 enhances progesterone receptor activity and IGFBP1 expression driving endometrial decidualization. Commun Biol 9, 286 (2026). https://doi.org/10.1038/s42003-026-09567-1
关键词: 子宫内膜蜕膜化, 胚胎着床, 孕激素信号, 不孕症, HBP1