Clear Sky Science · zh
胶质母细胞瘤干细胞显示转录学相关的空间组织
为何脑癌中的细胞模式重要
胶质母细胞瘤是最具侵袭性的脑癌之一,数十年来生存率几乎没有改善。许多实验室研究一种特殊的肿瘤细胞——胶质母细胞瘤干细胞,这类细胞能在治疗后重新生长肿瘤。在这项研究中,研究者提出了一个看似简单但影响深远的问题:这些细胞在培养皿中的排列方式——肉眼在普通显微镜下能看到的模式——能否揭示其内部哪些基因处于活跃状态,并可能加速新疗法的筛选?
图片里藏着的不止表象
为探究这一想法,团队收集了约17,000张来自15条不同患者来源的胶质母细胞瘤干细胞系的时间序列显微镜图像,这些细胞在平底塑料培养皿上培养。所用图像为标准相差显微镜拍摄,类似许多生物实验室每天都会生成的影像。乍看之下,图片只是显示细胞逐渐填满培养皿,但仔细观察可见细胞组织方式存在显著差异:有些细胞形成了长而对齐的条状,方向一致;而另一些则以更圆的团簇生长,方向更随意或出现重叠层。这些视觉模式暗示,细胞的内部“个性”可能体现在群体行为中。

将纹理翻译为生物学信息
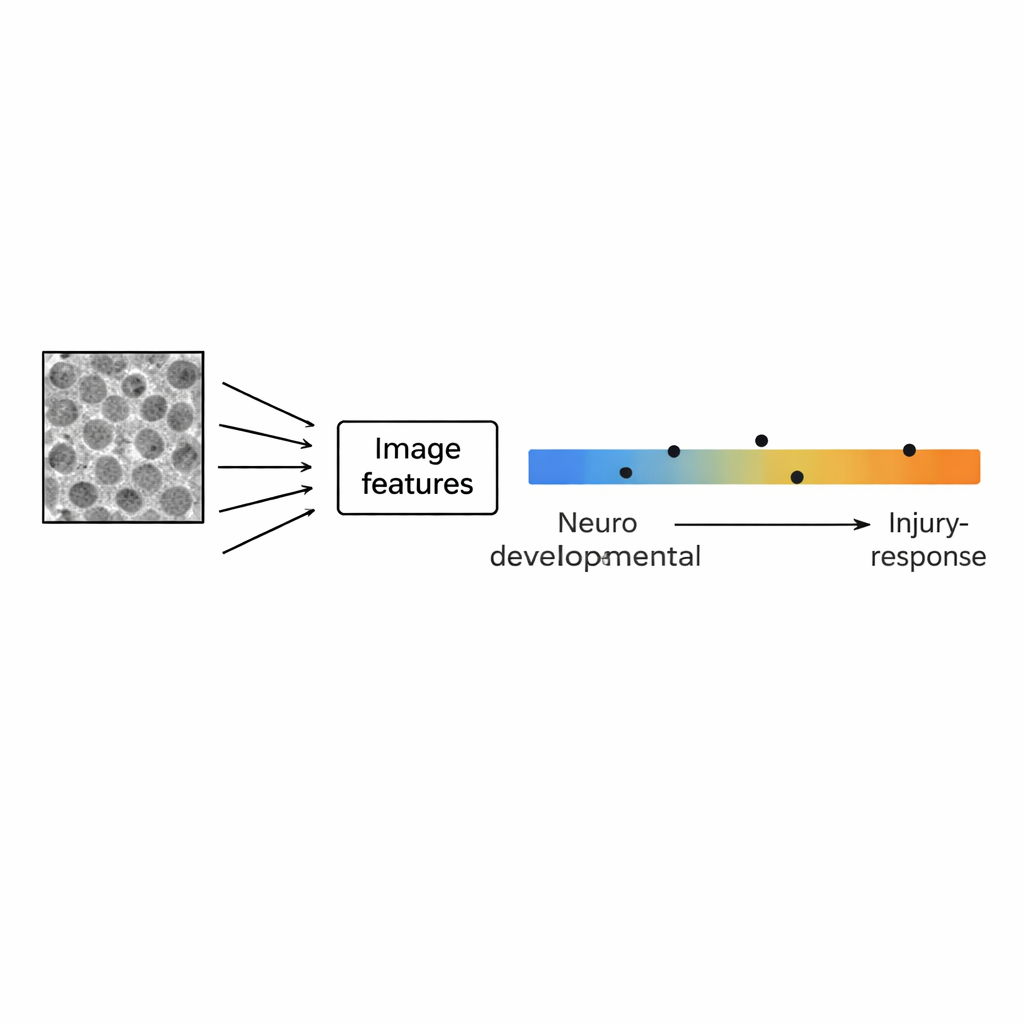
研究者没有聚焦单个细胞,而是将每张图像视为一个整体模式。借助开源软件,他们将每张图片转换为29个数值特征,描述图像的纹理和结构——例如不同尺度下的颗粒感、相邻像素相似的频率,以及不同方向上的对比强度。随后,他们将这些基于图像的指纹与同一细胞系的基因活性谱进行比较,使用111个基因签名来表征脑发育、正常脑细胞类型以及与炎症相关的状态。主成分分析这一统计技术显示,图像模式的主要变异轴对应一个已知的生物学梯度:一端是与正常脑发育相关的基因(神经元、干细胞、支持性的胶质细胞)表达较高,另一端则是与损伤、炎症以及更具侵袭性的“间充质”行为相关的基因表达较高。
随培养生长仍然持续的模式
解释细胞图像的一大挑战在于,培养物从稀疏到高密度时外观会发生显著变化。作者通过将图像按细胞密度分为九个等级并分别重新分析来应对这一点。值得注意的是,空间模式与基因活动之间的关联在所有生长阶段都成立:无论培养皿是刚接种还是几乎融合,更“类发育”细胞系的图像往往显示更平滑、更均匀的纹理,而更偏向损伤反应的细胞系则表现出更不规则、异质的结构。然而,承载这一信号的具体图像特征会随密度而变化——例如,在低密度时反映小尺度颗粒感的指标最具信息量,而随着细胞拥挤,描述对称性和均匀性的特征变得更重要。这表明底层生物学限制了模式随时间演变的方式,即便其物理外观在变化。
从显微镜快照到分子预测
为检验仅靠图像能否预测细胞系在发育—损伤梯度上的位置,团队训练了简单的统计模型,输入仅为29个图像特征,输出为基于基因表达的评分。一个能自动选择最有信息组合的模型准确再现了原始15条细胞系的梯度,并在另外四条测试细胞系上显示出令人鼓舞的一致性。最有用的图像特征既包括纹理描述符,也包括结构尺寸的度量,这与模式分析的结论相呼应。重要的是,该模型能在标准、无标记的明场图像上工作——无需荧光染料或特殊显微镜——为将常规成像转化为快速、廉价的细胞状态读出提供了可行路径。
这对未来脑癌研究的意义
对非专业读者来说,关键信息是:癌细胞的外观及其作为群体的排列方式,可以作为窥视其所使用基因的窗口。在胶质母细胞瘤干细胞中,简单的明场图像就能捕捉到足够的信息,以区分更像正常发育中脑细胞的群体与偏向损伤和炎症驱动状态的群体——后者通常与更具侵袭性的疾病相关。未来,这类基于图像的“指纹”方法可帮助科学家通过观察药物或基因变动如何推动细胞沿这一梯度移动,快速筛选候选药物或遗传改变,而无需每次都进行RNA测序。更广泛地说,这项工作提示,活细胞培养的结构不仅具视觉上的趣味——它还编码了可用合适工具解码的生物学意义信息。
引用: Ayyadhury, S., Sachamitr, P., Kushida, M.M. et al. Glioblastoma stem cells show transcriptionally correlated spatial organization. Commun Biol 9, 208 (2026). https://doi.org/10.1038/s42003-026-09566-2
关键词: 胶质母细胞瘤干细胞, 细胞成像, 空间组织, 基因表达, 高通量筛选