Clear Sky Science · zh
放射性核素激发的动态疗法诱导互补的免疫原性坏死性凋亡和凋亡癌细胞死亡途径
将癌症的伎俩反过来对付它自己
癌症以规避我们最佳治疗而臭名昭著,尤其是那些会在全身扩散的侵袭性乳腺肿瘤。本研究探索了一种称为放射性核素激发的动态疗法(RaST)的创新方法,它利用医学影像示踪剂与光响应纳米颗粒杀死癌细胞,同时唤醒免疫系统。对读者而言,这项工作重要在于它表明现有的影像工具和智能材料可能被重新利用,产生更持久的、由免疫驱动的癌症控制,而非短暂的肿瘤缩小。
从内部点亮肿瘤的新途径
传统的光疗只能作用于外部光束能到达的部位,比如皮肤或表浅肿瘤。RaST 绕过了这一限制,使用一种放射性糖类——类似于用于 PET 扫描的示踪剂——它自然积聚在快速生长的癌细胞中。当该示踪剂在肿瘤中传播时,会发出一种微弱的蓝色光,称为切伦科夫辐射。研究人员设计了包覆有肿瘤靶向蛋白的小型二氧化钛纳米颗粒,使它们也能聚集到肿瘤部位。当示踪剂和纳米颗粒相遇时,内部光会激活这些颗粒,进而产生一阵阵活性氧物种——这些高度反应性的分子从内部损伤癌细胞。
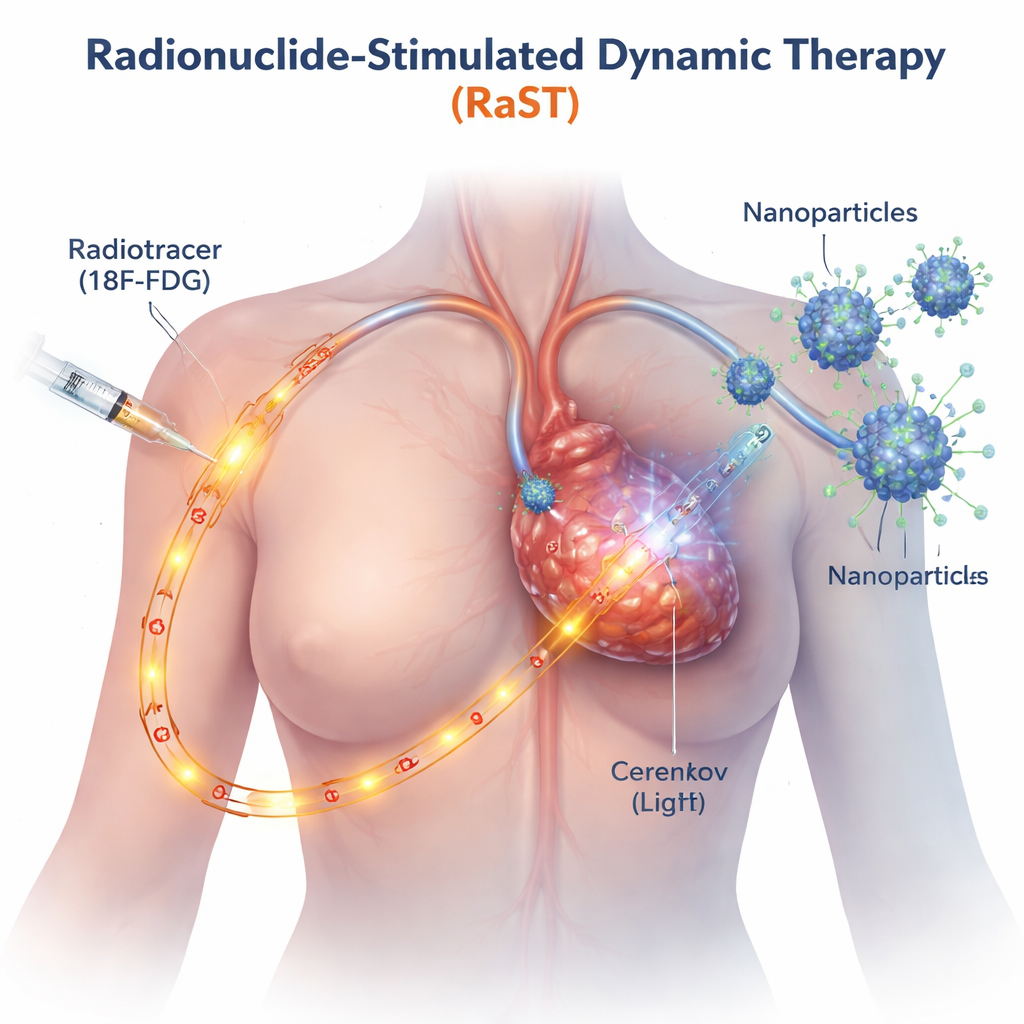
触发两条截然不同的细胞死亡路径
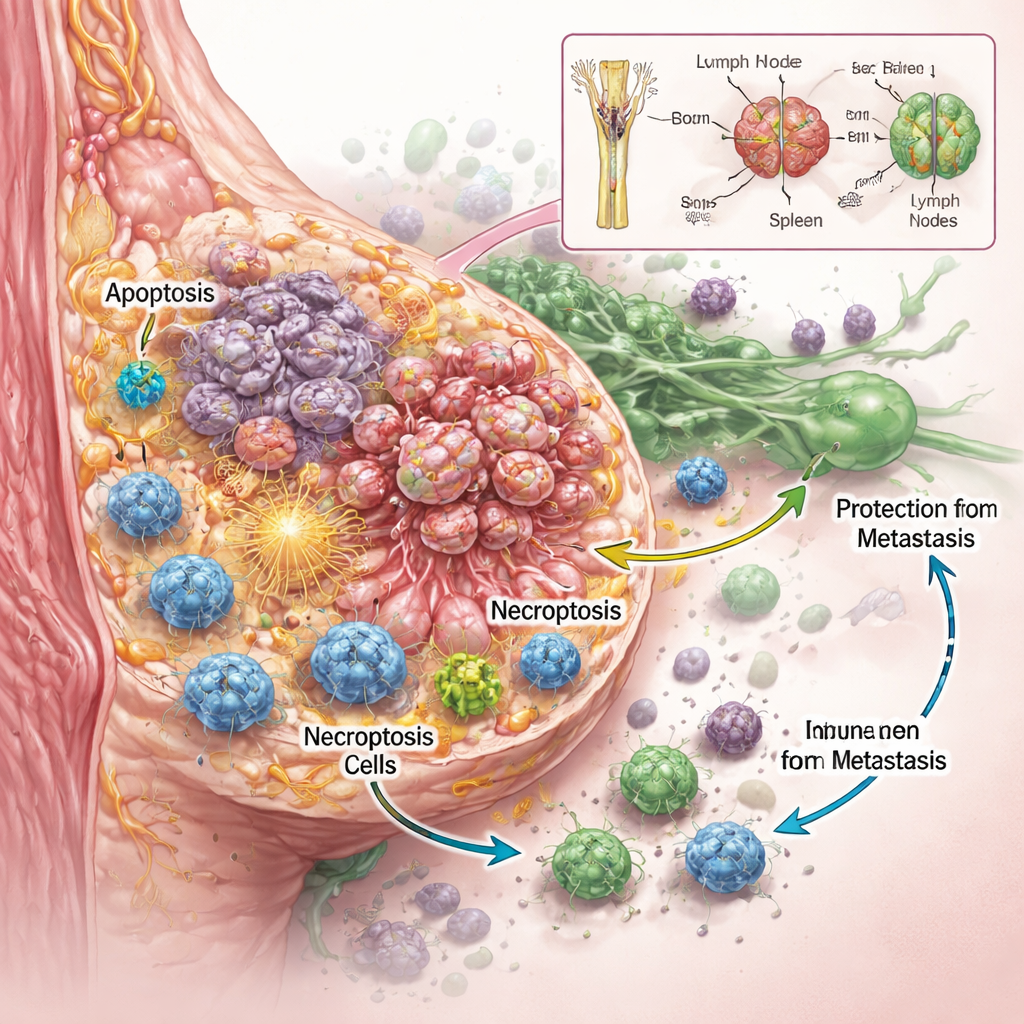
团队不仅想知道 RaST 是否能杀死癌细胞,还要弄清楚其方式。在多种侵袭性乳腺癌细胞系的体外实验中,他们发现精心调配剂量的放射性示踪剂和纳米颗粒协同作用,比任何单一组分都更有效地损伤肿瘤细胞,即便是那些已知对标准化疗有抵抗的类型。细致的成像和蛋白测定显示,RaST 同时激活了两种受调控的细胞死亡程序。一种是凋亡,常被描述为细胞的“自杀”,细胞以有序方式自我拆解。另一种是坏死性凋亡,这是一种更具爆炸性的死亡形式,细胞肿胀、破裂并向周围释放分子应激信号。这些称为损伤相关分子和炎性细胞因子的信号,可以像照明弹一样吸引并激活免疫细胞。
动员免疫系统以实现持久控制
为了解这种炎性肿瘤杀伤是否在生物体内也重要,研究者在小鼠乳腺癌模型中测试了 RaST。在缺乏关键免疫防御的小鼠中,尽管局部细胞死亡大量产生,RaST 对肿瘤生长或肺转移几乎没有抑制作用。但在免疫功能完整的小鼠中,相同的治疗产生了部分和完全的肿瘤反应并阻止了肺部转移。暴露于 RaST 的肿瘤充斥着免疫细胞——尤其是髓系细胞如巨噬细胞和树突状细胞——这些细胞擅长吞噬死亡物质并向 T 细胞呈递肿瘤片段。血液检测显示随时间推移出现免疫刺激和免疫调节信号的波动,表明 RaST 先点燃针对癌症的攻击,随后随着肿瘤缩小或稳定而转向更平衡的状态。
追捕隐匿残余并防范复发
即便在那些看似被 RaST 完全治愈的小鼠中,一种高灵敏度的成像染料后来仍显示在淋巴结内藏有微小的残余癌细胞。值得注意的是,这些动物在数月内仍未出现新肿瘤或远处转移。化学分析显示,二氧化钛纳米颗粒最初在骨骼和肝脏中丰富,随后逐渐重新分布到脾脏和淋巴结——恰恰是免疫细胞巡逻的枢纽。这种缓慢迁移可能为免疫细胞提供持续的局部活性氧来源,帮助它们识别并控制这些隐匿的癌细胞残余,防止其再生或扩散。
这对未来癌症护理可能意味着什么
简言之,这项工作表明 RaST 不仅仅是另一种毒杀肿瘤细胞的方法。通过将放射性示踪剂、光响应纳米颗粒与机体自身防御相结合,它将癌细胞推入两种强烈向外发出警报的程序性死亡状态,从而大幅唤醒免疫系统。在免疫功能完整的动物中,这导致对侵袭性乳腺肿瘤的持久控制并阻断转移,即使少量癌细胞仍潜伏在淋巴结中。虽仍需大量工作才能在更广泛的人群中开展临床测试,但该研究指向了未来的治疗方向:不只是追求肿瘤缩小,而是重塑癌症、细胞死亡与免疫之间的关系,让机体能够在更长时间尺度上帮助控制疾病。
引用: Egbulefu, C., Black, K., Su, X. et al. Radionuclide-stimulated dynamic therapy induces complementary immunogenic necroptosis and apoptosis cancer cell death pathways. Commun Biol 9, 275 (2026). https://doi.org/10.1038/s42003-026-09555-5
关键词: 乳腺癌, 纳米颗粒, 免疫疗法, 放射性核素治疗, 坏死性凋亡