Clear Sky Science · zh
糖原自噬是支持通过STBD1结构演化实现代谢适应的古老双侧动物通路
牡蛎如何揭示隐藏的能量妙招
动物在艰难时期通过动用储存的燃料生存,但它们并非都依赖同一种“电池”。这项研究检视了太平洋牡蛎,表明与许多依赖脂肪的动物不同,牡蛎在很大程度上依靠以糖原形式存在的储备糖。该研究揭示了一条鲜为人知的细胞回收通路——糖原自噬——帮助牡蛎快速耗尽并补充其糖类储备,并追踪了这一系统在动物界的演化历程。
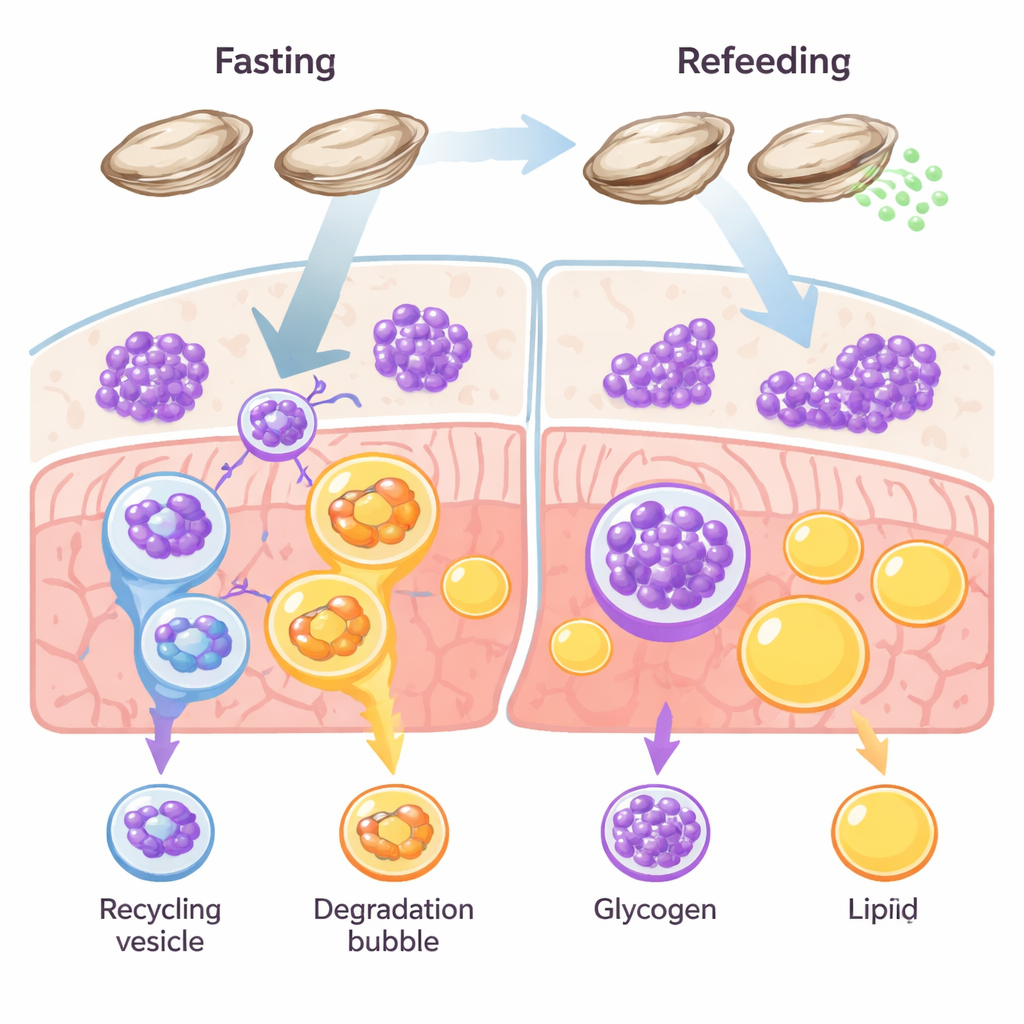
以糖为先的生存策略
大多数动物会在几种能量储备之间权衡,主要是脂肪和糖原。在鱼类和哺乳动物等脊椎动物中,脂肪通常作为长期储备占主导。牡蛎打破了这一规律。它们的组织充满糖原,早期研究表明,当食物匮乏或在生成配子时,这些贝类更多地消耗糖而非脂肪。作者着手检验糖原自噬——细胞内针对糖原的定向分解——是否在牡蛎禁食与恢复期间作为主要的生存通路发挥作用。
观察细胞如何从储存切换到消耗
研究团队将太平洋牡蛎禁食两周然后再喂养,随时间追踪它们组织的反应。禁食期间,显微染色显示自噬标记——细胞“清理”信号——在糖原储存处显著增加,同时糖原本身减少。相比之下,脂肪储备几乎没有变化。再次喂养后,糖原迅速恢复,自噬信号下降。与此同时,一种名为STBD1的关键受体蛋白(专门将糖原连接到自噬机械)水平与糖原使用同步升降。另一个与脂肪回收相关的受体p62则基本保持稳定。综合这些模式表明了一条专门的以糖为中心的回收通路:在牡蛎能量平衡中,糖原自噬而非脂肪分解的脂质自噬承担了主要作用。
抓住糖原的分子钩
糖原自噬依赖STBD1充当分子钩:它结合糖原并将其交给构建回收囊泡的小型适配蛋白。在牡蛎中,STBD1的连线方式与脊椎动物对应物不同。牡蛎蛋白将其结合糖原的区域——称为CBM20结构域——置于蛋白的前端(N端),而脊椎动物的STBD1则将该模块放在后端(C端),并包含一个额外的疏水尾巴用于锚定至细胞膜。计算机模型和模拟表明,牡蛎的N端布局使CBM20对分支糖链具有更强且更灵活的抓握能力。实验室实验支持了这一点:纯化的牡蛎STBD1比鱼或小鼠的STBD1与糖原结合更紧密,当将所有版本在人体细胞中表达时,牡蛎蛋白在诱导自噬期间导致糖原下降更明显。
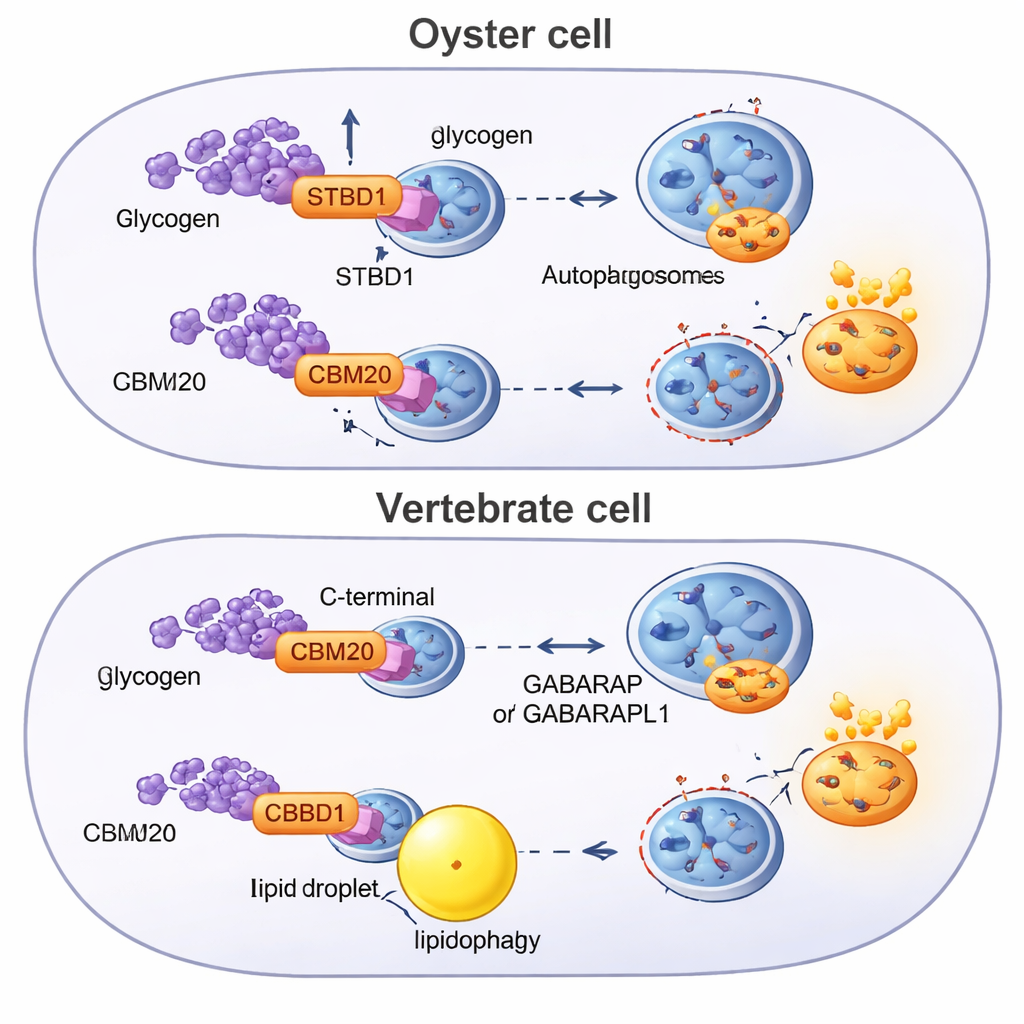
在动物中改造这一古老通路
为了解该系统的起源,研究者在数十种动物的基因组中搜索携带CBM20的蛋白并构建进化树。他们发现STBD1是一个双侧动物的发明——出现在具备左右对称体型动物的共同祖先中——但其结构在不同谱系中被重排。牡蛎和其他轮有类动物倾向于保持祖先型的N端CBM20设计,有时甚至复制该结合糖模块。包括脊椎动物在内的Chordata表现出一种不同版本,将CBM20移到了蛋白的尾部。这种重排与较弱的糖原结合相关联,并与一种更偏向脂肪分解的代谢策略相吻合,该策略依赖其他自噬受体和适配蛋白,而这些蛋白在牡蛎中缺乏。
这对生命的能量选择意味着什么
对非专业读者而言,结论是动物已经演化出不止一种方式来度过能量短缺期。牡蛎展示了一种古老的、以糖为中心的策略:高亲和力的STBD1版本能迅速抓住糖原并将其送入细胞回收单元,使糖原自噬在应激期间成为主要能量来源。相比之下,脊椎动物似乎在某种程度上放弃了这种强力的糖类抓握,转而采用更平衡或偏向脂肪的策略,由不同的蛋白伙伴和结构域布局支持。通过将详细的蛋白结构与整体有机体的燃料选择联系起来,这项研究说明了微小的分子“重连”如何帮助动物树的不同分支适应各自的环境和生活方式。
引用: Ren, L., Bai, Y., Shi, C. et al. Glycophagy is an ancient bilaterian pathway supporting metabolic adaptation through STBD1 structural evolution. Commun Biol 9, 268 (2026). https://doi.org/10.1038/s42003-026-09546-6
关键词: 糖原自噬, 糖原代谢, 牡蛎生物学, 自噬, 代谢的演化