Clear Sky Science · zh
由SDHB突变驱动的转移性嗜铬细胞瘤和副神经节瘤的表观遗传与代谢重编程
这些罕见肿瘤为何重要
嗜铬细胞瘤和副神经节瘤是由分泌激素的神经样细胞生长而来的罕见肿瘤,常见于肾上腺附近。大多数为生长缓慢的良性肿瘤,可通过手术治愈,但约五分之一最终会转移到其他器官,变得危及生命。本研究提出了一个简单却关键的问题:是什么让其中一些肿瘤变得具有侵袭性?通过深入研究这些癌症如何开关基因以及它们如何获取能量,研究者发现了一个潜在的弱点,未来可能成为新的治疗靶点。
从静默生长到致命转移
研究团队聚焦于携带SDHB基因改变的肿瘤。SDHB在细胞线粒体——细胞的动力工厂——中参与柠檬酸循环的部分过程。当SDHB受损时,琥珀酸(succinate)积累,细胞会表现出类似低氧的反应,即便实际并非缺氧。研究者分析了34名患者的组织,比较了局限性肿瘤与已发生转移的肿瘤。通过高分辨率的DNA“甲基化”图谱——显示化学标签如何调节基因表达——他们发现转移性肿瘤相比良性肿瘤具有更强的基因沉默模式,尤其是在存在SDHB突变时。
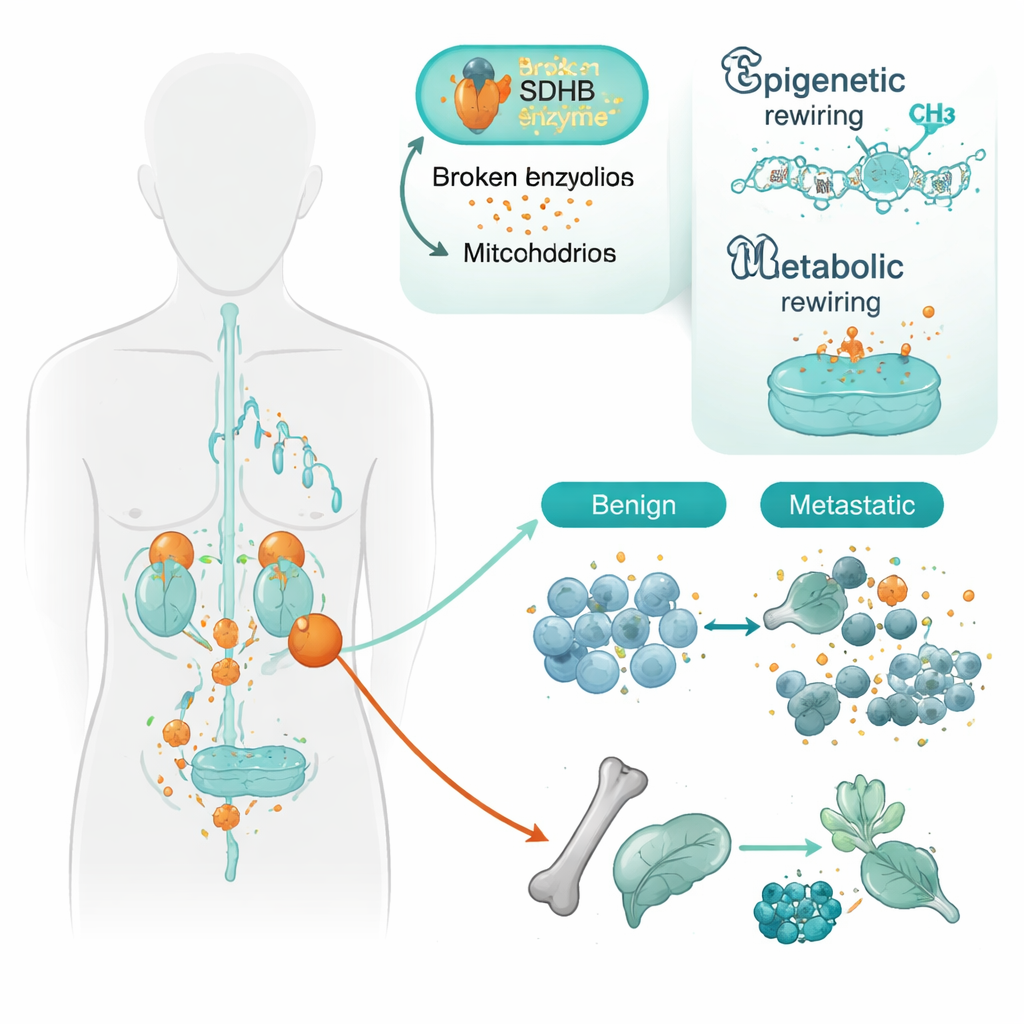
细胞身份的重编程
在侵袭性肿瘤中被关闭的许多基因,都是帮助神经样细胞成熟并维持其特化身份的基因。这包括指导细胞黏附、染色质组织以及细胞命运决定的一系列基因家族。一个突出例子是名为PCDHGC3的细胞黏附基因。即使在未转移但带有SDHB突变的肿瘤中,该基因的控制区已经部分沉默;在转移性肿瘤中,这种沉默更加明显。另一个负责组织大片段DNA的基因SATB2则仅在转移性肿瘤中被沉默,与SDHB状态无关。总体而言,这些模式提示SDHB丢失会“预置”细胞进入更不成熟、更易移动的状态,随后额外的表观遗传变化帮助它们脱离原位并发生转移。
肿瘤“吃糖”方式的重接线
出人意料的是,并非所有变化都表现为基因关闭。一小部分基因甲基化减少、表达增强,这些基因与将糖类转运入细胞密切相关。其中果糖转运基因SLC2A5尤为突出。其产物GLUT5负责将果糖——一种常见于水果和许多加工食品的糖——运入细胞。在缺氧的肿瘤样细胞模型中,SLC2A5持续被激活,而其他糖转运蛋白的反应则不那么一致。作者随后建立了来自患者PPGL肿瘤的细胞培养,并证明在葡萄糖匮乏时,补充果糖有助于这些细胞继续分裂,尤其在模拟肿瘤微环境的低氧条件下更为明显。
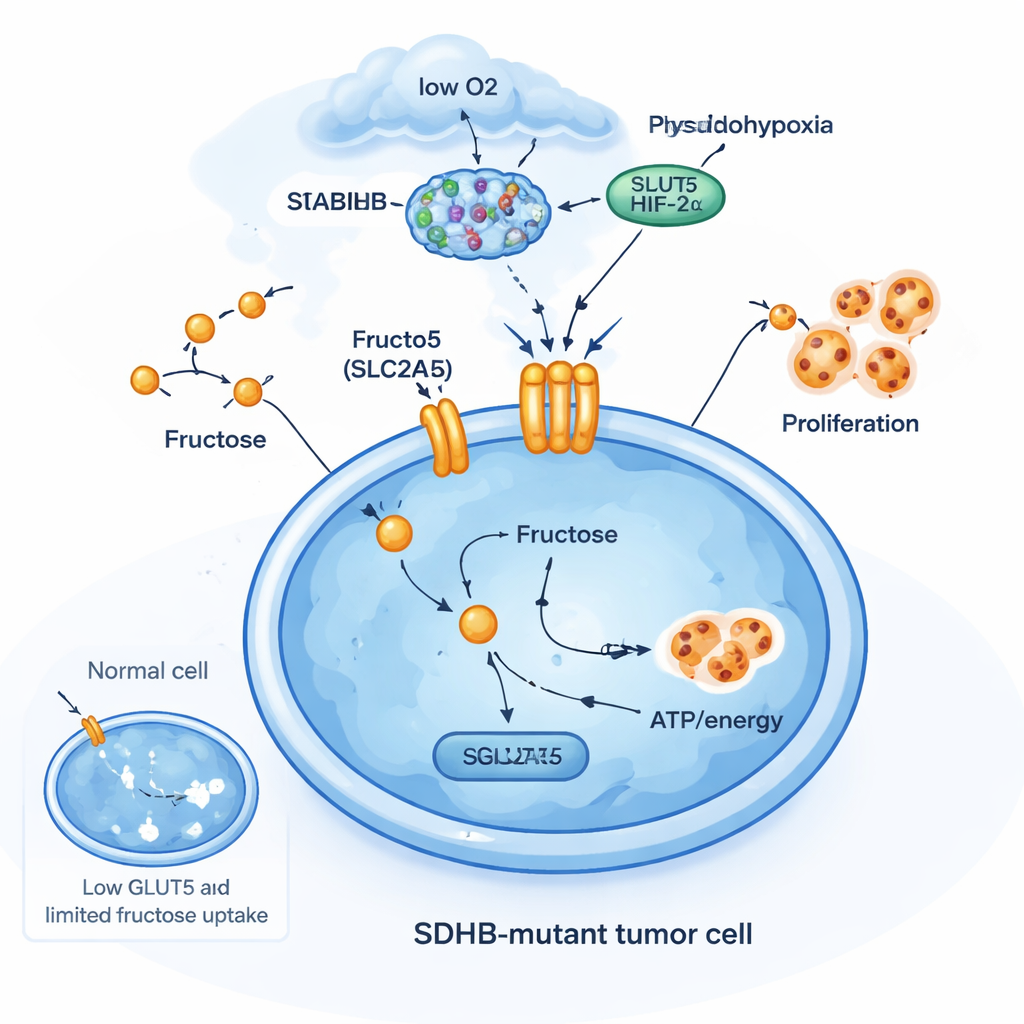
一种以果糖为动力的生存技巧
为弄清SDHB突变在此处的作用,团队在多种细胞类型中敲除SDHB。在来自肾上腺的类嗜铬细胞以及一个具有持续激活氧感受因子HIF2α的肾癌细胞系中,SDHB缺失提升了SLC2A5的水平。但在缺乏这些神经内分泌特征或HIF2α特征的更常见癌细胞系中,相同的SDHB敲除并未激活SLC2A5。这表明果糖转运器并非一种普遍的应激反应产物;它是在某些已经处于“拟低氧”状态的细胞类型中特异性适应的结果。在这些细胞中,SDHB丢失、琥珀酸积累与HIF2α活性协同,打开了一扇新的代谢之门:在氧气和葡萄糖受限时通过摄取果糖维持生长。
这对患者意味着什么
简而言之,该研究揭示了SDHB突变转移性PPGL的双重转变。首先,它们的DNA调控系统被重编程,使细胞变得不那么特化、更加可塑,从而更易侵袭;其次,它们的能量系统被重接线,在恶劣的低氧低糖微环境中转向利用果糖作为替代燃料。通过确定果糖转运蛋白SLC2A5/GLUT5在这一过程中的关键作用,这项工作指出了一个可能的阿基里斯之踵:阻断果糖摄取或代谢或能选择性地饿死这些肿瘤,同时对大多数正常组织影响较小。尽管此类疗法尚不可用,但绘制这幅表观遗传与代谢图谱是迈向针对高危SDHB突变PPGL开展更精确、以代谢为导向治疗的重要一步。
引用: Cubiella, T., Alba-Linares, J.J., San-Juan-Guardado, J. et al. Epigenetic and metabolic rewiring in metastatic pheochromocytomas and paragangliomas driven by SDHB mutations. Commun Biol 9, 266 (2026). https://doi.org/10.1038/s42003-026-09543-9
关键词: 嗜铬细胞瘤, 副神经节瘤, SDHB 突变, 表观遗传学, 果糖代谢