Clear Sky Science · zh
靶向PAK4通过NLRP1/胱天蛋白酶-3/GSDME轴促进吉西他滨诱导的胰腺癌细胞焦亡
为何用“燃烧式”方式杀死癌细胞可能重要
胰腺癌是最致命的癌症之一,即便是我们最有效的化疗药物,随着肿瘤产生耐药也常会失效。本研究探讨了一个令人意外的转折:相同的药物吉西他滨在关键分子“刹车”PAK4被关闭时,能以一种更剧烈、带炎症反应的方式——焦亡——杀死癌细胞。理解并靶向这一刹车,有望让现有治疗对更多患者更有效。
一种顽固且对治疗不敏感的癌症
胰腺导管腺癌通常诊断较晚且对治疗反应差,因此尽管有局限,吉西他滨仍是核心药物。吉西他滨通常通过凋亡来杀死细胞,凋亡是一种整齐、沉默的程序性细胞死亡。但在本研究中,超过一半被检验的胰腺肿瘤表达高水平的GSDME蛋白,而GSDME能将这种“安静”的死亡转为焦亡——一种迅速的“爆裂”式细胞死亡,会破坏细胞膜并释放炎性信号。这就提出了一个关键问题:如果肿瘤能经历焦亡,为什么仍有那么多对吉西他滨耐药?
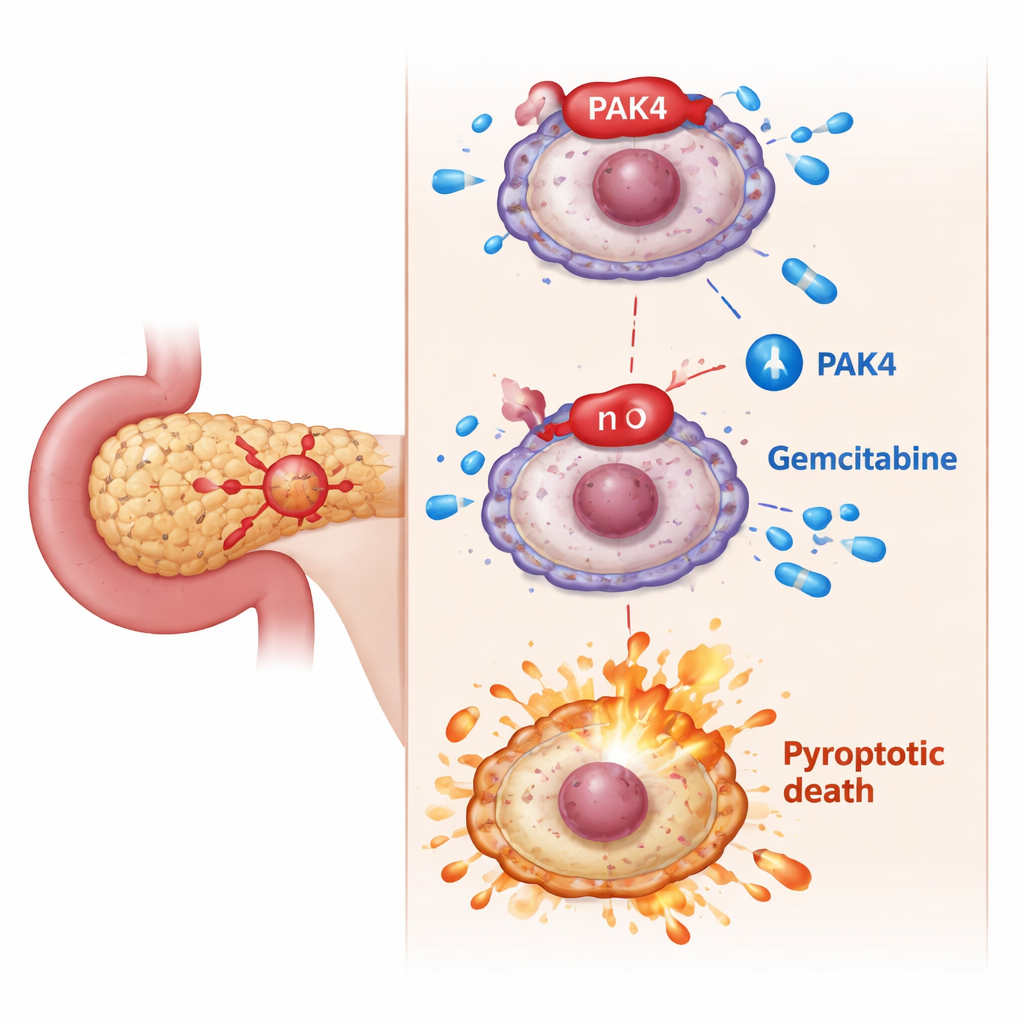
隐藏的刹车:PAK4阻断燃烧式细胞死亡
研究者将注意力集中到PAK4上,这是一种在胰腺癌中过度活跃并与吉西他滨疗效差相关的促生长蛋白。在细胞实验中,PAK4水平高的癌细胞更难被吉西他滨杀死。当团队降低PAK4时,吉西他滨的致死性骤然增强:细胞表现出典型的焦亡特征——肿胀、气泡样突出、膜破裂以及胞内物质更多释放。在分子水平上,这一转变依赖于GSDME被另一种蛋白质胱天蛋白酶-3切割成活性片段。阻断胱天蛋白酶-3会阻止GSDME触发焦亡,证实PAK4通常起到抑制该死亡通路的作用。
PAK4如何拆解细胞的死亡报警系统
进一步研究表明,PAK4并不直接作用于GSDME,而是破坏上游的“报警传感器”NLRP1。在患者样本中,较高的NLRP1水平与更好的生存相关,表明它有助于抑制肿瘤。在癌细胞中,去除NLRP1后,吉西他滨诱导的细胞死亡和GSDME活化明显下降,显示NLRP1参与了焦亡机械。肿瘤样本中PAK4与NLRP1呈负相关:PAK4高时NLRP1低。研究显示,活性PAK4通过另一个蛋白——E3连接酶Mdm2——将NLRP1标记为降解目标,由细胞的废弃处理系统清除。通过如此标记NLRP1,PAK4阻止了通过胱天蛋白酶-9和胱天蛋白酶-3的级联反应,这条反应链本应最终以GSDME介导的焦亡为终点。
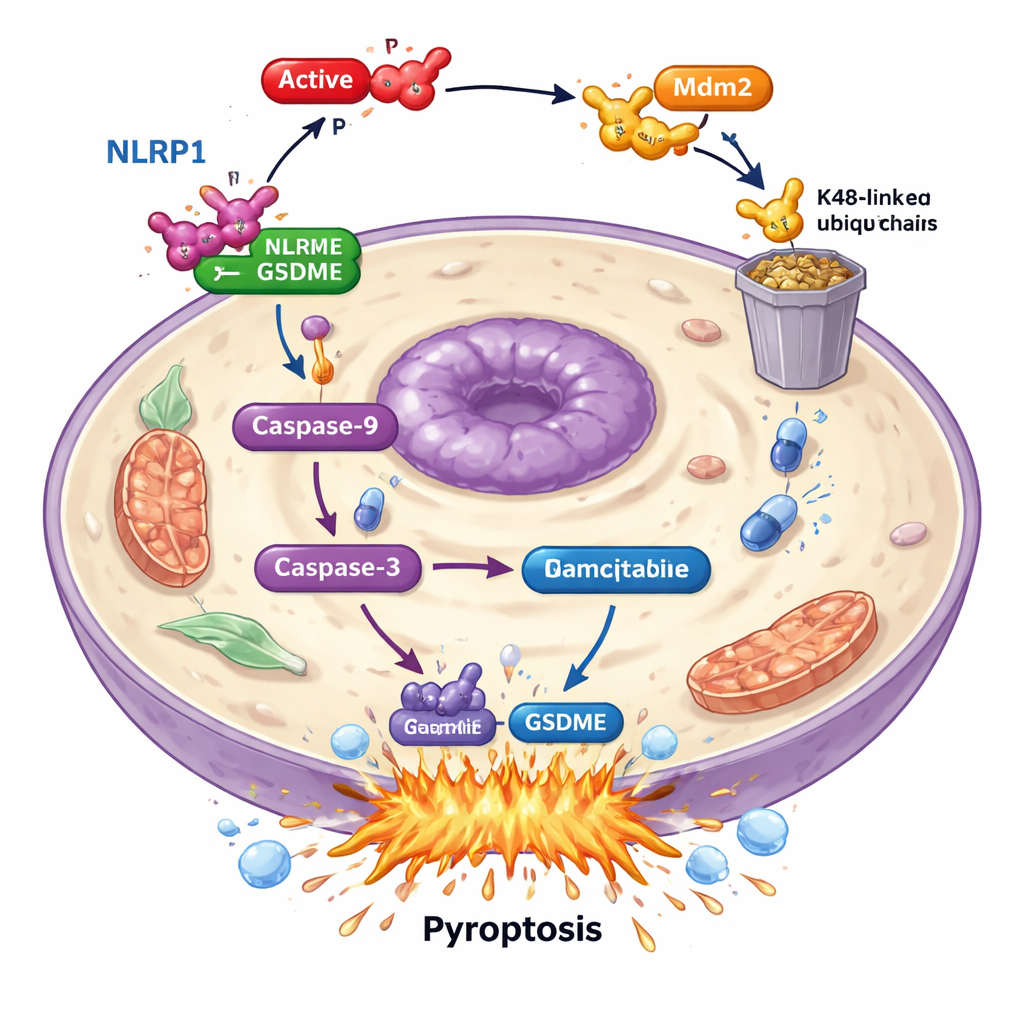
关闭PAK4以增强化疗效果
鉴于PAK4对焦亡起抑制作用,团队测试了阻断其活性是否能重新唤醒吉西他滨的杀伤力。他们使用了一种名为PF-3758309的小分子PAK4抑制剂。单独使用该抑制剂就能促使胰腺癌细胞倾向焦亡,增加胱天蛋白酶-3活化、GSDME切割和细胞膜破裂。与吉西他滨联合使用时,效果更为显著:更多细胞通过焦亡死亡,且死亡通路的分子标志被放大。在携带人类胰腺肿瘤的小鼠模型中,降低PAK4或使用PAK4抑制剂都使吉西他滨更有效地缩小肿瘤,并在肿瘤内增强了焦亡标志物。
对患者和未来治疗的意义
简而言之,这项工作揭示了一个分子“锁”——PAK4,它阻止胰腺癌细胞在化疗下以一种尤其破坏性的方式死亡。通过禁用PAK4,医生可能将接受吉西他滨治疗的肿瘤推向焦亡,使药物更有效并可能激活免疫系统对抗癌症。尽管还需要在患者来源模型和临床试验中做更多工作,但该研究提供了一条清晰的路线:靶向PAK4–Mdm2–NLRP1–GSDME通路,利用现有药物通过更智能的组合将耐药肿瘤转变为敏感肿瘤。
引用: Lu, T., Song, Y., Liang, K. et al. Targeting PAK4 promotes Gemcitabine-induced pyroptosis in pancreatic cancer via NLRP1/caspase-3/GSDME axis. Commun Biol 9, 260 (2026). https://doi.org/10.1038/s42003-026-09538-6
关键词: 胰腺癌, 吉西他滨耐药, 焦亡, PAK4, 靶向治疗