Clear Sky Science · zh
来自多种谱系的胎儿样逆转维持肠道干细胞库并赋予应激耐受性
肠道在压力下如何自我修复
肠道上皮是体内最繁忙的组织之一。它负责消化食物、吸收营养并抵御病原体,同时每隔几天就完成一次自我更新。本文探讨了这一脆弱表面如何在炎症或化疗等严重冲击下存活:通过短暂地将细胞回拨到更像胎儿的、可塑性更高的状态,帮助肠道修复并抵御损伤。
肠道中的日常生产线
在健康状态下,一类称为隐窝基柱状细胞(CBCs)的特殊细胞位于称为隐窝的小凹底部。这些类干细胞不断分裂,将子代推向突入肠腔的指状绒毛。在迁移过程中,细胞分化为不同角色,例如负责吸收营养的吸收性肠细胞,或产生粘液和抗菌物质的分泌性细胞。在正常情况下,这种自下而上的流动维持了肠道上皮的更新和有序性。
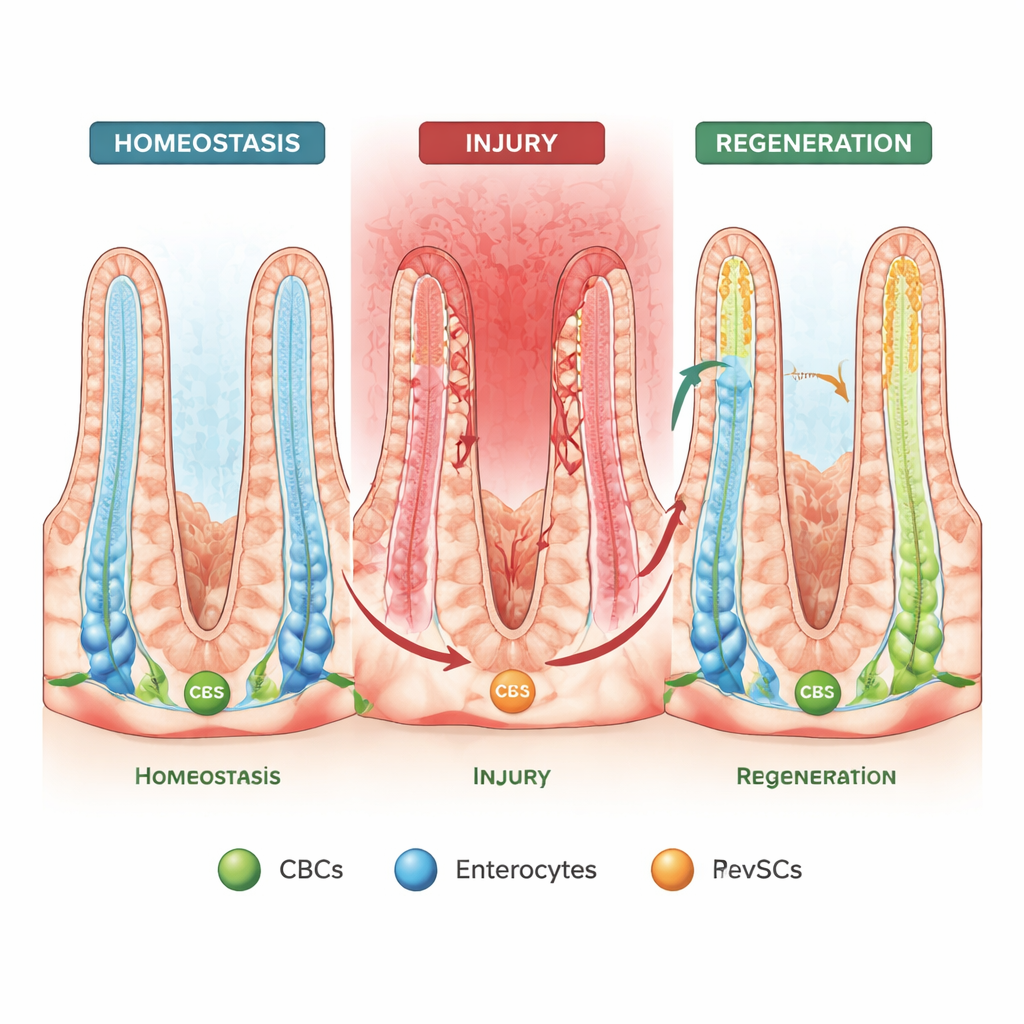
能够把生产线倒转的细胞
当肠道上皮受损且CBCs丧失时,早期研究表明一些成熟细胞可以“走回去”到隐窝,重新获得类干能力,这种行为称为空间可塑性。另一种较新的现象是“胎儿样逆转”,即细胞采用类似发育中肠道的基因表达程序。在这项研究中,作者使用复杂的类器官(迷你肠)培养、单细胞RNA测序和小鼠谱系追踪,将这两种想法联系起来。他们鉴定出一种特殊的胎儿样群体,称为复苏干细胞(revSCs),可以由CBCs和普通吸收性肠细胞两者产生,然后再生出完整的肠道细胞谱系。
迷你肠揭示隐藏的可塑性
为了观察这些变化,团队在两种不同的基质中培养小鼠和人类肠类器官。在Matrigel中,类器官表现得如同正常成年组织,富含CBCs和成熟细胞类型。然而在胶原基质中,类器官被具有胎儿基因特征的revSC样细胞主导。单细胞分析显示,revSCs可沿两条主要路径追溯:来自经典CBCs和来自吸收性肠细胞。分选实验证实CBCs具有最高的转化为revSCs的能力,但即便更成熟的细胞在合适的环境下也能发生转化。关键是,纯化的revSCs可被移回Matrigel,并重新生成CBCs和所有主要肠道谱系,证明胎儿样状态既可逆又功能完整。
绒毛细胞与真实伤害情境
研究进一步探问这种可塑性是否在体外以外也出现。研究者在小鼠绒毛中标记了肠吸收细胞,然后将绒毛碎片培养,或将动物暴露于致肠损伤的化疗药物5-氟尿嘧啶(5-FU)。在胶原中,通常被认为缺乏干细胞的绒毛碎片形成了新的类器官,表现出revSC特征,随后在转回标准条件时重新获得CBC标记。当移植到结肠炎模型中时,这些“绒毛来源”类器官重建了健康的肠上皮。在接受5-FU处理的活体小鼠中,被标记的吸收性肠细胞开始表达revSC标记,随后以包含隐窝基部新CBCs的长条克隆条带重新出现,证实了成熟细胞介入并补充了干细胞库。
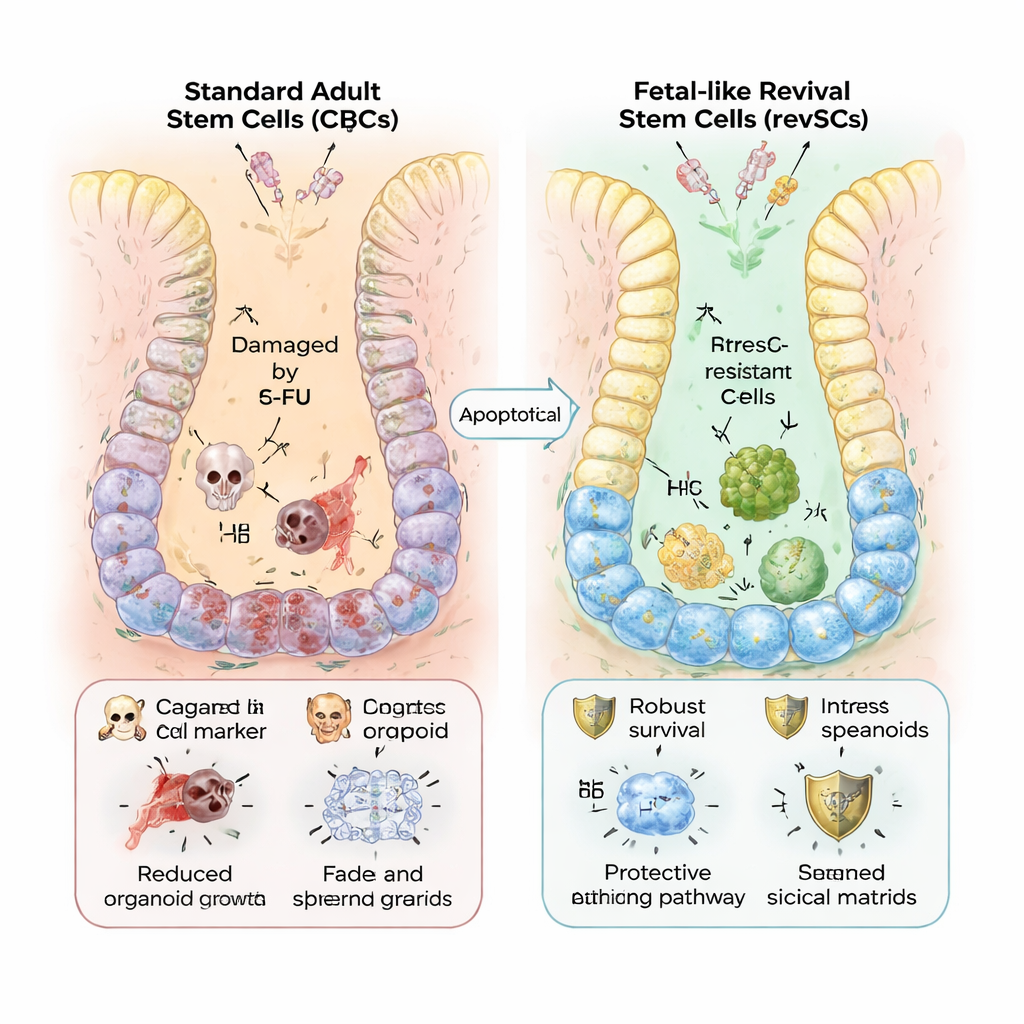
耐压的修复小分队
为什么要走这条胎儿样的迂回路?作者表明revSCs在抵抗应激方面远优于常态细胞。当类器官受到5-FU冲击时,置于标准Matrigel中的类器官缩小并显示出与DNA损伤和狂热增殖相关的广泛基因程序。相比之下,富含revSCs的胶原培养类器官继续生长,并表现出更为冷静、目标明确的应答。基因分析显示抗氧化系统、抗凋亡蛋白和热休克伴侣等分子的活性更高——这些分子盾帮助细胞在炎症和毒性损伤中存活。类似模式在小鼠和人类细胞中均有观察,并且这些revSC相关基因在人类炎症性肠道中也呈上调。
这对肠病与治疗意味着什么
对非专业读者而言,结论是肠道上皮有一套内置的紧急应对方案。当炎症或药物威胁其常态干细胞时,干细胞和普通吸收细胞都能暂时逆转为一种胎儿样、耐压的revSC状态。从那里,它们可以重建正常的干细胞区并修复组织。这项工作将两种再生概念——空间可塑性与胎儿样逆转——统一为单一的修复层级,并提示有望通过谨慎利用这一可塑、胎儿样程序改善炎症性肠病和结直肠癌等疾病的治疗;同时也警示,若对逆转调控不当,可能助长肿瘤生长。
引用: Kirino, S., Uefune, F., Miyake, K. et al. Fetal reversion from diverse lineages sustains the intestinal stem cell pool and confers stress resilience. Commun Biol 9, 255 (2026). https://doi.org/10.1038/s42003-026-09533-x
关键词: 肠道干细胞, 组织再生, 细胞可塑性, 炎症性肠病, 类器官