Clear Sky Science · zh
氟伐他汀通过靶向CYP4Z1抑制乳腺癌的起始与进展
为什么一种降胆固醇药物与乳腺癌相关
许多接受乳腺癌治疗的女性会出现异常血脂水平,并面临疾病复发或转移的持续威胁。这项研究探讨了一个引人注目的想法:一种常见的降胆固醇药物氟伐他汀,能否被重新用于减缓或预防乳腺癌——通过解除一种驱动特别危险、类干细胞肿瘤细胞的蛋白的活性?
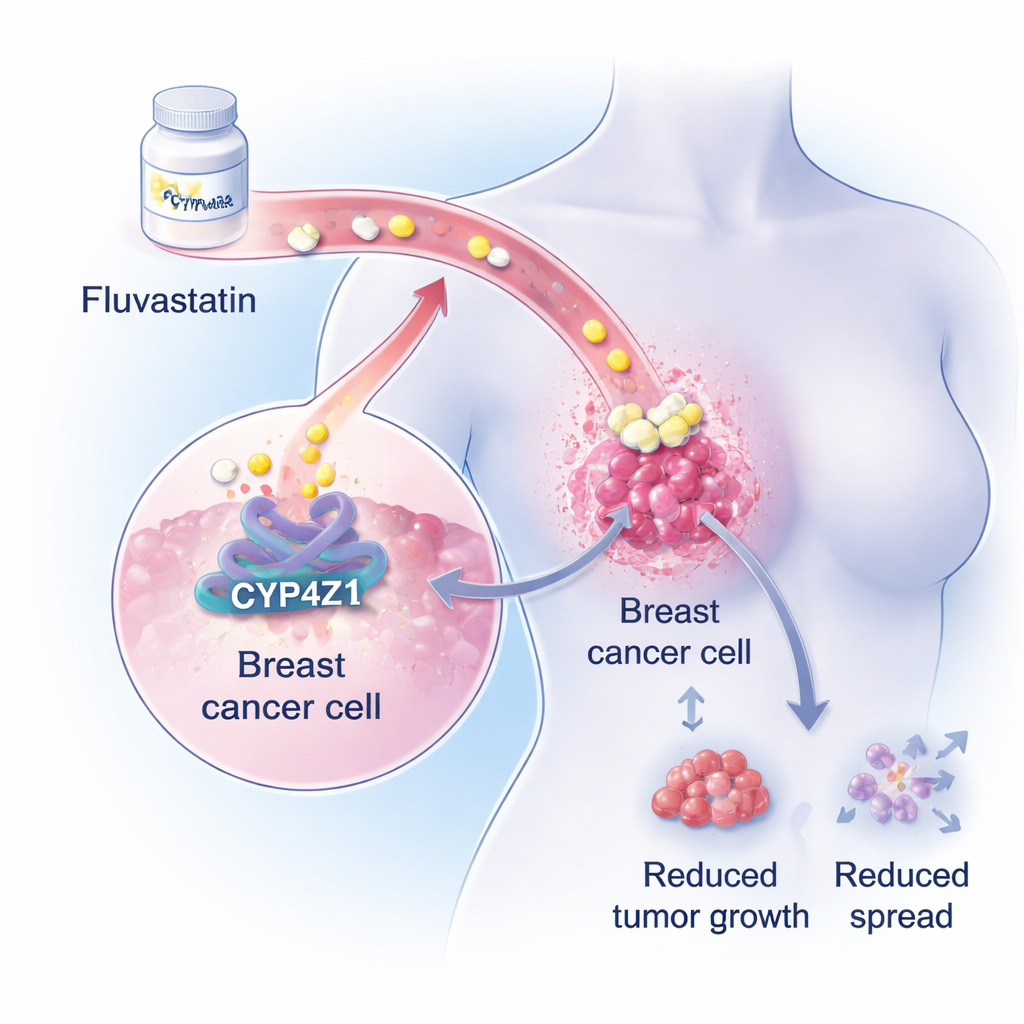
乳腺肿瘤内的隐秘驱动因子
研究人员聚焦于一种鲜为人知的蛋白CYP4Z1,在乳腺癌细胞中高表达而在健康乳腺组织中不显著。早期工作显示CYP4Z1有助于让癌细胞表现出更多类干细胞特性——这些细胞能够无限自我更新、耐受化疗,并在治疗后重启肿瘤。在大规模的基因组和生化分析中,研究团队现在显示,过度活跃的CYP4Z1强烈促进乳腺癌细胞内的脂质合成通路,尤其是三酸甘油酯的生成,三酸甘油酯是主要的储脂形式。由于许多乳腺癌患者在化疗期间已经出现血脂紊乱,CYP4Z1的这一促脂作用暗示了使用现有降脂药的可能切入点。
将氟伐他汀从心血管用途重新用于癌症治疗
为检验这一想法,科学家筛选了一个包含23种经FDA批准的降脂药的小型药物库。氟伐他汀——一种广泛用于高胆固醇的他汀类药物——脱颖而出:它以剂量依赖的方式直接抑制CYP4Z1的酶活性。在对正常乳腺细胞相比对癌细胞毒性较小的剂量下,氟伐他汀显著降低了关键的干性标志物,抑制了乳腺癌细胞形成悬浮“肿瘤球”的能力,并减少了它们在体外实验中穿越类组织屏障的迁移和侵袭能力。它还使肿瘤细胞对化疗药物阿霉素更为敏感,提示可增强现有治疗效果。
在活体动物中检验该药物
随后,团队在小鼠模型中评估了氟伐他汀的作用。在植入了人源乳腺癌细胞的小鼠中,间歇性氟伐他汀治疗延缓了肿瘤生长,降低了肿瘤中干性标志物(ALDH1A1)和细胞增殖标志Ki67的水平,并减少了出现在肺部的转移结节数量。重要的是,接受氟伐他汀的小鼠保持体重稳定,血液和骨髓未见明显异常,表明在所用剂量下具有良好的安全性。在更接近真实病理的遗传模型中——工程化小鼠会因致癌基因驱动而发生乳腺肿瘤——研究人员进一步在乳腺组织中引入了人的CYP4Z1基因。这些小鼠比对照动物出现更多癌前和癌性病变,以及更多肝脏和肺部转移。氟伐他汀治疗显著减少了乳腺病变和远处转移的数量,尤其是在携带额外CYP4Z1基因的小鼠中。
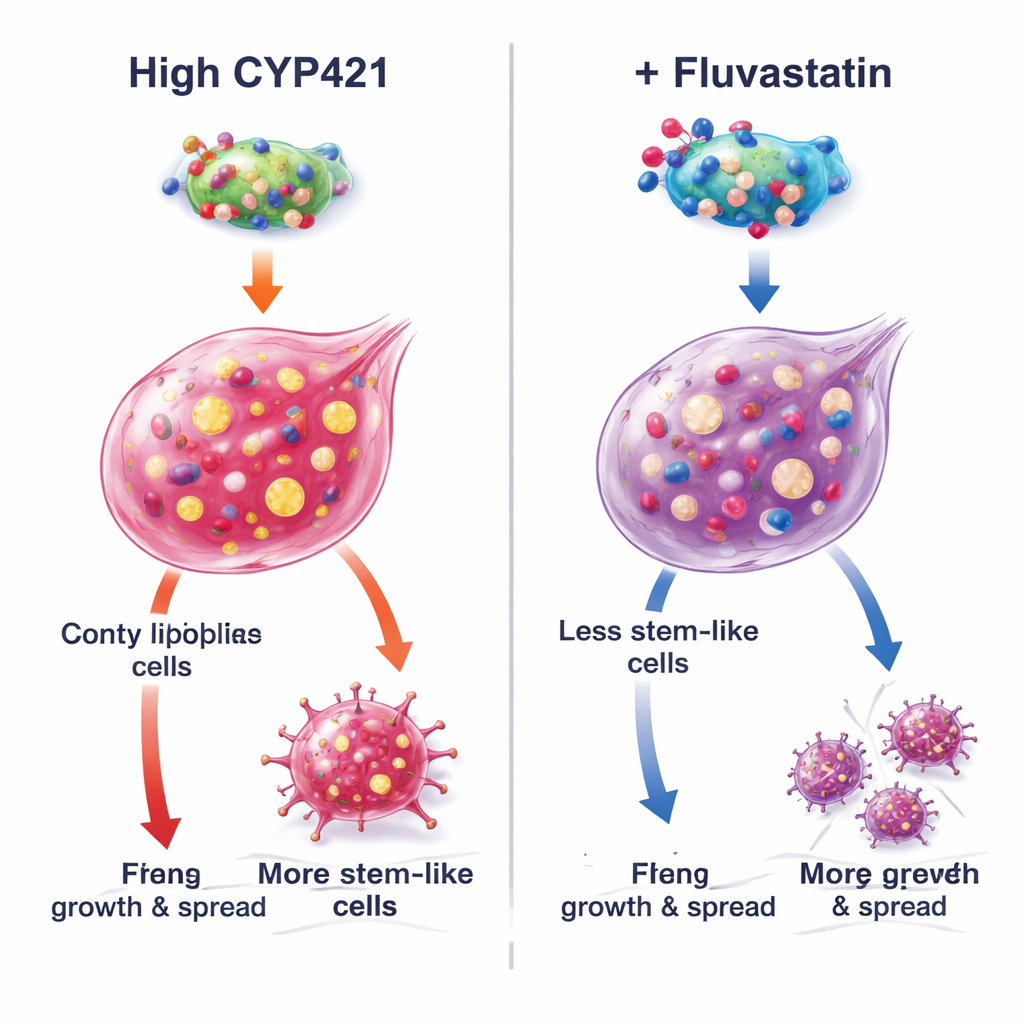
氟伐他汀如何解除一种促癌蛋白的作用
为揭示机制,作者结合了计算建模与精确的蛋白工程研究。他们预测氟伐他汀嵌入CYP4Z1的活性位点,与三个关键氨基酸(Lys109、Pro444 和 Arg450)相互作用。当这些位点被突变时,CYP4Z1的活性下降且氟伐他汀不再能进一步抑制它,证实这些位点为结合位点。在自然缺失CYP4Z1的细胞中加入正常蛋白会增强干性并激活促生长的PI3K/AKT信号通路,而氟伐他汀能逆转这些效应。突变体的CYP4Z1活力较弱且对药物的响应也降低。额外实验显示,当人为提高三酸甘油酯生成或敲低CYP4Z1时,氟伐他汀的作用减弱,这强调了该药物最强的效应来自于阻断这一特定蛋白及其促脂后果,而不是通过铁驱动的“铁死亡”诱导细胞死亡。
这对患者意味着什么
总体而言,研究表明氟伐他汀除了降低胆固醇外,还能在实验模型中通过靶向CYP4Z1抑制乳腺癌的早期发生及后期扩散。CYP4Z1是一种推动肿瘤脂质代谢和类干细胞行为的蛋白。由于氟伐他汀已获批准且安全性特征明确,这些发现为更快开展临床试验作为辅助治疗提供了有希望的路径,尤其针对肿瘤强烈表达CYP4Z1的患者。尽管仍需更多工作来在人群中验证该策略并识别该药物可能的其他靶点,这项研究为将一种熟悉的心血管药物纳入对抗侵袭性、易复发乳腺癌的新策略打开了大门。
引用: Li, H., Chen, Y., Shi, W. et al. Fluvastatin suppresses breast cancer initiation and progression via targeting CYP4Z1. Commun Biol 9, 254 (2026). https://doi.org/10.1038/s42003-026-09532-y
关键词: 乳腺癌, 氟伐他汀, 癌症干细胞, 脂质代谢, 药物再利用