Clear Sky Science · zh
利拉鲁肽通过调节oxLDL/LPA/LPAR1通路减轻氯化铝诱导的大鼠阿尔茨海默病样损伤
为什么一种糖尿病药物可能与记忆丧失相关
随着人们寿命延长,越来越多的家庭面临阿尔茨海默病带来的缓慢且毁灭性的记忆和人格丧失。同时,2型糖尿病与肥胖率上升,科学家注意到血糖代谢问题与痴呆之间存在令人意外的关联。本研究提出一个充满希望的问题:一种已用于治疗糖尿病的药物——利拉鲁肽,是否也能在一定程度上保护大脑免受类似阿尔茨海默病的损伤——至少在模拟该病关键特征的动物模型中是否有效?
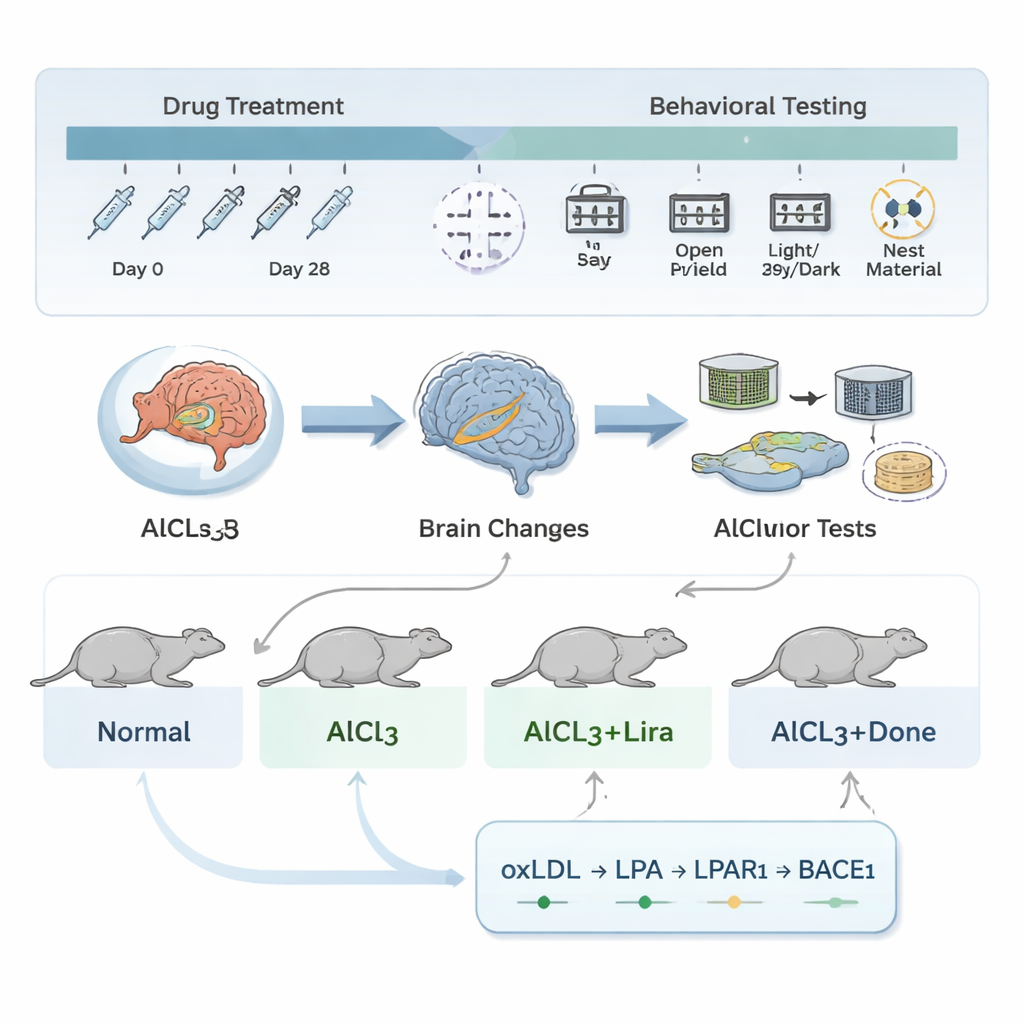
在实验室建立类阿尔茨海默状态
为探究这一问题,研究者使用雄性大鼠,并将它们分为四组:健康对照组、接受氯化铝(AlCl3)以诱发类阿尔茨海默变化的组,以及两组在接受AlCl3的同时分别给予利拉鲁肽或标准阿尔茨海默药物多奈哌齐的治疗组。已知铝暴露会在啮齿动物中引发与人类阿尔茨海默相似的大脑变化,包括记忆丧失、焦虑和有害蛋白质沉积。在45天内,大鼠每天接受铝注射,治疗组还同时接受指定药物。此后,动物接受了一系列行为测试,以评估焦虑、抑郁样表现以及不同类型的记忆,例如在水中找到隐藏平台的学习与记忆或识别新物体的能力。
行为、情绪与记忆的显微观察
仅暴露于铝的大鼠表现出更强的焦虑、更不愿探索光亮或开放空间,并在被迫游泳测试中表现出更多绝望样行为。它们识别新物体的能力以及在水迷宫中学习并记住隐藏平台位置的能力也明显受损。利拉鲁肽治疗改变了这种局面。与铝共同处理的利拉鲁肽组在开放空间中更勇敢,在光区停留时间更长,游泳测试中的静止时间更少。它们在记忆任务中的表现也显著改善,常常与或超越多奈哌齐组的改善。简言之,这种糖尿病药物并非仅缓解单一症状——在该模型中,它广泛改善了与情绪相关的行为以及多种学习和记忆形式。
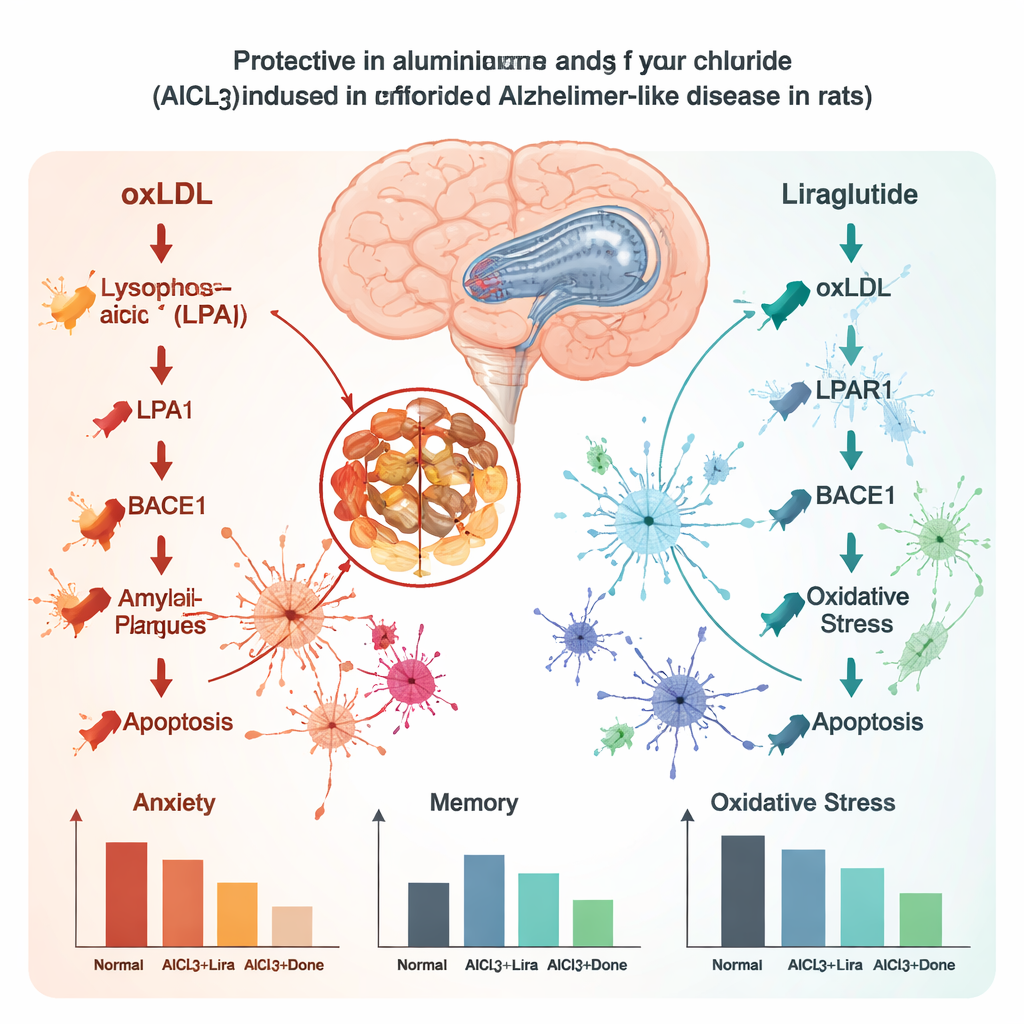
脑内发生了什么
当科学家检查大鼠大脑时,发现铝损伤了与认知和情绪相关的关键区域,如海马和前额叶皮层。健康神经细胞减少,越来越多细胞萎缩和死亡,并出现类似于人类阿尔茨海默病的淀粉样斑块和缠结的结构。铝还扰乱了大脑的化学平衡:天然抗氧化物耗竭,脂质损伤相关分子增加,分解记忆相关神经递质乙酰胆碱的酶活性过高。利拉鲁肽在很大程度上逆转了这些趋势。经治疗的大鼠脑结构保存更好,斑块和缠结样沉积减少,保护性抗氧化物水平更高,氧化损伤标志物降低,分解乙酰胆碱的酶活性也减少,这些效应与或优于多奈哌齐组。
在脑细胞中被突出的一条新型连锁反应
除了这些可见变化,研究团队还聚焦于一条在脑细胞内可能推动阿尔茨海默病理的特定事件链。这条通路涉及氧化的“有害”胆固醇(oxLDL)、一种脂类信使溶血磷脂酸(LPA)、其受体LPAR1,以及一种名为BACE1的酶,该酶参与生成淀粉样蛋白。铝暴露使海马中这些组成成分及其下游信号上调,同时伴随细胞自杀信号的增加(BAX上升、保护性BCL-2下降)以及淀粉样前体蛋白和Tau水平升高——这些都是斑块和缠结的原料。利拉鲁肽抑制了这一整条级联反应:oxLDL、LPA、LPAR1和BACE1水平下降,促死亡信号减少,淀粉样和Tau阳性细胞负担降低。这些结果表明,利拉鲁肽的脑部益处不仅是表面现象,而是与驱动阿尔茨海默样损伤的分子机制发生了更深层次的变化有关。
这对未来治疗可能意味着什么
对非专业读者来说,结论是:一种最初用于控制血糖和体重的药物,可能也能保护大脑免受类似阿尔茨海默病的变化——至少在暴露于强烈化学诱因的大鼠身上是如此。利拉鲁肽改善了行为,保护了脑组织,并抑制了与淀粉样蛋白沉积相关的有害脂质与胆固醇通路。尽管动物研究不能保证在人体中同样成功,但这些发现支持了将某些糖尿病药物重新用途于减缓或预防痴呆的可能性。如果未来在更逼真的模型和临床试验中证实这些效应,患者或许有朝一日能从一种医生和监管机构已熟悉的具有脑保护潜力的治疗中受益。
引用: Abo El-Magd, N.F., Ramadan, N.M. & Eraky, S.M. Liraglutide attenuates aluminum chloride-induced Alzheimer’s disease in rats by modulating the oxLDL/LPA/LPAR1 pathway. Commun Biol 9, 262 (2026). https://doi.org/10.1038/s42003-026-09531-z
关键词: 阿尔茨海默病, 利拉鲁肽, 2型糖尿病, 胆固醇与大脑健康, 神经保护