Clear Sky Science · zh
阿尔茨海默病患者颞叶皮层中差异表达的miRNA及其与tau病理的关联
为何这些微小的大脑开关至关重要
阿尔茨海默病会逐渐剥夺人的记忆和独立生活能力,但我们仍缺乏能阻止或逆转病程的疗法。本研究关注大脑中一些极小的控制开关——称为微小RNA的短RNA分子,它们帮助决定细胞合成哪些蛋白质。通过检查阿尔茨海默病患者的脑组织,研究者探讨了这些微小RNA的改变是否与疾病的关键特征相关:即异常tau蛋白在细胞内的积聚和传播。
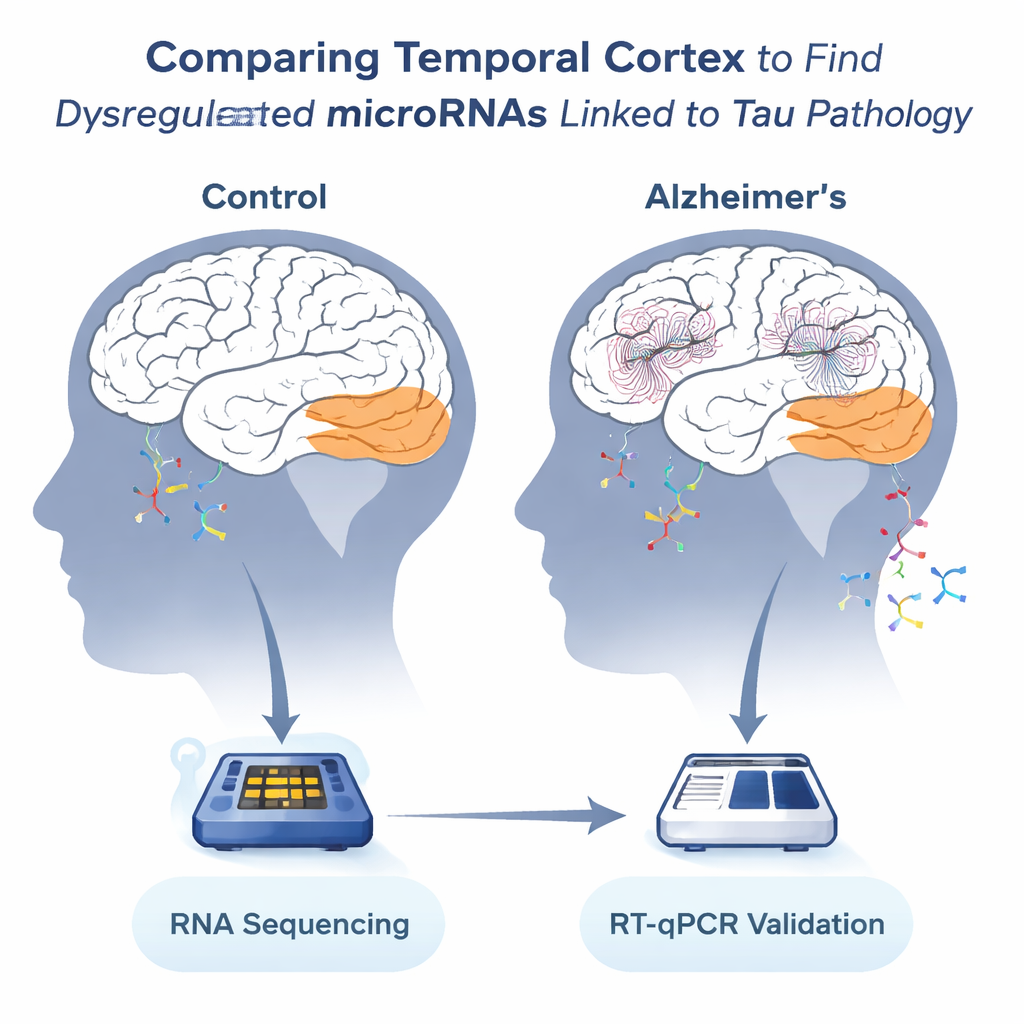
在易受损的大脑区域中查看信息
研究团队聚焦于颞叶皮层——一个与语言和记忆密切相关且在阿尔茨海默病中受影响严重的区域。尸检后,从两个欧洲脑库收集了36名个体的样本——13名无阿尔茨海默病者和23名患病者。科学家从这些组织中提取RNA,并使用高通量测序计数数百种不同的微小RNA。由于脑组织在死后会降解,他们仔细检查了RNA质量,并挑选出19个完整性可接受的样本用于最详细的分析,然后用全部36个样本来验证主要发现。
发现阿尔茨海默病的微小RNA特征
在检测到的449种微小RNA中,有13种在阿尔茨海默病颞叶皮层中表现出持续的改变。与对照脑相比,8种下调,5种上调。其中若干最强的信号涉及先前就被怀疑与阿尔茨海默病相关的微小RNA:miR-129-5p、miR-132-3p和miR-146b-5p水平均降低,而miR-151a-5p则升高。这些分子在大脑中含量丰富,已知参与调节与神经元健康相关的基因网络。作者使用第二种、更有针对性的技术(RT-qPCR)验证了这些相同的微小RNA在相同方向上的变化,即便纳入了质量较低的样本,也增强了这一模式为真实现象的可信度。
将微小开关与恶化的tau缠结联系起来
大脑中阿尔茨海默病的严重程度通常用Braak分期来分级,该分期反映tau缠结在不同区域的扩散程度。研究者发现,miR-129-5p、miR-132-3p和miR-146b-5p的水平随着Braak分期的升高而稳步下降,而miR-151a-5p则有上升趋势。他们还在相同样本中直接测量了一种高度磷酸化、易形成缠结的tau形式。含有更多异常tau的脑样本显示出相同的模式:miR-129-5p、miR-132-3p和miR-146b-5p减少,miR-151a-5p增加。换言之,微小RNA的变化与显微分期和tau病理的生化指标一致,表明这些变化与病程密切相关,而非偶然的伴随现象。
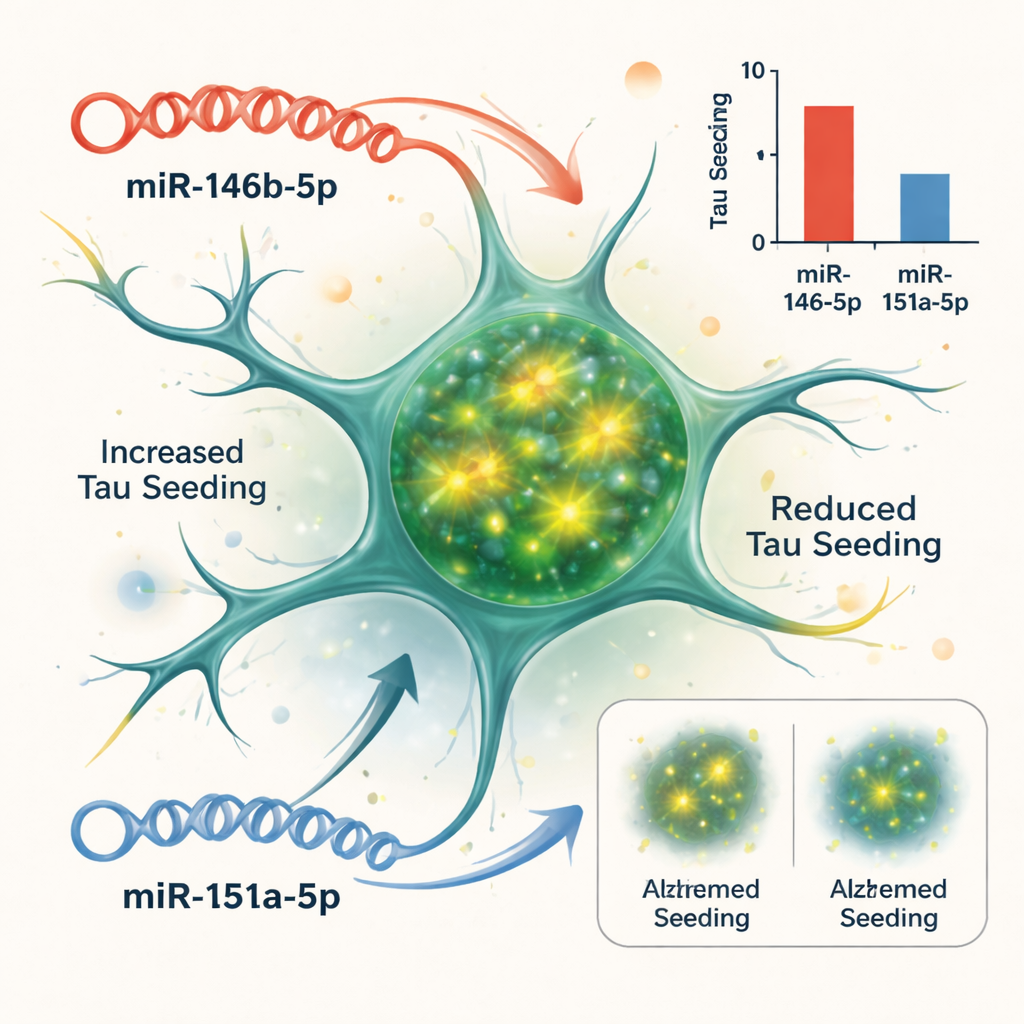
在细胞模型中检验因果关系
相关性并不能证明微小RNA驱动疾病,因此团队转向一种基于细胞的系统来报告tau聚集如何“种子”新团块的能力。他们使用了经过工程改造的生物传感细胞,这些细胞在细胞内形成tau纤维时会发光。当他们加入来自阿尔茨海默病大脑的富含tau的物质时,细胞产生了强烈的荧光信号。通过在这些细胞中增强或抑制特定微小RNA,科学家可以观察哪些microRNA会改变tau的种子性。其中两个最显著:增加miR-146b-5p会使tau种子性恶化,而抑制它则降低种子性;相反,增加miR-151a-5p会抑制tau种子性,而抑制miR-151a-5p会使种子性增强。其他被测试的微小RNA在该测定中影响不大。
这对未来诊断和治疗可能意味着什么
为理解这些微小RNA可能的作用,作者使用计算工具将其预测的基因靶点映射到已知的生物通路上。下调的微小RNA——尤其是miR-129-5p、miR-132-3p和miR-146b-5p——与参与神经元存活、突触化学信号传递以及与阿尔茨海默病相关通路的网络有关。这提示它们正常的“制动”作用丧失可能会同时破坏多重保护系统,而miR-151a-5p的上升可能代表大脑在晚期对抗tau聚集的一种部分补偿尝试。尽管这项工作依赖于死后组织和简化的细胞模型,但它加强了特定微小RNA既反映又调节tau病理的观点。从长远看,测量脑脊液或血液中的这些分子可能有助于追踪疾病进展,而在大脑中精确地调整它们的水平或许为减缓或阻止有毒tau扩散提供新的途径。
引用: Nagaraj, S., Quintanilla-Sánchez, C., Ando, K. et al. Differentially expressed miRNAs in the temporal cortex of Alzheimer’s disease patients and their association to tau pathology. Commun Biol 9, 253 (2026). https://doi.org/10.1038/s42003-026-09530-0
关键词: 阿尔茨海默病, 微小RNA, tau病理, 颞叶皮层, 神经退行性变