Clear Sky Science · zh
针对性阻断基因剪接可扰乱嵌入内含子的初级微小RNA
基因中的隐秘信息
许多新型基因疗法通过调控细胞的RNA信息发挥作用,但这些RNA常常隐藏着额外的“边注”,科学家们才开始理解它们的含义。本文表明,旨在纠正基因错误剪接的药物可能意外提升埋藏在内含子——基因编码片段之间非编码区段——中的微小调控RNA,从而对脑连接和发育产生出乎意料的影响。
改写RNA的基因疗法
反义寡核苷酸(ASO)是能结合RNA并改变其读取或处理方式的短合成核酸片段。已有若干ASO用于或正在用于针对罕见遗传病的临床试验,尤其是那些由RNA剪接缺陷引起的疾病。大多数安全性测试侧重于ASO是否恢复了正确的蛋白质并避免明显的副作用。但许多基因也携带非编码RNA,包括嵌入内含子的微小RNA。这些微小分子能强烈调节基因活性,脊椎动物中高达一半已知的微小RNA来源于内含子。本研究提出的问题是:当我们用ASO强制改变剪接时,被嵌入的这些微小RNA会发生什么变化?
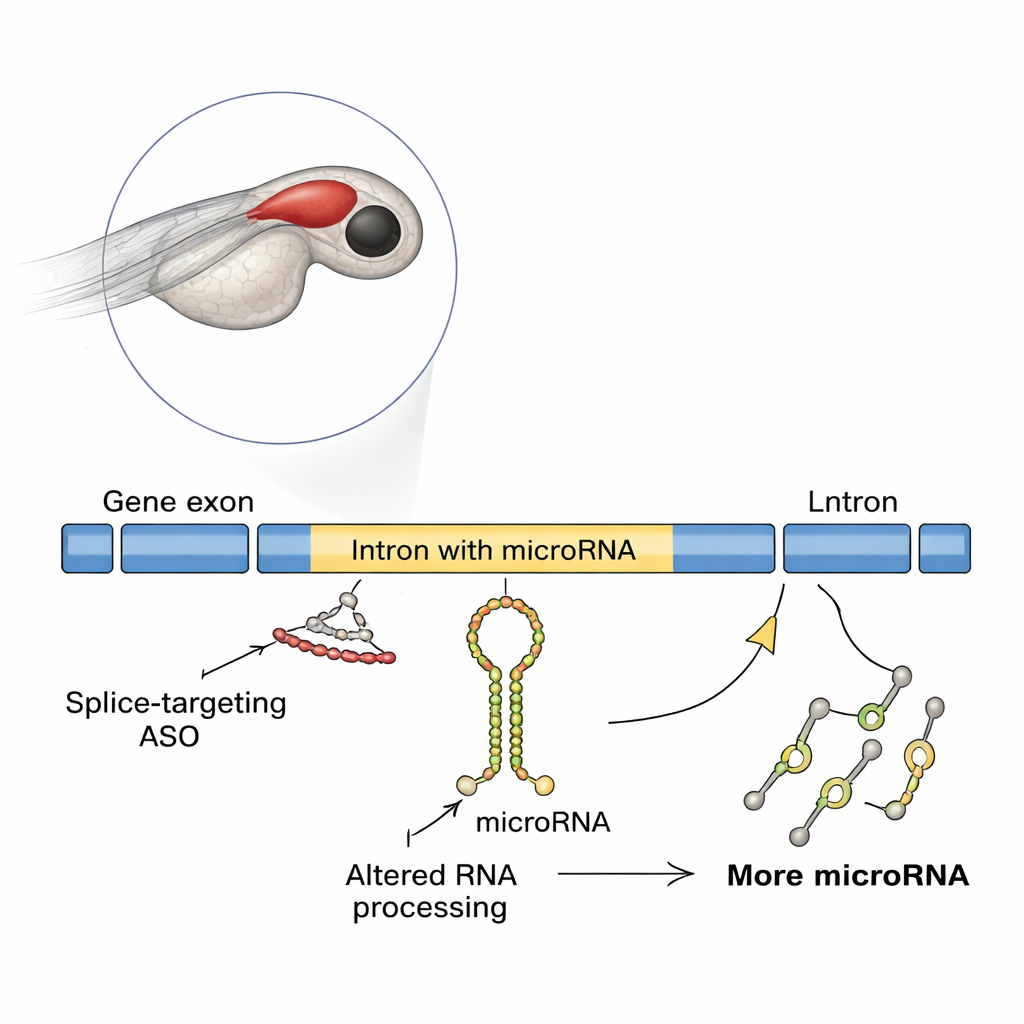
在发育中鱼类大脑中的意外效应
研究者使用斑马鱼这一常用的脊椎动物模型,其透明胚胎便于追踪大脑发育。他们聚焦于一个名为slit3的基因,该基因有助于神经纤维引导,并在其某个内含子中包含微小RNA mir-218a-1。当团队阻断slit3的起始翻译时,分泌激素的垂体轴突发育看起来正常。但当他们使用另一种ASO、阻断slit3特定位点的剪接时,原本应投射到后垂体的轴突明显减少,尽管产生催产素的神经元数量保持不变。分子检测显示,这种阻断剪接的ASO导致基因RNA的内含子滞留,出人意料地增加了slit3转录本、其长内含子以及内含子中初级mir-218a-1转录本的水平。
是微小RNA而非蛋白丢失导致缺陷
为弄清轴突问题的成因,作者比较了多种情形。单独阻断成熟的mir-218a-1并未改变slit3水平,而针对靠近该微小RNA的另一个剪接位点的ASO既未产生轴突缺陷也未提升mir-218a-1。关键证据是,当该阻断剪接的slit3 ASO与能中和mir-218a-1的ASO合用时,轴突连线大部分恢复。同样,在遗传上缺失mir-218a-1的斑马鱼中,相同的阻断剪接ASO不再引起轴突缺陷,而向正常鱼注入合成的mir-218a模拟物则能在正常鱼中复制该表型。这些实验证据指向内含子微小RNA升高——而非截短的Slit3蛋白——是发育紊乱的主要驱动因素。
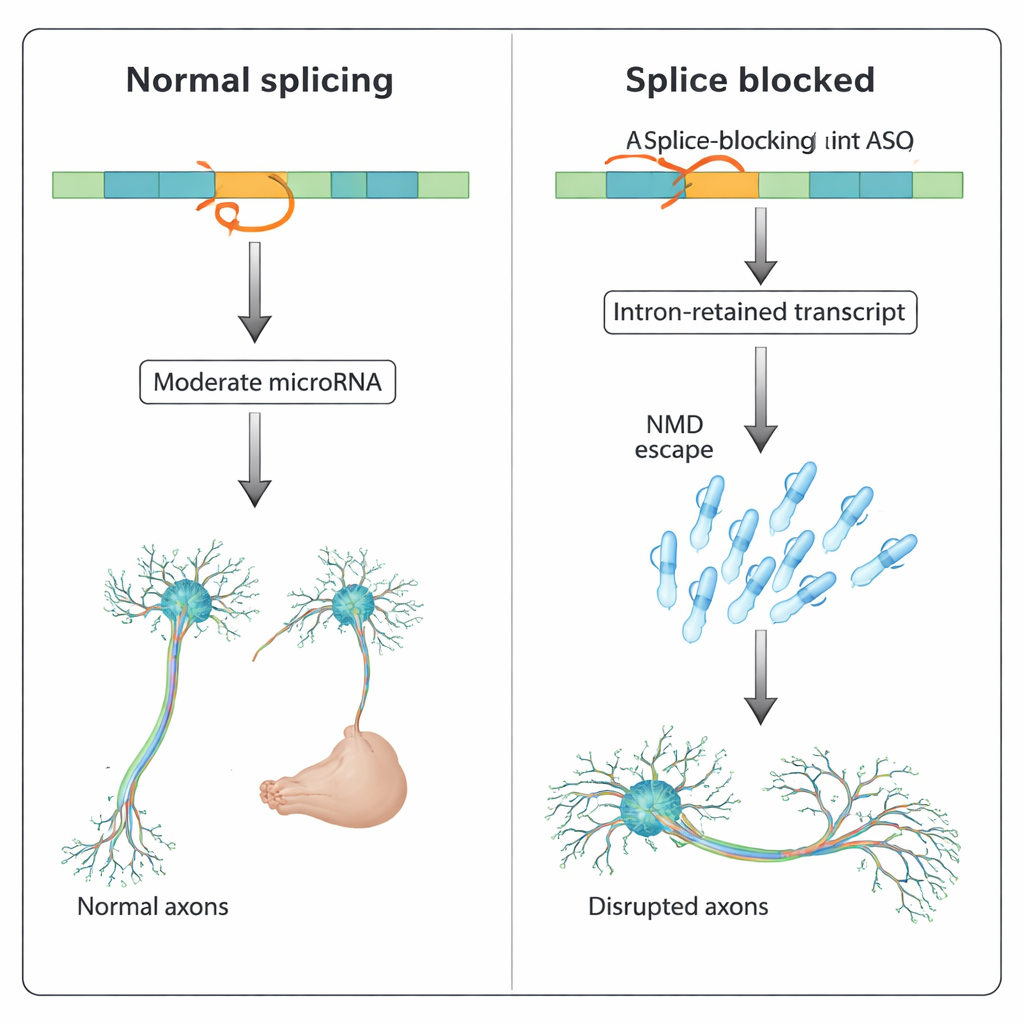
跨多基因的更广泛模式
研究团队随后探问该效应是否仅限于slit3。他们在斑马鱼基因组中检索,发现数十个编码蛋白的基因宿主内含子微小RNA,其中许多参与发育和信号传导。两个这样的基因pank2和dnm2a在此前被ASO阻断剪接时曾显示严重发育问题,包括脑积液增多、心脏肿胀和体形畸形——这些问题在基因敲除模型中并未重现。在本研究中,共注入能特异阻断内含子微小RNA mir-103(位于pank2)或mir-199-5p(位于dnm2a)的ASO部分挽救了这些由ASO诱发的表型。在某些情况下,微小RNA阻断还恢复了宿主基因表达,而在另一些情况下则没有,这表明即便整体表达变化有限,微小RNA活性升高本身也可能有害。
对未来治疗的意义
这些发现表明,靶向剪接的ASO不仅能导致外显子跳跃或内含子滞留:它们还可能稳定逃避细胞质控系统的内含子滞留转录本并提升内含子初级微小RNA,从而错误调控一系列靶基因。在发育中的神经元中,这类失控的微小RNA活动会扭曲轴突生长和连通性。对药物开发者而言,这意味着动物试验中出现的异常或“离靶”表型,并不总是源自诸如p53激活等通用毒性通路,而可能来自对隐藏内含子RNA的意外交互。仔细比较阻断翻译与阻断剪接的ASO,并监测内含子微小RNA表达,可帮助及早识别这些风险并在进入临床前优化ASO设计。
引用: Ali, M.H., Ramesh, A.R., Nedunchezhian, N. et al. Targeted blocking of gene splicing can dysregulate intron-embedded primary microRNAs. Commun Biol 9, 252 (2026). https://doi.org/10.1038/s42003-026-09529-7
关键词: 反义寡核苷酸, 微小RNA, RNA 剪接, 斑马鱼发育, 基因治疗安全性