Clear Sky Science · zh
haCCA:斑点型空间转录组学与代谢组学的多模块整合
为何在原位绘制分子图谱重要
我们的身体由无数微小的细胞群落构成,每个群落都有自己活跃的基因组合和化学物质。直到最近,科学家们仍需将组织研磨成均质糊状物来研究这些分子,因此丧失了“位置”信息。本文引入了一种新的计算方法,称为 haCCA,它将两种强大的成像技术拼接在一起,使研究者能够在原位观察基因与小分子如何在真实组织和肿瘤中分布。这类地图可以揭示被隐藏的病理模式并提示更精确的治疗策略。
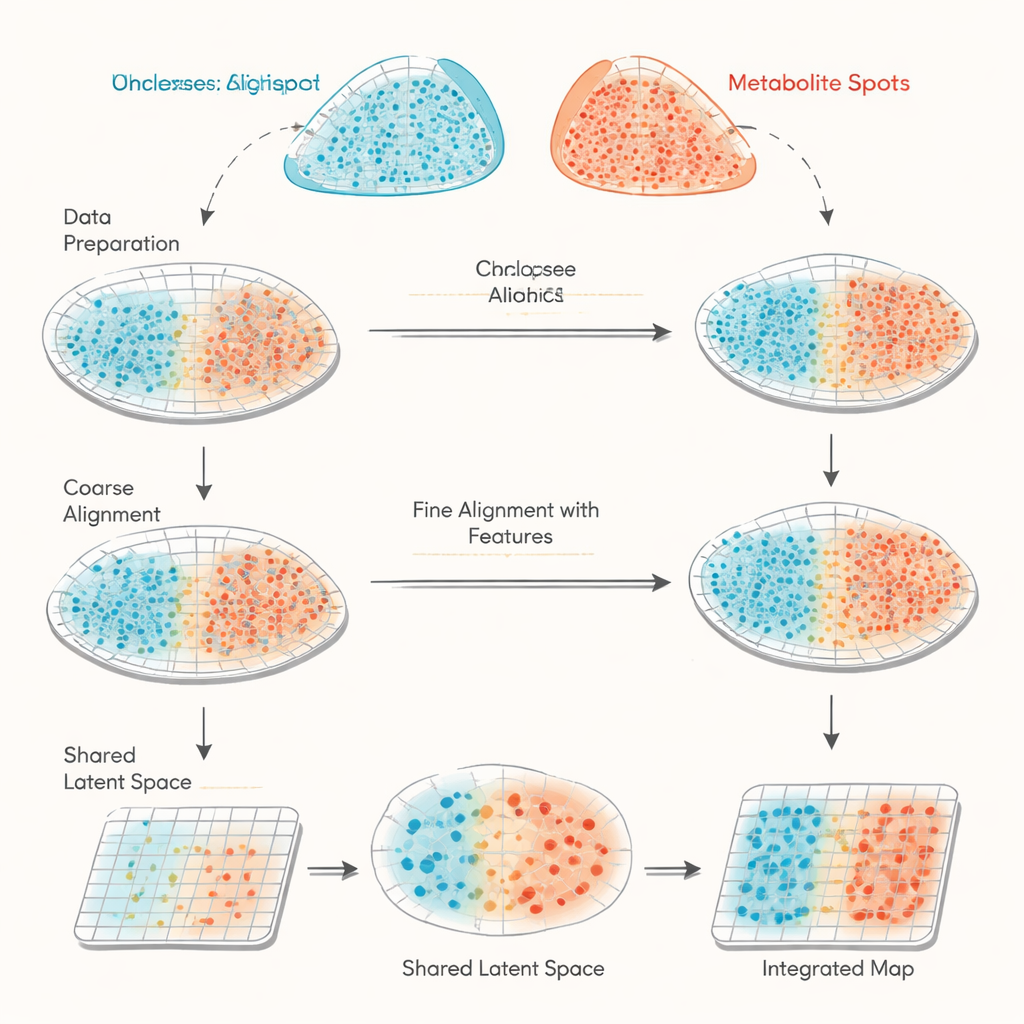
同一组织的两种不同视角
本研究着眼于整合两种在生物学中日益常用的空间方法。空间转录组学记录了组织切片上成千上万微小斑点处哪些基因被激活。MALDI 质谱成像则在类似密集的斑点网格上记录许多小分子(如代谢物和脂质)的含量。问题在于,这两台仪器并不测量完全相同的位置或相同的特征集合,因此它们的数据就像两张未对齐且图例不同的地图。现有方法大多仅基于坐标匹配组织形状,这在精度上可能不足,也缺乏检查对齐效果的方法。
一种更智能的分子图谱对齐方式
haCCA(分层锚点引导的典型相关分析)通过将几何信息与生物学信息结合起来应对这一挑战。首先,它对两种技术的斑点网格执行两步“形态学对齐”。人工专家在组织图像上选取少量匹配的标志点以粗略校正平移和旋转,然后自动化步骤对撕裂边缘或缺失区域附近的异常点进行微调。接着,该方法寻找空间上接近且位于局部均匀区域的“锚点”对,使它们很可能代表相同的组织区域。基于这些锚点,haCCA 计算哪些基因与代谢物倾向于共同变化,并将它们提炼为一个共享的低维表示,以捕捉最强的联合模式。
将相关性转化为统一的组织图谱
在掌握了空间坐标和共享的分子表示后,haCCA 求解一个优化问题,以决定每个基因斑点与每个代谢物斑点匹配的可能性。该步骤旨在既保持斑点的空间接近性,也保持它们在基因—代谢物组合特征上的相似性。最终结果是一个“传输方案”,将一个数据集中每个点与其在另一数据集中最匹配的点连接起来,生成整合的多模态地图。在精心构造的测试数据上(真实关系已知),作者展示了工作流程的每个阶段(粗对齐、精细对齐和考虑特征的匹配)如何逐步提高三个独立的准确性度量。与主要依赖几何信息的其他工具相比,haCCA 在对齐质量和区域标签的忠实传递方面始终表现更好。
在脑与肝癌中揭示隐藏的生物学
随后,作者将 haCCA 应用于真实的小鼠脑组织和肝肿瘤组织。对于脑组织,他们整合了商业化的空间转录组数据与来自同一或邻近切片的代谢物图像。该方法保留了已知的代谢区域,并重建了预期的共位图像,例如多巴胺与编码其关键酶的基因的共定位。通过对基因与代谢物联合聚类,他们发现整合数据能比任何单一模态更细致地区分组织亚区域。在一种肝内胆管细胞癌的前临床模型中——这是一种肝癌类型——他们利用 haCCA 比较能否形成中性粒细胞胞外诱捕网(由免疫细胞释放的网状结构)的肿瘤。整合后的地图显示,当这些诱捕网存在时,一种名为 Scd1 的基因及其相关脂肪酸在恶性区域中富集,指向肿瘤中脂质代谢发生改变的转向。
对未来研究的意义
通俗地说,haCCA 就像将用不同相机拍摄的航拍照片对齐——一台对建筑轮廓敏感,另一台对热信号敏感——从而获得更清晰的每个街区图景。通过准确合并基因活性位置与关键代谢物积累位置,这一工作流帮助科学家同时描绘细胞行为的两面:遗传指令与由此产生的化学反应。该方法在早期对齐方法之上有所改进,并以易用的 Python 工具形式提供,且可扩展到其他空间技术。随着此类整合图谱变得愈加常规,它们有望深化我们对肿瘤及其他组织如何组织其代谢、如何响应治疗以及如何随时间演化的理解。
引用: Xu, J., Shen, XT., Zhang, C. et al. haCCA: multi-module Integration of spot-based spatial transcriptomes and metabolomes. Commun Biol 9, 248 (2026). https://doi.org/10.1038/s42003-026-09526-w
关键词: 空间多组学, 转录组学, 代谢组学, 肿瘤代谢, 数据整合