Clear Sky Science · zh
尼莫唑德通过破坏NLRP3炎性小体活化缓解ARDS和溃疡性结肠炎
为何平抑失控炎症至关重要
许多严重疾病——从危及生命的肺功能衰竭到疼痛的肠道疾病——不仅由病原体或损伤直接驱动,更多情况下是机体自身免疫系统过度反应造成的。本研究探讨了一种来自印楝树的天然化合物尼莫唑德是否能作为对免疫细胞内一种强大炎症机器的精确“刹车”,从而为治疗急性呼吸窘迫综合征(ARDS)和溃疡性结肠炎等病症开辟更安全的途径。
免疫细胞内的麻烦警报器
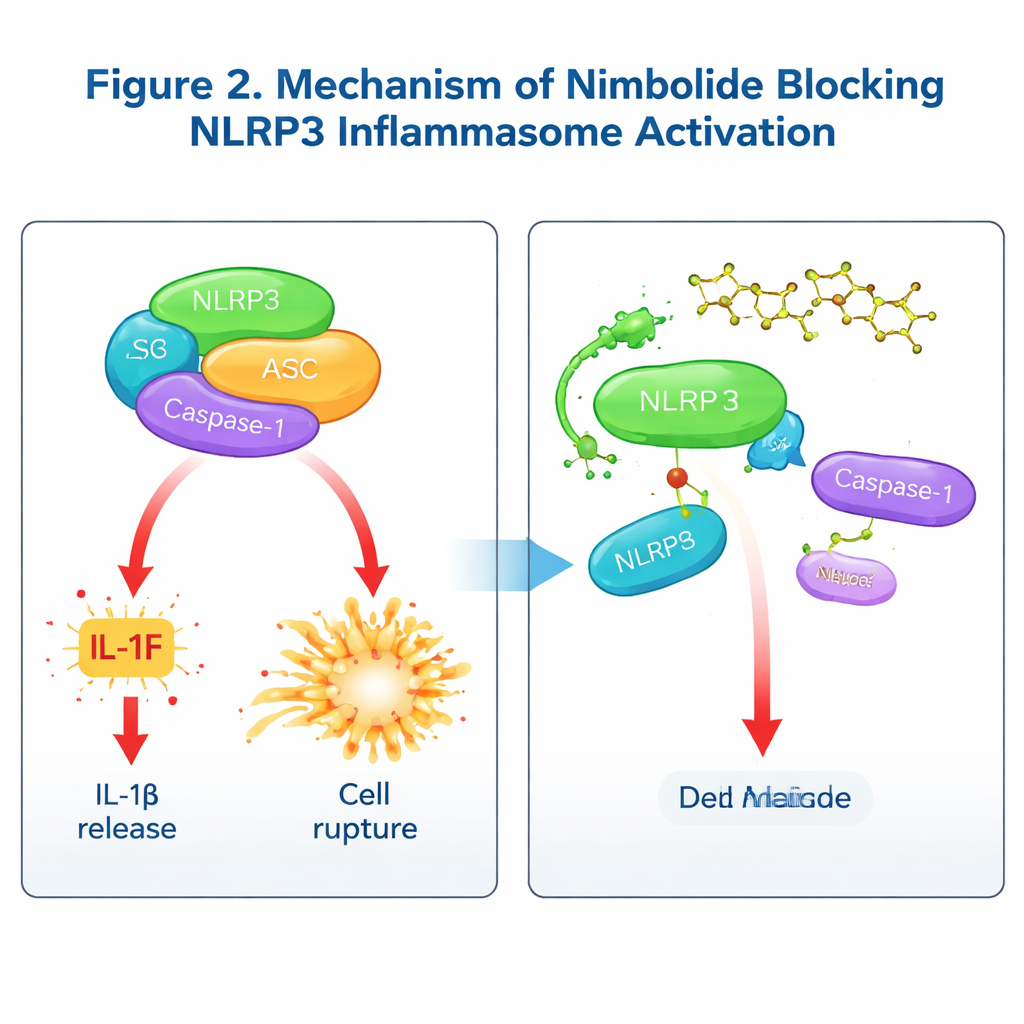
本研究的核心是一个分子级的警报系统,称为NLRP3炎性小体。当免疫细胞感知到危险信号——来自感染、组织损伤或晶体——该系统可像三部分组成的乐高结构一样组装:感受器NLRP3、连接蛋白ASC和酶Caspase‑1。组装完成后,这一复合体会激活强效的信使分子如IL‑1β和IL‑18,并能触发一种称为焦亡的剧烈细胞死亡形式。虽然该反应有助于清除威胁,但过度激活时会促成慢性和急性疾病的发展,包括关节炎、糖尿病并发症、阿尔茨海默病、ARDS和炎性肠病。药物开发者曾试图用合成化合物抑制NLRP3,但许多候选药物因毒性、副作用或体内不良表现而受挫,因此迫切需要更安全、更具选择性的抑制剂。
发现一种有效的植物来源抑制剂
研究者筛选了126种天然化合物,以确定哪种最能阻断小鼠免疫细胞释放IL‑1β。尼莫唑德脱颖而出,在测试剂量下使IL‑1β分泌降低超过80%。进一步实验显示,尼莫唑德显著抑制Caspase‑1活化、IL‑1β释放以及来自小鼠骨髓来源巨噬细胞的焦亡细胞死亡,其效力与基准药物MCC950相当。重要的是,尼莫唑德并未抑制其他免疫因子如IL‑6的释放,表明其作用较为聚焦,而非简单地全面抑制免疫。对多种触发NLRP3的刺激(如ATP、尼杰霉素、明矾晶体和imiquimod)进行测试时,尼莫唑德均持续降低炎性小体活性,包括在人类THP‑1细胞中。相反,它并不抑制两个相关的炎性小体AIM2和NLRC4,凸显其对NLRP3的特异性。
尼莫唑德如何阻断这一炎症机器
为弄清尼莫唑德的作用机制,团队探查它是干扰由NF‑κB通路控制的早期“致敏”步骤,还是作用于炎性小体物理组装的后期阶段。短期处理(在致敏后给予)并未影响关键的致敏信号和基因表达,但仍降低了IL‑1β和Caspase‑1的活化,表明尼莫唑德主要作用于组装步骤。详细的生化检测显示,尼莫唑德不改变钾或钙流动、线粒体损伤或NLRP3与其辅助蛋白NEK7的相互作用。相反,它扰乱了NLRP3与ASC之间的关键结合,减少ASC聚集成斑点,并阻止NLRP3形成更高阶的寡聚体。通过结合试验和分子建模,作者表明尼莫唑德直接附着在NLRP3的NACHT区的一个特定氨基酸赖氨酸565(Lys565)上。当该位点发生突变时,尼莫唑德不再能保护NLRP3免于降解或切断其与ASC的连接,从而确认Lys565为关键对接点。值得注意的是,尽管其他药物常靶向NLRP3的ATP酶活性,尼莫唑德则在不影响ATP利用的情况下阻断组装,提供了一种不同的作用模式。
在肺和肠疾病模型中测试尼莫唑德
研究团队接着检验这一分子效应是否能在疾病模型中转化为实际保护作用。在通过细菌毒素诱导ARDS的小鼠中,于挑战前给予尼莫唑德可减少肺组织损伤、液体积聚和空气腔蛋白质外漏。肺内浸润的免疫细胞减少,肺组织和血液中的IL‑1β水平下降。在将毒素直接送入气道的模型中也观察到类似益处。在另一个溃疡性结肠炎模型中,小鼠饮用损伤结肠的化学物质后,尼莫唑德减少了体重下降,改善了大便性状和出血评分,维持结肠长度,降低显微镜下的炎症和组织侵蚀迹象,并降低结肠中IL‑1β水平。关键的是,在基因工程敲除NLRP3的小鼠中,疾病本已较轻且尼莫唑德不再提供额外益处,这强调了其保护作用依赖于阻断NLRP3。
这对未来治疗意味着什么
对非专业读者而言,关键结论是尼莫唑德像一个智能刹车,针对机体最强大的炎症开关之一。它通过锁定NLRP3上的精确位点并阻止炎性小体组装,抑制肺部和肠道的过度炎症,同时不广泛破坏免疫防御。尽管尼莫唑德本身在稳定性和给药方式等方面仍需改进才能成为药物,这项工作将其定位为一个有前景的起点——也是设计下一代针对NLRP3驱动疾病(如ARDS和溃疡性结肠炎)药物的蓝图。
引用: Xu, H., Lin, Y., Luo, W. et al. Nimbolide ameliorates ARDS and ulcerative colitis by disrupting NLRP3 inflammasome activation. Commun Biol 9, 246 (2026). https://doi.org/10.1038/s42003-026-09524-y
关键词: 尼莫唑德, NLRP3炎性小体, 炎症, 急性呼吸窘迫综合征, 溃疡性结肠炎