Clear Sky Science · zh
全基因组甲基化关联循环白细胞介素‑6的研究将DNA甲基化与免疫代谢和炎症健康联系起来
这对日常健康意味着什么
慢性、低水平的炎症在无声中影响我们患2型糖尿病、心脏病和炎症性肠病等疾病的风险。血液中的一种信号蛋白白细胞介素‑6(IL‑6)是这一过程中的关键角色。本研究提出一个基本问题:IL‑6如何与我们的表观基因组——即帮助控制基因活性的DNA化学标记——相互作用,这对我们的长期健康意味着什么?
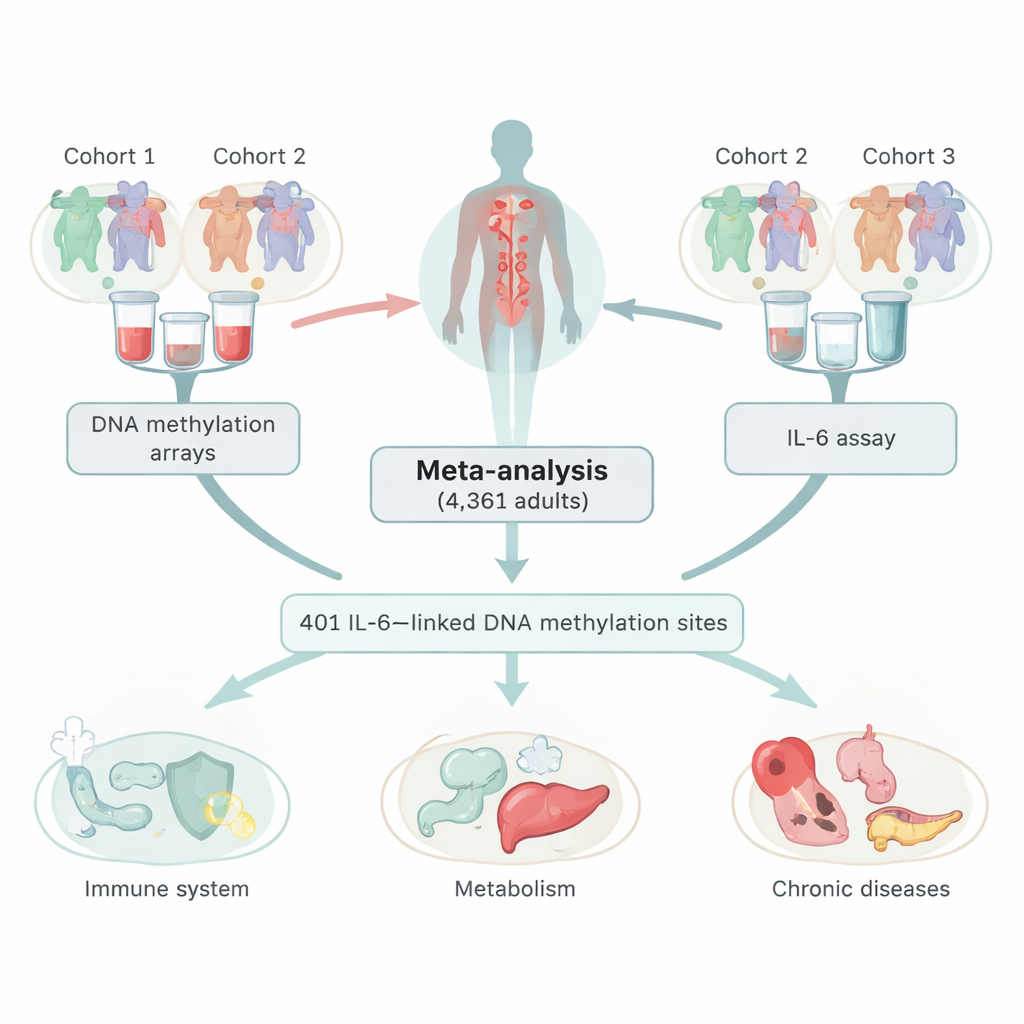
观察DNA上的化学标记
研究者汇集了三项大型欧洲研究的数据,涵盖了4,361名提供血样的成年人。在这些样本中,他们同时测量了IL‑6水平和DNA甲基化(一种常见的DNA化学标记,可在不改变遗传密码的情况下调节基因表达)。通过扫描基因组中超过40万个位点,他们识别出401个甲基化位点,其甲基化水平与血液中循环的IL‑6量相关。大多数这些位点表现出反向关系:IL‑6水平越高,这些位点的甲基化越低。研究团队还仔细验证了这些关联并非简单地由吸烟、血细胞类型差异或另一种炎症标志物C‑反应蛋白(CRP)引起的副作用。
将炎症与代谢和疾病联系起来
接下来,作者检验了这些与IL‑6相关的DNA位点是否与其他大型表观遗传研究中发现的信号重叠。他们发现这些位点在具有炎症或代谢成分的性状中高度富集,包括体重指数(BMI)、血脂、血压、血糖、2型糖尿病、慢性肾病以及精神和压力相关疾病。许多相同的甲基化位点此前也与CRP有关,但模式显示IL‑6和CRP各自携带部分不同的表观遗传特征。换言之,与IL‑6相关的化学标记并非CRP相关标记的简单复制,可能为个人的炎症和代谢状态提供额外信息。
基因组中活跃的区域
为了理解这些甲基化位点可能的功能,研究团队将它们映射到已知的基因组调控区域。他们发现与IL‑6相关的位点集中在活跃的控制元件中,如增强子——帮助开启基因的一段DNA——而非沉默区域。这些位点也位于与直接调控IL‑6和应激反应的转录因子结合序列附近,包括NF‑κB、Atf4、CHOP和Nrf2。通过将甲基化数据与大型基因表达数据集结合,研究者将400多个基因与IL‑6相关位点联系起来。许多这些基因位于免疫和代谢调控的核心,包括SOCS3、IL6R、AIM2、IFI16、MTOR和RORC,并参与驱动一种特化T细胞(Th17细胞)激活和能量使用的通路,该细胞类型与慢性炎症性疾病有关。
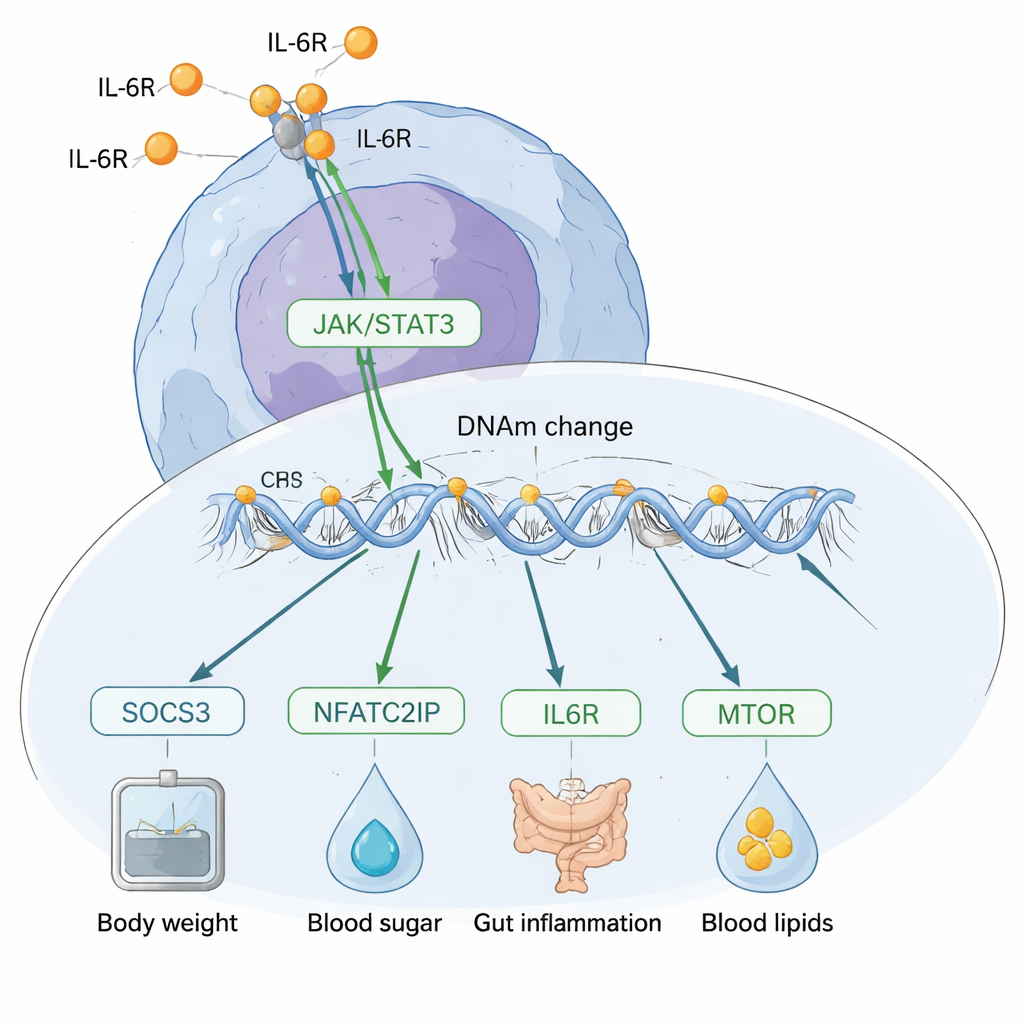
因果关系的方向是怎样的?
一个主要挑战是弄清DNA甲基化是导致IL‑6变化,还是IL‑6在重塑甲基化。研究团队使用了若干遗传学方法来探讨这一方向性。在全基因组层面,他们的“多角证据”分析支持这样一个模型:IL‑6主要驱动DNA甲基化的变化,而不是相反。随后他们聚焦于具体位点,发现SOCS3基因附近的甲基化变化似乎在中介IL‑6对体重、胆固醇、CRP水平和炎症性肠病等风险因素的影响。相反,靠近一个名为NFATC2IP的基因调控因子的一个突出位点则显示出可能影响IL‑6产生本身的迹象,并且似乎影响包括体重指数、2型糖尿病和肠道炎症在内的多种病况。
这对未来预防和治疗的意义
对非专业读者而言,核心信息是IL‑6与DNA上的表观遗传标记密切交织,影响多种常见疾病。大多数情况下,IL‑6会在基因组上留下化学“足迹”,特别是在免疫细胞中,标记并可能稳定促炎状态。然而在少数关键位点,甲基化可能帮助设定IL‑6的产生量以及免疫通路的反应强度。这些发现表明,DNA甲基化模式是有前景的血液生物标志,可用于反映炎症和代谢健康,并提示经过精确靶向的表观遗传改变——尤其是围绕SOCS3和NFATC2IP等基因——有朝一日可能补充IL‑6抑制药物,用于预防或治疗慢性疾病。
引用: Sinke, L., van Dongen, J., Delerue, T. et al. Epigenome-wide association study of circulating interleukin-6 connects DNA methylation to immunometabolic and inflammatory health. Commun Biol 9, 242 (2026). https://doi.org/10.1038/s42003-026-09520-2
关键词: 白细胞介素‑6, DNA甲基化, 炎症, 代谢性疾病, 表观遗传学