Clear Sky Science · zh
MAT2A通过SRF增强PARN转录以加速糖酵解并驱动骨肉瘤的恶性进展
这项骨癌研究为何重要
骨肉瘤是儿童和青少年中最常见的骨癌,几十年来治疗几无改变。许多年轻患者仍面临不良预后,尤其是在癌症转移或对化疗产生耐药时。本研究发现了一个隐蔽的“主控开关”蛋白MAT2A,能够帮助骨肉瘤细胞增殖、重塑能量代谢并形成侵袭性肿瘤——研究还表明,针对MAT2A的药物可以在实验模型中减缓或缩小这些肿瘤。
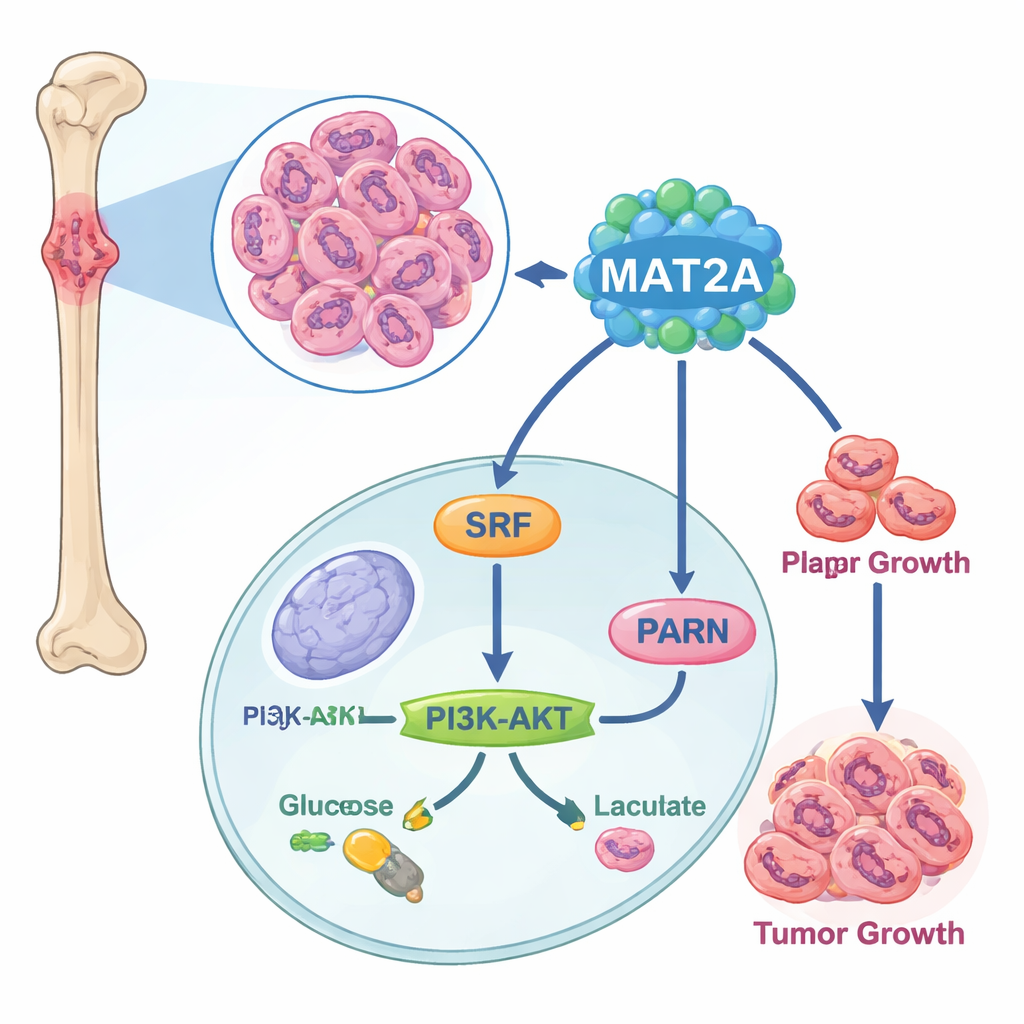
肿瘤细胞内的隐秘发动机
研究人员首先在单细胞水平比较了骨癌样本与正常骨组织。他们发现骨肉瘤组织中用于构建肿瘤的细胞更多、免疫细胞更少,且有一个基因——MAT2A——在癌细胞中异常活跃。对公共癌症数据库和体外细胞系的分析证实,骨肉瘤中MAT2A水平远高于健康骨细胞,且MAT2A较高的患者往往病情更晚期并伴有淋巴结转移。这使MAT2A被视为可能的疾病驱动因子,而非被动旁观者。
降低MAT2A可放慢癌症生长
为检验MAT2A对肿瘤行为的重要性,研究团队用基因学工具在骨肉瘤细胞系中降低MAT2A水平。沉默MAT2A后,癌细胞分裂变慢且更易发生程序性细胞死亡。在植入这些经改造细胞的小鼠中,肿瘤生长明显放慢且体积显著减小,而动物体重保持稳定。这些实验表明,骨肉瘤细胞在生存和形成肿瘤方面高度依赖MAT2A。
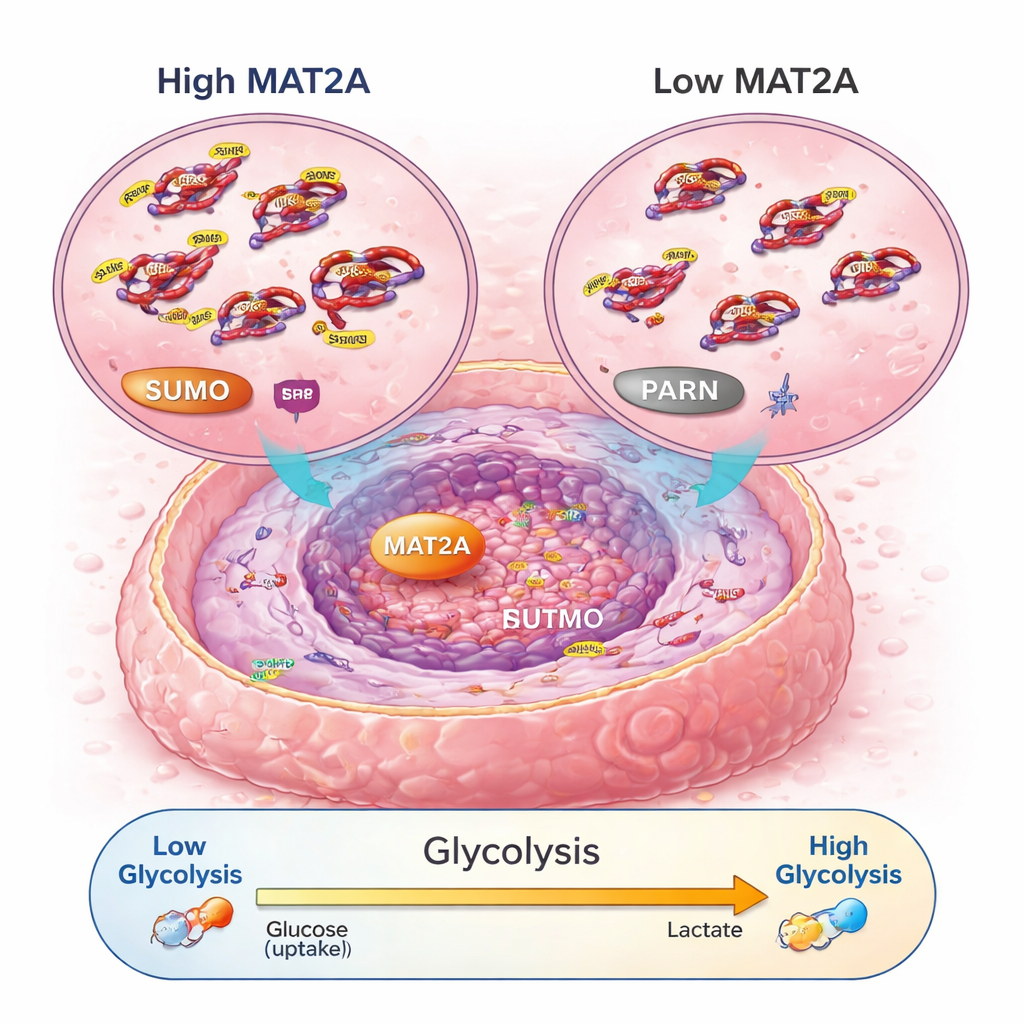
增强细胞燃料利用的信号传递
进一步研究发现,MAT2A不仅仅执行其常见的代谢功能。在细胞核内,它与转录因子SRF结合,通过促进一种称为SUMO的化学标记来维持SRF的稳定和活性。反过来,SRF启动了PARN基因的表达,PARN随后激活了众所周知的PI3K–AKT通路并上调有氧糖酵解的机制——这种快速但效率较低的能量生成方式是癌细胞偏好的。当降低MAT2A时,癌细胞的ATP(能量货币)减少、葡萄糖摄取下降、乳酸生成减少,并向更依赖氧的呼吸方式回归。破坏PARN或AKT可以抵消MAT2A带来的促生长和促糖酵解效应,证实了MAT2A→SRF→PARN→PI3K–AKT这一传递线路是骨肉瘤中的关键能量与生长回路。
非常规功能与可药靶点
值得注意的是,即使MAT2A缺失其常规酶促活性,仍能支持SRF稳定性和PARN激活,说明其促癌作用并不依赖于其典型的化学反应。相反,MAT2A更像一个组织其他蛋白的支架。这具有实际意义:药物不必一定阻断其催化位点就能削弱肿瘤。研究者测试了一种名为FIDAS-5的小分子抑制剂,针对MAT2A,在细胞培养和小鼠模型中均进行了验证。该药物处理减少了核内SRF,降低了PARN和PI3K–AKT信号,抑制了糖酵解,放慢了细胞生长并诱导癌细胞死亡。在小鼠体内,FIDAS-5使肿瘤缩小或增速放缓且未见明显体重下降,提示在该设定下具有可耐受的副作用。
对患者与未来疗法的意义
对非专业读者而言,核心信息是:骨肉瘤细胞依赖MAT2A维持其生长程序和高强度的“烧糖”动力。通过稳定关键调控蛋白并放大一系列信号,MAT2A帮助肿瘤更快生长并变得更具侵袭性。阻断这一蛋白——无论是基因手段还是像FIDAS-5这样的药物——都能切断这种支持,使癌细胞放慢增殖、降低亢奋的能量代谢并最终走向死亡。尽管在此类治疗进入临床之前仍需大量工作,这项研究将MAT2A定位为抗骨癌的有前景新靶点,为为年轻患者开发更精确、毒性更低的治疗打开了潜在路径。
引用: Ren, Z., Chen, H., Qiao, Q. et al. MAT2A enhances PARN transcription via SRF to accelerate glycolysis and drive malignant progression in osteosarcoma. Commun Biol 9, 241 (2026). https://doi.org/10.1038/s42003-026-09518-w
关键词: 骨肉瘤, MAT2A, 癌症代谢, PI3K AKT通路, 靶向治疗