Clear Sky Science · zh
来自抗体稀释系列的免疫染色位点异质性计算分析
为什么抗体染色质量很重要
从追踪癌细胞到诊断感染,现代生物学在很大程度上依赖于能够“点亮”细胞内特定分子的抗体。然而,许多实验室暗地里都在与一个令人头疼的问题斗争:染色信号过弱、噪声太大或结果误导性强。本文介绍了一种实用的、基于计算的方法,从常规抗体稀释系列中提取更多信息,帮助研究人员调优染色以获得更清晰的图像、更可靠的测量,甚至实现用单一颜色通道染色多个靶点的新方法。 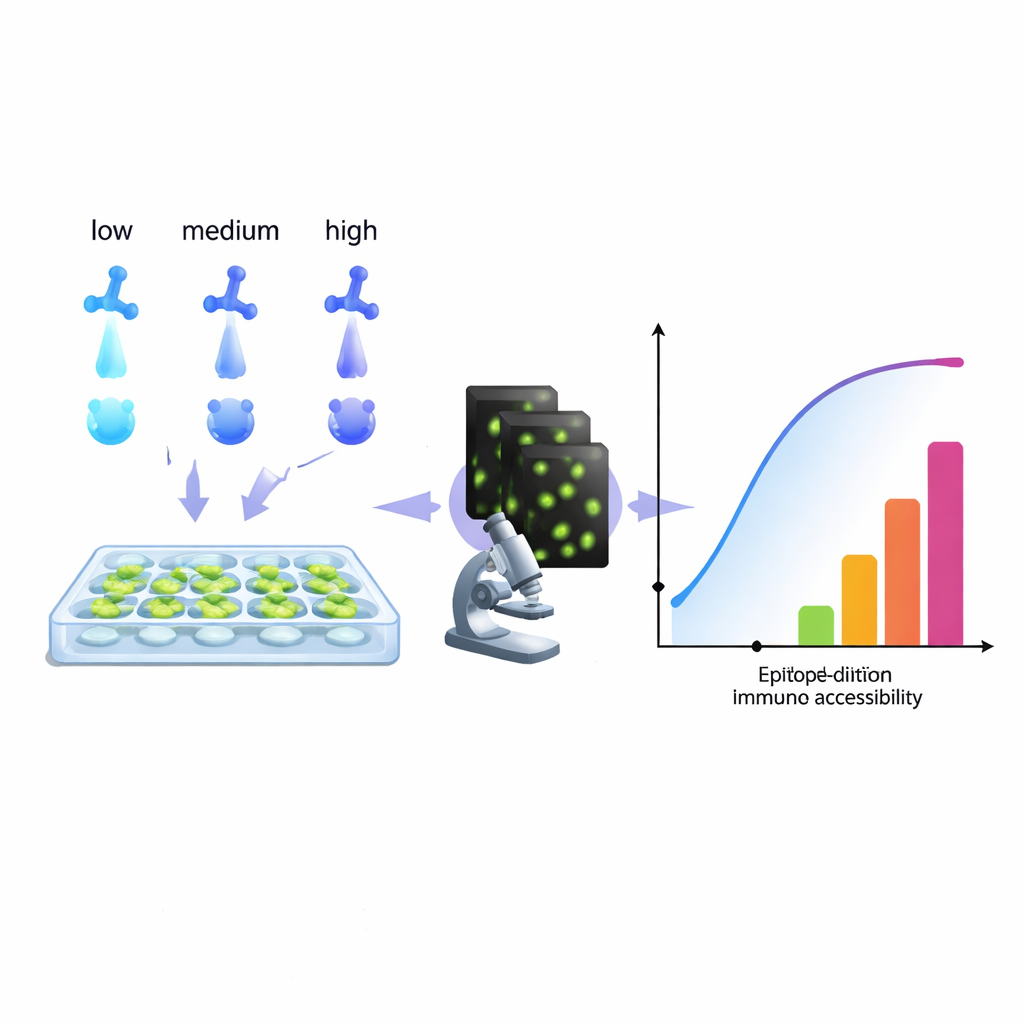
科学家通常如何调整抗体染色
当研究人员设置免疫染色实验时,通常根据产品说明书估算抗体浓度,尝试几种稀释度,然后选择“看起来不错”的那一个。但在背后,无数细小因素——蛋白质构象、细胞内部的拥挤程度、pH 值以及抗体能否灵活进入结合位点——决定了抗体是结合还是被洗掉。传统测量抗体结合的工具(如表面等离子共振)在纯化蛋白和人工表面上效果最好,而不适用于高密度的细胞或组织。这意味着这些方法给出的数值可能与抗体实际使用的生物系统不一致。因此,实验室可能在不知情的情况下选择会增强模糊背景或掩盖重要但难以可及靶点的浓度。
将简单的稀释系列转化为“可及性图谱”
作者提出了一种不同的思路:把标准的抗体稀释系列视为丰富的数据集,用一个反映显微镜实际观测到内容的模型去拟合——也就是洗涤后仍保持结合的抗体。通过分析信号随浓度的增长情况,他们的算法重构出一个“可及性直方图”。与其试图隔离纯化学结合常数,这个直方图把靶位点按在真实条件下染色难易程度分为若干技术性的“表位类别”。同一生物学表位可能在多个类别中出现,例如在细胞某一部分容易达到而在拥挤区更难到达。关键是,该方法直接以显微镜读数为依据,不需要纯化蛋白或额外硬件,因此任何能够执行稀释系列并量化荧光的实验室原则上都可以构建这样的直方图。 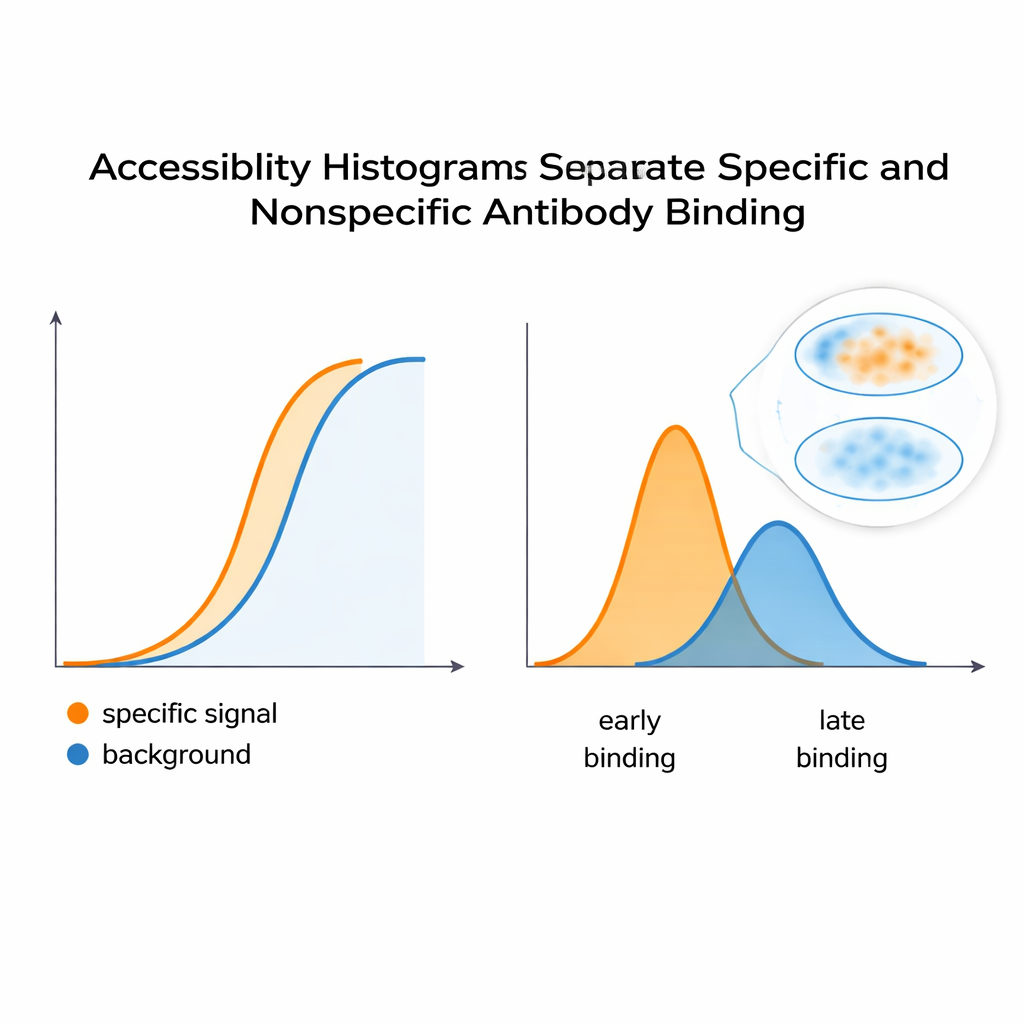
将真实信号与背景分开
为了检验这些直方图是否真正捕捉了染色行为,研究团队建立了一个受控体系,使用 HeLa 细胞和两种单克隆抗体:一种模拟期望的特异性信号,另一种充当不想要的背景。当两者混合时,整体荧光曲线看上去像一条平滑的单一响应——表面上没有明显提示有两个不同的贡献者。但计算分析将这条曲线拆分为可及性直方图中的独立峰,揭示了至少两类潜在表位。类似策略应用于识别 PKA 调节亚基的构象敏感位点的抗体,显示由 cAMP 触发的蛋白构象变化会改变可及表位的分布。这表明该方法可以标记蛋白结构的打开或闭合,进而改变抗体在细胞内的结合难易。
选择更好的稀释度并用一种颜色染出更多信息
由于可及性直方图中的每个峰主要在某一浓度范围内贡献信号,作者将这些峰作为选择“最佳稀释度”的指南。仅在非常高抗体浓度下出现的低可及性峰很可能包含非特异性结合,而早期出现的峰通常反映预期靶点。通过对各个峰如何构建整体剂量—反应曲线建模,团队可以建议在问题峰出现前最大化特异性信号的稀释度——有时远比供应商的推荐要稀释得多。他们还将这一思路扩展为一种巧妙的“计算复用”方法:对同一样本用精心选择的不同浓度反复染色,每轮成像并将早期图像从后期图像中减去,从而分离出与不同可及性类别相关的信号,有效地在单一荧光通道中区分多个靶点。
对日常实验室工作的意义
简而言之,这项工作把一个常规的故障排查步骤——运行抗体稀释系列——变成了一个定量工具。可及性直方图帮助科学家发现染色中的隐藏复杂性、选择能减少误导性背景的稀释度,并在某些情况下无需额外荧光标记就能分离重叠信号。尽管其基础模型刻意保持简洁,未能覆盖所有分子细节,但它被设计为易于使用且对真实数据足够稳健。如果被广泛采纳,这种方法有望使基于抗体的技术——从基础成像到诊断检测——更可靠、更具信息量并减少摸索式试验。
引用: Tschimmel, D., Saeed, M., Milani, M. et al. Computational epitope heterogeneity analysis in immunostainings from antibody-dilution series. Commun Biol 9, 238 (2026). https://doi.org/10.1038/s42003-026-09517-x
关键词: 抗体染色, 免疫荧光, 表位可及性, 剂量反应, 计算复用