Clear Sky Science · zh
将分子张力与细胞牵引相连:一种多尺度的黏着斑力学方法
细胞如何感觉并拉扯周围环境
每当细胞移动、分裂或重塑组织时,它都会悄悄地拉动周围环境。这些微小的机械牵引在伤口愈合、癌症扩散和器官发育中起着关键作用,但它们难以被观察,测量起来更是棘手。本研究提出了一种从两个角度同时观察这些力的新方法:一是整个细胞对软材料施加的总体牵引,二是细胞黏着位点内单个“分子弹簧”所承受的力。通过将这两种视角联系起来,工作有助于解释细胞如何感知刚度并调节它们与周围环境的抓取力。
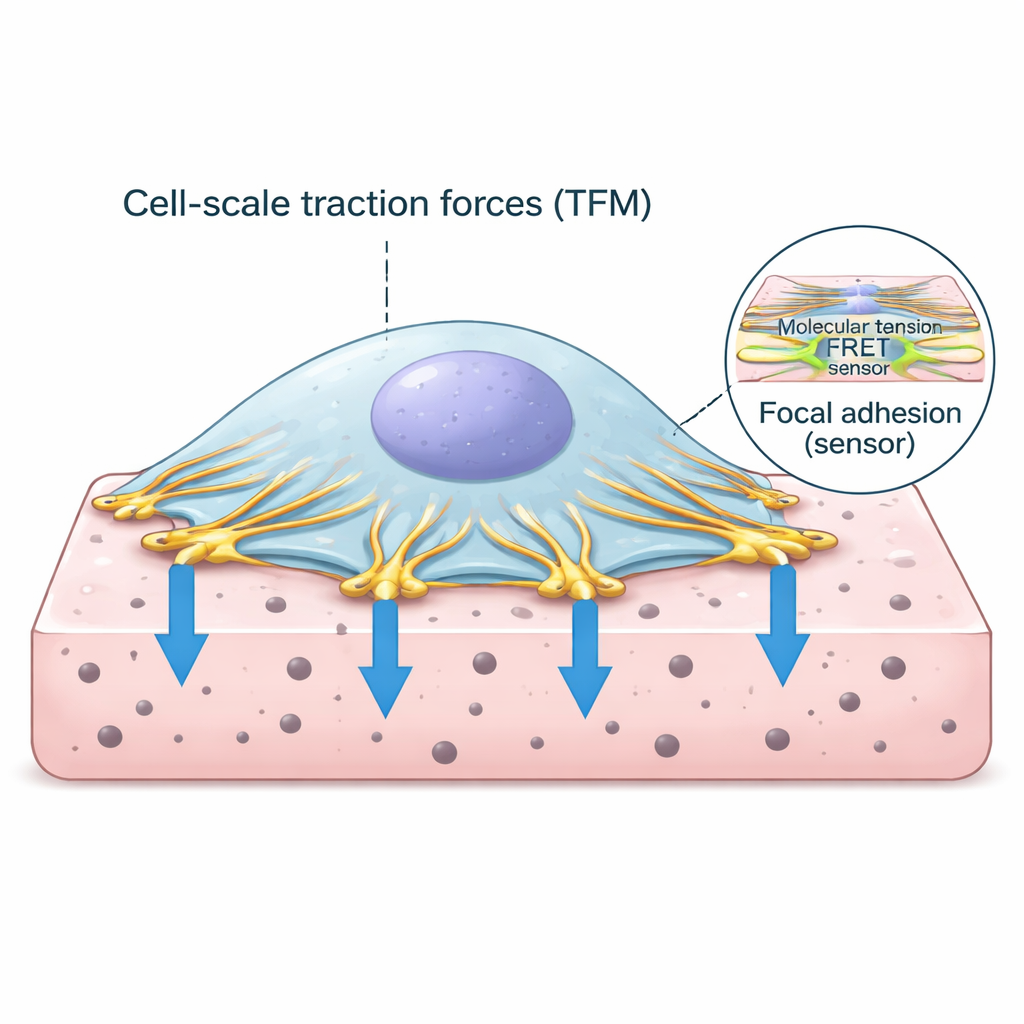
细胞在外部世界的抓握点
细胞并非在组织中漂浮不定;它们通过称为黏着斑的专门接触点将自己锚定。在这些位置,细胞内部的肌动蛋白纤维骨架连接到穿过细胞膜并与周围基质结合的蛋白质复合体。黏着复合体中的关键蛋白之一是文库林,它像一个对力敏感的连接件。当细胞的收缩装置牵拉肌动蛋白时,文库林感受到负载并有助于加强连接。理解有多少力通过这些连接传递以及这与细胞的整体牵引之间的关系,对于解码组织如何保持健康或转为病变至关重要。
观察细胞力的两扇窗口
研究者将两种强有力的技术整合到单一工作流程中。首先,牵引力显微术通过追踪凝胶中微小荧光微球的位移来测量细胞使柔软凝胶基底发生的变形。根据这些微球的运动,可以计算出细胞下方的推拉力分布。其次,一种经特殊设计的文库林蛋白携带荧光张力传感器,该传感器在被拉伸时会改变其光学信号。利用先进的寿命成像技术,研究团队将这一光学信号转换为文库林上的分子张力读数。他们制备了可进行高分辨率成像的薄平水凝胶,并编写了定制软件来对齐、分割并分析这两套数据,精确到单个黏着位点。
刚度如何改变细胞的用力
当细胞在软凝胶与更硬凝胶上培养时,它们的整体行为发生了明显变化。在较硬的基底上,细胞铺展得更开并在凝胶表面施加更强的牵引力。与此同时,来自文库林传感器的荧光信号显示黏着斑内的分子张力增大。有趣的是,这些黏着斑的基本结构特征——例如数量或平均大小——在软硬基底之间并未发生显著变化。变化的是力的组织方式。大而沿放射状排列、文库林含量更多的黏着斑往往承担更高的牵引力,这表明这些位点的几何形态和分子组成共同决定了细胞的拉力大小。
局部牵引与分子力之间的复杂关系
更加细致地观察单个黏着斑显示,局部牵引与文库林张力之间的关系并非千篇一律。在一些细胞中,产生较高牵引的黏着斑同时表现出较高的文库林张力,这意味着承载负荷的接触点通过其分子连接更直接地分担力。而在另一些细胞中,出现了相反的模式:强牵引区域的文库林张力较低,而其它黏着斑承受更多的分子负载却未产生大的外向牵引。许多细胞则没有显示出明确的模式。这些不同的行为很可能反映了细胞处于不同状态——例如积极铺展、稳固黏附或收缩—并暗示细胞可以通过多种方式在其黏着网络中重新分配力。
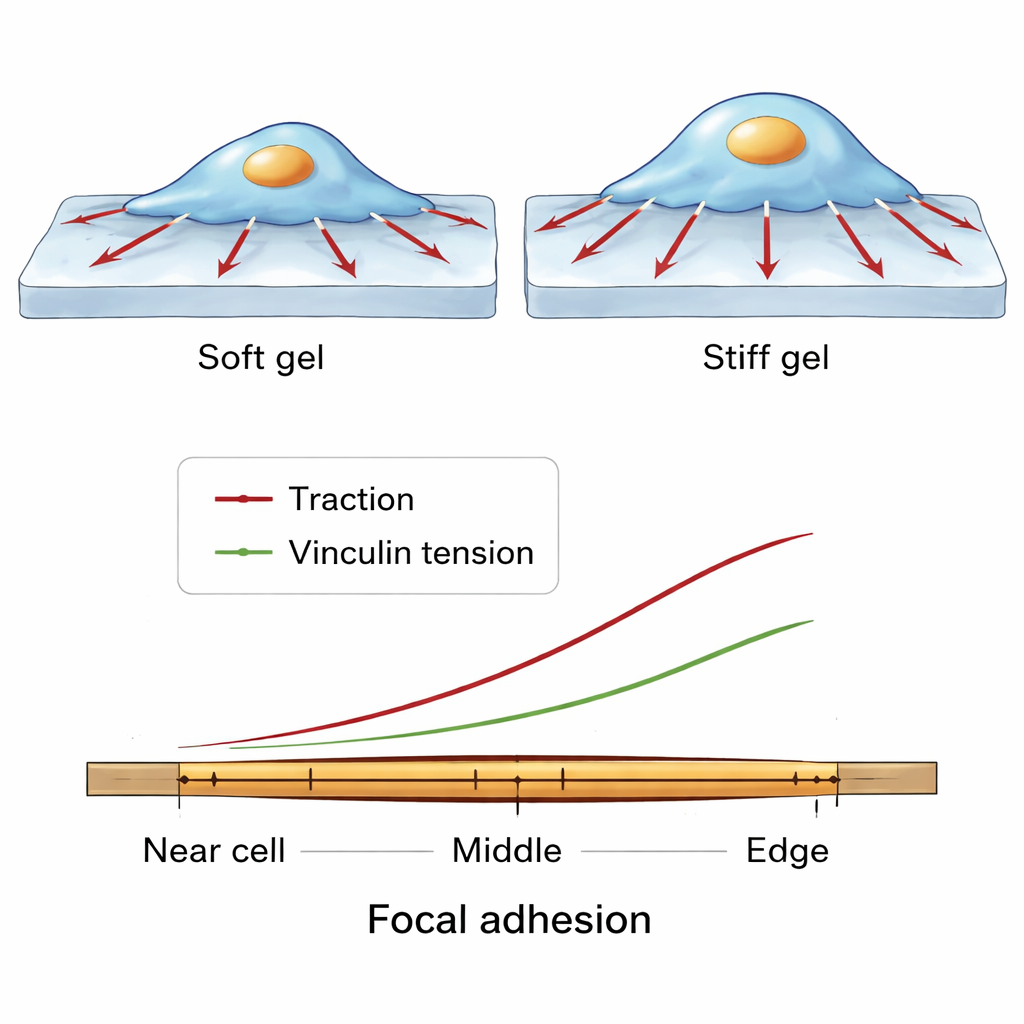
沿单一抓握点的精细力模式
研究团队进一步放大观察,检查单个位点黏着斑沿长度方向的力如何变化——从靠近细胞中心的一侧到靠近细胞边缘的一端。在许多细胞和条件下,出现了一个一致的模式。文库林分子在黏着斑的中部更为密集。然而,无论是作用于基底的牵引力还是文库林上的分子张力,都朝向外周端升高。这提示一种平衡:在中心区域,许多文库林分子可以分担负载,因此每个分子感受到的张力较小;而在外缘,较少的分子承受相对更多的力,从而支持局部强力牵拉同时保持黏着斑的完整性。
这对健康与疾病意味着什么
通过将整细胞的牵引图与蛋白水平的张力测量融合,本研究提供了一个关于细胞如何管理机械抓握的多尺度图景。研究表明,随着环境变硬,细胞既更用力地拉扯,也更多地给文库林连接施加负载,但外向牵引与分子张力之间的具体关系在不同黏着斑和不同细胞间各不相同。同时,单个黏着斑内存在一个稳健的力空间分布模式。对于非专业读者来说,关键结论是:细胞微妙地调整它们拉扯的位置与方式,通过将力在许多小的分子“弹簧”之间重新分配来适应不同的机械环境——这一原理可能是组织发育、纤维化与癌症侵袭等多种过程的基础。
引用: Aytekin, S., Kimps, L., Coucke, Q. et al. Linking molecular tension and cellular tractions: a multiscale approach to focal adhesion mechanics. Commun Biol 9, 236 (2026). https://doi.org/10.1038/s42003-026-09514-0
关键词: 细胞力学, 黏着斑, 文库林, 牵引力显微术, 机械信号转导