Clear Sky Science · zh
LbuCas13a在人体细胞中对伴随RNA切割的时间动力学
将细菌防御机制变为可精确触发的细胞自毁开关
研究人员发现了一种方法,可以把一种细菌免疫蛋白改造为对人类细胞高度选择性的“自毁”开关。通过利用一种名为LbuCas13a的CRISPR酶,他们能够识别细胞内指定的RNA信息,然后几乎摧毁该细胞的其他大部分RNA。对于普通读者来说,这很有吸引力,因为RNA信息决定细胞制造哪些蛋白;学会按需抹除这些信息,将为癌症新疗法、抗病毒策略以及强大的研究工具打开新途径。
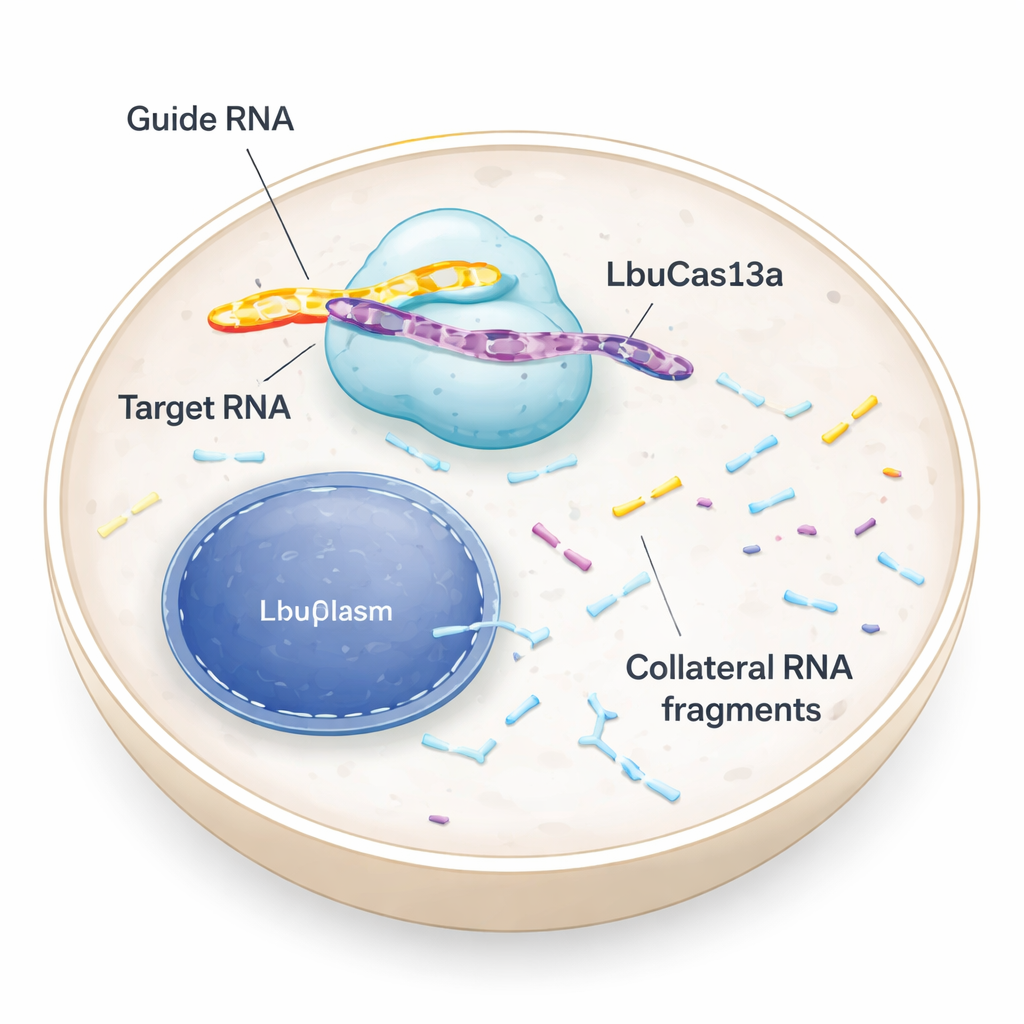
针对RNA的分子剪刀,而非DNA
大多数人听说过会切割DNA、重写遗传代码的CRISPR工具。LbuCas13a则不同:它识别并切割RNA,这些是从DNA到细胞蛋白质工厂的临时指令。在细菌中,Cas13酶属于抗病毒防御机制。一旦识别到病毒RNA,它不仅会切割该入侵者的RNA,还会开始切割周围的许多其他RNA。这种所谓的“伴随”活性可以使受感染细胞进入休眠或死亡,从而保护细菌群体。早期在动物和人类细胞中的测试显示,Cas13的伴随切割较弱或不存在,因此该酶主要被用作精确的RNA“关闭”工具。新研究重新审视了这一假设,并表明在适当条件下,人类细胞中的伴随活性既能强烈出现又具有实用价值。
在人类细胞中释放伴随切割
研究团队比较了多种Cas13变体,发现LbuCas13a尤其强效。他们将预先加载了短向导RNA的纯化LbuCas13a蛋白直接输送到人类细胞中,这种类似分子“蛋白注射”的方式称为核糖核蛋白(RNP)递送。当向导序列与目标RNA匹配——例如荧光标记基因或如GAPDH和18S核糖体RNA等丰度较高的天然转录本——酶先切割该目标,然后开始吞噬许多其他RNA。大约50分钟内,细胞的整体RNA谱发生显著变化,出现了典型的切割片段。这种伴随效应在不同的递送方法和多种细胞类型中均有观察到,表明它并非某一细胞系或某一人工靶标的特殊现象。
从RNA粉碎到细胞死亡与富集选择
当一个细胞的RNA信息突然消失时会发生什么?通过活细胞成像,研究者观察到表达目标RNA的细胞逐渐进入凋亡,这是一种整洁的程序性细胞死亡,伴随典型的“早期预警”信号,随后细胞崩解。重要的是,不表达目标RNA的邻近细胞大多不受影响,表明自毁是有特异性的。研究组随后将这一特性用作选择工具。当他们将带有目标的细胞与正常细胞混合并激活LbuCas13a时,带目标的细胞在数天内被选择性消耗。反复处理数次可进一步降低其比例。他们展示了这可用于富集成功基因编辑的细胞,也可调节用于攻击过度表达致癌基因(此处为CDK4)的癌细胞,同时较少影响那些该RNA产量远低于其的相关细胞。
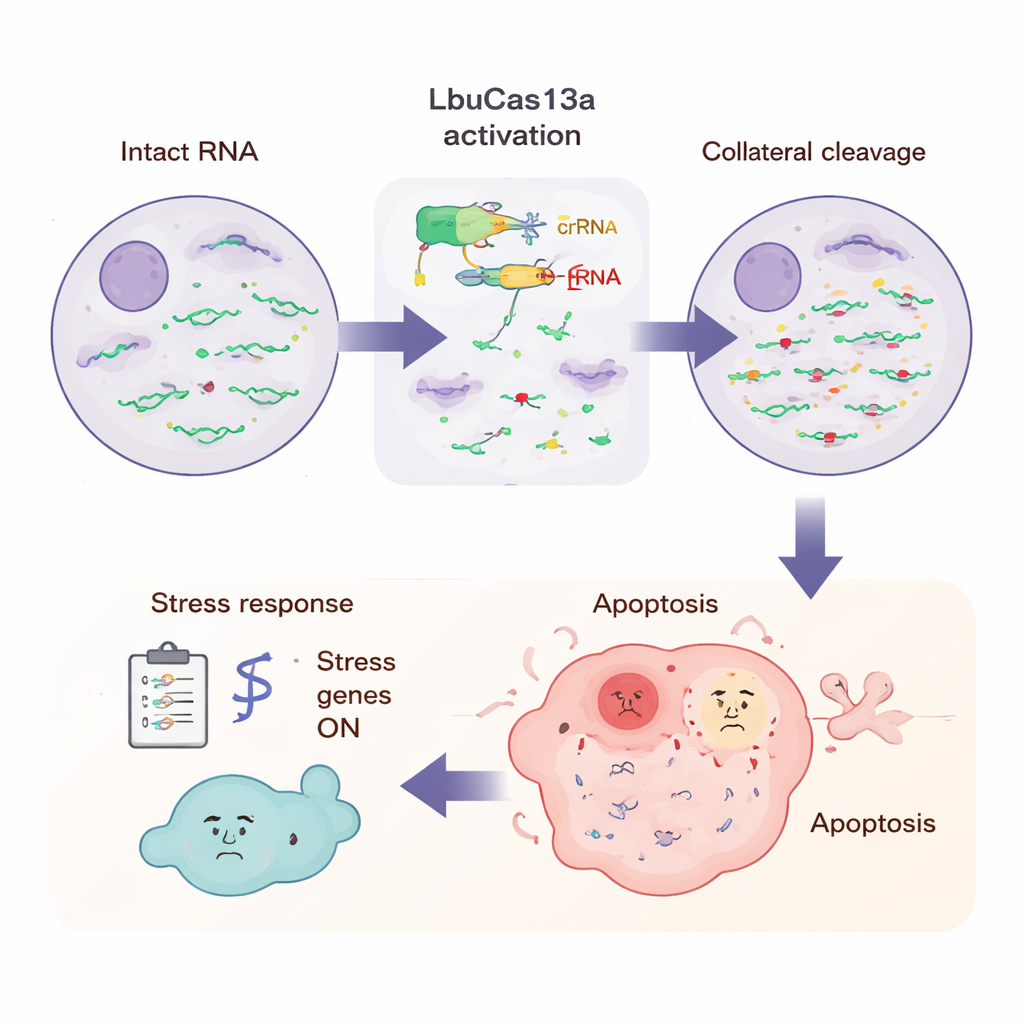
细胞在攻击过程中经历了什么
为了看到更全面的情况,科学家在激活LbuCas13a后多个时间点测量了细胞中的全部RNA。通过加入已知的RNA标准,他们能够确定大多数胞质中的蛋白编码RNA在数小时内下降超过一半,而某些RNA——例如线粒体转录本和一些核内非编码RNA——在很大程度上得以保留。长读长测序显示切割发生在重复且特异的核苷酸位置,常见于富含尿嘧啶的、呈环状回折的柔性RNA区段,这与体外实验中观测到的模式相符。在后期时间点,许多应激和固有免疫基因被激活,包括与炎症信号和抗病毒防御相关的基因。该模式表明,细胞感知到大量断裂的RNA末端,类似于检测到病毒感染,从而触发一套警报程序,最终导致凋亡。
为何重要以及可能的前景
简单来说,这项研究表明LbuCas13a可以被转化为一个由RNA引导的“细胞杀伤开关”:如果细胞产生过量某种RNA,针对该RNA激活LbuCas13a会导致近全局的RNA丧失、类似免疫的警报反应,随后是可控的细胞死亡。由于该过程强烈依赖于目标RNA的丰度,它可用于消除过度表达有害基因的细胞——例如某些癌细胞——或在研究或细胞治疗制造过程中清除混合培养中不需要的细胞。与此同时,这项工作也提醒人们:针对RNA的CRISPR工具可能产生强烈的副作用,必须谨慎管理。理解伴随RNA切割何时以及如何发生,对于在医学和生物技术中安全使用Cas13技术至关重要。
引用: Bot, J.F., Zhao, Z., Li, M. et al. Temporal dynamics of collateral RNA cleavage by LbuCas13a in human cells. Commun Biol 9, 233 (2026). https://doi.org/10.1038/s42003-026-09511-3
关键词: CRISPR-Cas13, RNA切割, 细胞死亡, 癌症靶向, 基因编辑工具