Clear Sky Science · zh
血浆膜脂质对人类B1类GPCR的调节
微调我们细胞信号接收器的脂质
我们的细胞依靠称为受体的小型蛋白天线来感知激素和脑内化学物质。许多畅销药物就是通过靶向这些受体发挥作用。本研究揭示,存在于细胞外层的常见脂质远不止形成静态背景:它们直接抓握并塑形整簇关键受体,细微地引导信号的开启或关闭。理解这一隐蔽的调控层可有助于设计更智能、副作用更少的药物。
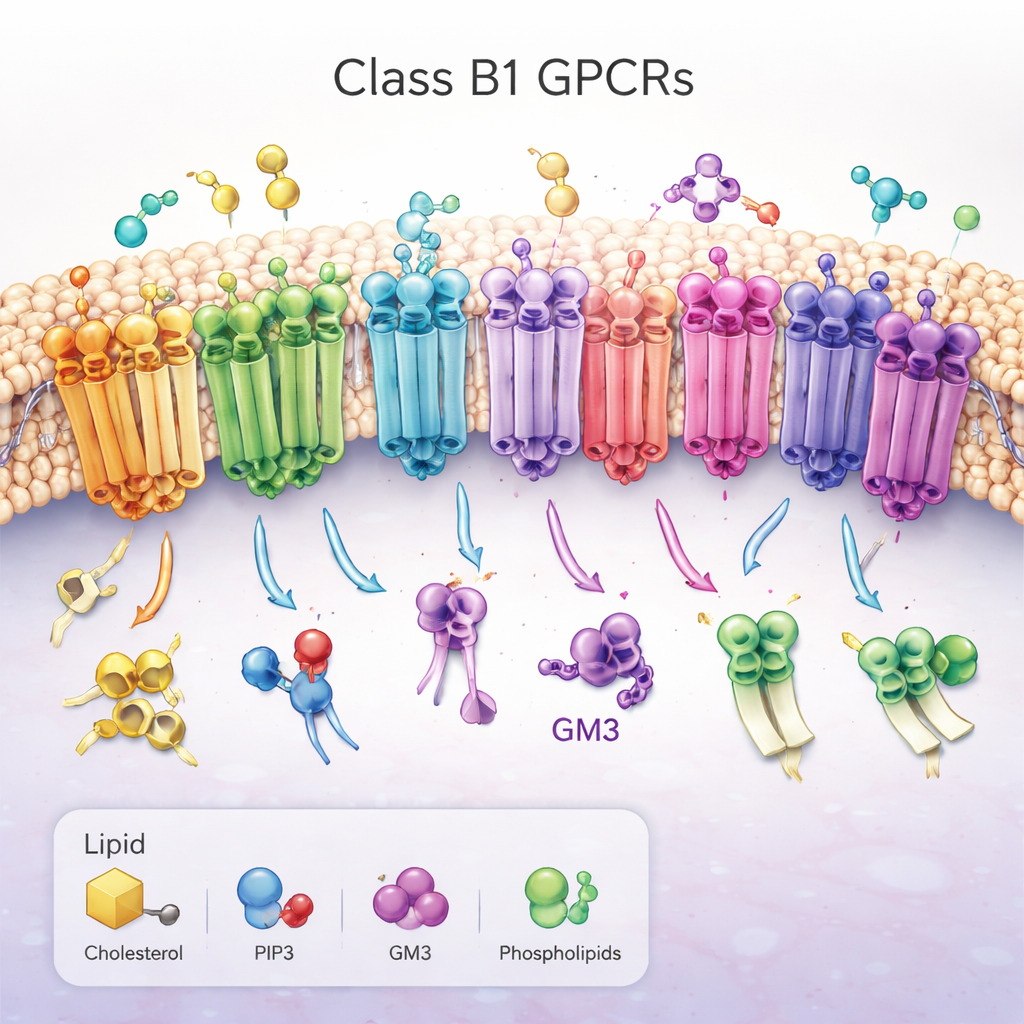
一类重要的分子天线
工作聚焦于B1类G蛋白偶联受体(GPCRs),这是一组由15个密切相关的受体组成的家族,参与调控血糖、代谢、发育和应激反应。它们横跨细胞外膜,细胞外有一个较大的“头部”用于抓取类激素分子,穿膜部分由七个螺旋束组成。当激活时,这些受体在细胞内侧改变构象,打开一个沟槽以招募配对蛋白并触发信号级联。由于它们在糖尿病和肥胖等疾病中的核心作用,B1类GPCR是重要的药物靶点,但周围膜脂如何调控它们长期以来仍不清楚。
在天然环境中模拟受体
研究者没有在人工的去污剂泡中研究受体,而是将全部15个人类B1类GPCR置入计算构建的膜中,以模拟真实细胞中复杂的脂质混合物。利用一种称为粗粒化分子动力学的技术,他们对每种受体的活性和非活性状态进行了多次长时间模拟,总计约一毫秒的模拟时间。他们跟踪了三种“调节性”脂质——胆固醇、信号脂PIP2和带糖基的脂质GM3——如何接近、结合并解离每个受体的不同区域。为确保他人可复现并在这一庞大数据集上继续工作,他们使用名为 aiida-gromacs 的开放工作流工具记录了每一步的设置和分析,并将基于物理的结果与一个新AI模型(Chai‑1)对蛋白与小分子结合预测的结果进行了比较。
隐蔽口袋与保守的脂质把握
模拟揭示了在整个受体家族中反复出现的结合模式。众所周知的胆固醇不仅被观察到停驻在某一已知的螺旋位点,还进入螺旋之间的“深膜”口袋,其极性头部异常地深埋入膜内。分泌素受体在其活性和非活性构象中显示出尤其长寿命的胆固醇结合,提示胆固醇可能强烈偏向其信号传导方式。PIP2表现出引人注目的保守行为:它在受体的内侧面聚集,位于两段螺旋与一段短尾部(TM6、TM7 和 H8)的连接处,尤其在受体处于活性状态时。在该位点,一系列带正电的氨基酸抓住带负电的PIP2头基,提示这种脂质可能通过稳定活性构象或帮助在细胞内招募信号配对蛋白来发挥作用。
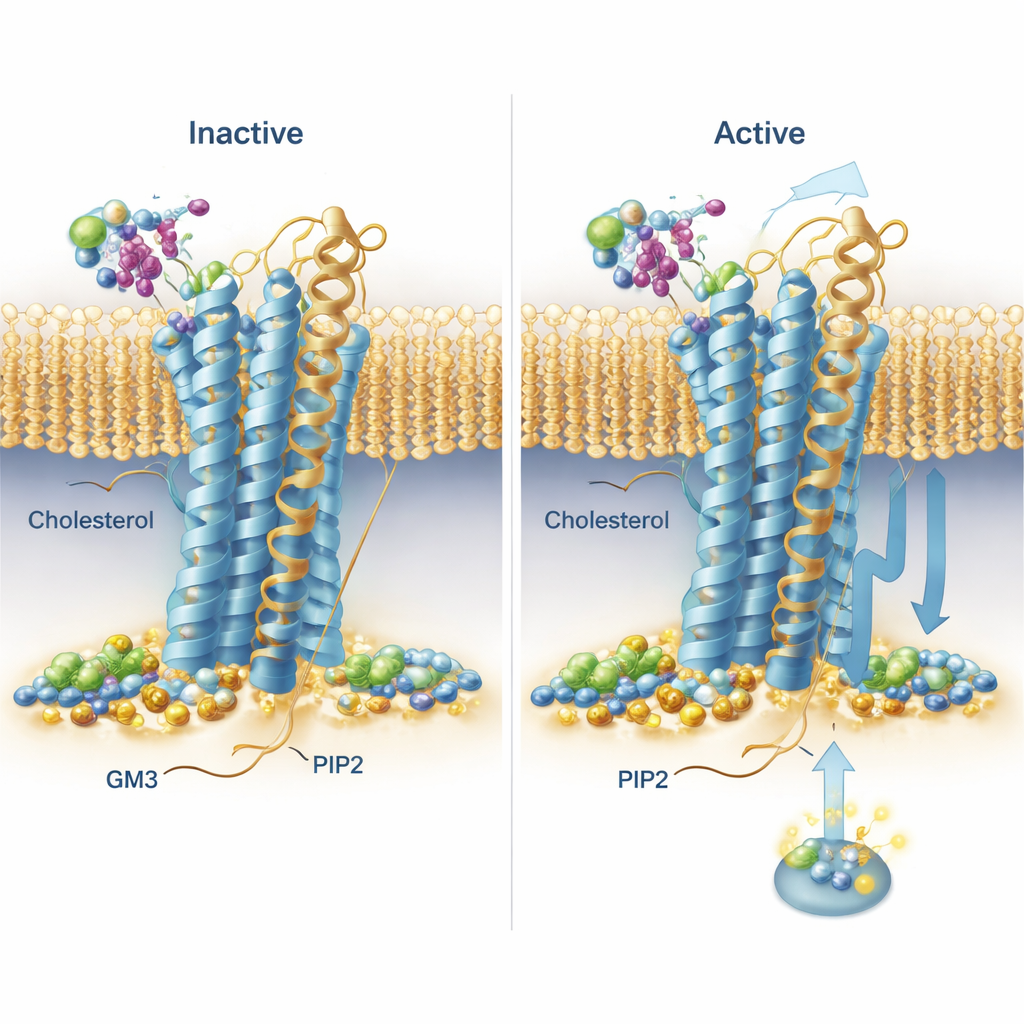
一种带糖的脂质推动受体运动
GM3是一种带糖头基的复杂脂质,主要与受体较大的外侧头部相互作用。团队注意到一些受体的外部结构相对于膜明显摆动和弯曲较多,而另一些则更受限。针对两个与药物相关的受体——GLP‑1R 和 GIPR——他们详细考察了GM3的作用。在含GM3的模拟中,该脂质要么贴靠在外部结构底部和配体结合口袋附近(GLP‑1R),要么抓住外部结构的远端(GIPR),在两种情况下都影响这些结构的运动自由度。为在活细胞中检验这些预测,研究者使用了一种基于光的技术(TR‑FRET),用于报告带标记的受体头部与膜的接近程度。当他们用小分子抑制剂降低GM3水平时,观察到受体头部在刺激下位移的可测变化,整体上支持GM3以受体和状态特异的方式调节受体柔性的观点。
这些脂质—受体伙伴关系为何重要
综述来看,该研究将B1类GPCR描绘为不仅仅是激素开关,而是与周围脂质紧密编排舞动的一部分。胆固醇可以占据隐蔽口袋,细微地偏向某些信号输出;PIP2 形成保守的内侧“把手”,可能将受体锁定为活性构象并引导配对蛋白;GM3 则调整受体外部区域的运动方式和配体相遇。对非专业读者来说,关键信息是膜是一个主动的调节层:脂质组成的细微差异可能改变同一受体在不同组织或疾病状态下的行为。通过详尽绘制这些相互作用并共享基础模拟数据,这项工作为未来设计利用或回避特定脂质接触的药物奠定了基础,或可使治疗更具选择性与有效性。
引用: Chao, K.W., Wong, L., Oqua, A.I. et al. Human class B1 GPCR modulation by plasma membrane lipids. Commun Biol 9, 317 (2026). https://doi.org/10.1038/s42003-025-09445-2
关键词: G 蛋白偶联受体, 膜脂质, 胆固醇, PIP2, GM3