Clear Sky Science · zh
通过多模态人工智能解码 ERS–CAF 免疫调节轴及其泛癌预后与治疗预测价值
无需手术刀也能洞察肿瘤
肿瘤医生越来越认识到,包围肿瘤的环境可能与肿瘤本身同样重要。但反复通过活检取样来观察这一隐匿的“邻里”既具侵入性又常常不现实。本研究展示了人工智能(AI)如何解读常规医学扫描和显微镜图像,以推断肿瘤内部难以直接测量的免疫与瘢痕样过程,可能将日常影像转变为一种可跨癌种使用的“数字活检”。
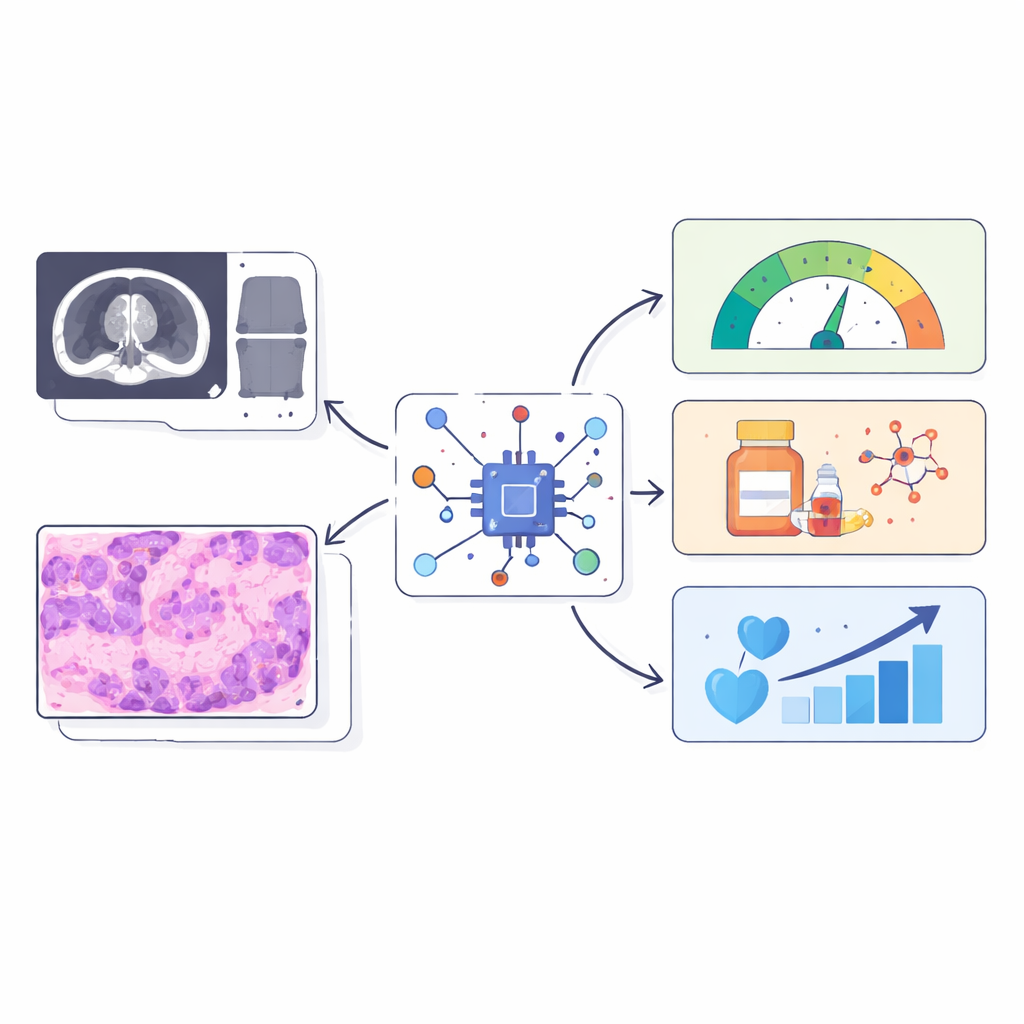
塑造癌症的隐秘支持细胞
许多实体瘤被专门的支持细胞——成纤维细胞制造的坚韧纤维外壳所包裹。当这些细胞在内质网(细胞的蛋白质工厂)内处于压力状态时,它们会进入一种具有促癌性的激活状态。在脊索瘤(一种罕见的骨癌)中,这些受压的成纤维细胞会构建致密基质并阻挡免疫细胞进入,使治疗效果下降。胰腺癌和结直肠癌等其他癌种也会出现类似的纤维化、免疫稀缺的环境,表明这种生物学并非单一疾病所独有。挑战在于,当前测量这些受压成纤维细胞及其免疫阻隔行为的方法依赖组织样本和复杂的分子检测,难以重复并可能错过肿瘤的重要区域。
教会 AI 识别不可见的生物学特征
研究团队探问常规术前磁共振(MRI)和常规 H&E 病理切片中是否已包含关于这种受压成纤维细胞免疫屏障的视觉线索。他们从肿瘤的 RNA 测序中构建了三个数值型“参考评分”:一个反映成纤维细胞应激程序的活跃程度,一个概括这些细胞与免疫细胞之间信号交流的强度,另一个描述周围免疫与支持细胞群体的多样性。与其去预测数千个基因,AI 被训练仅从图像预测这三个具有生物学意义的评分。为此,团队结合了两条分支:一条分析 MRI 的纹理与形态特征,另一条扫描数千个数字切片的小区域,并使用语言引导的注意力机制聚焦于与专家描述的纤维化、免疫稀缺组织相匹配的区域。
融合扫描与切片以获得更强信号
在 126 例同时具有配对 MRI、病理切片、RNA 数据和随访信息的脊索瘤患者中,融合的多模态 AI 模型优于仅使用 MRI 或仅使用切片的模型。其对三个分子评分的预测与 RNA 基于测量高度一致,并在不同医院和扫描仪之间保持良好校准。当病理学家独立标注纤维化和免疫被排斥的区域时,AI 的“热点”往往在相同区域被点亮,表明它在追踪真实的生物学特征而不仅仅是肿瘤大小。该模型还捕捉到了预后信息:更高的预测应激‑成纤维细胞和信号评分与更差的生存相关,而更高的微环境多样性预测则具有部分保护作用。将这些 AI 导出的评分加入常规临床因素后,提高了随时间区分高危与低危患者的能力。
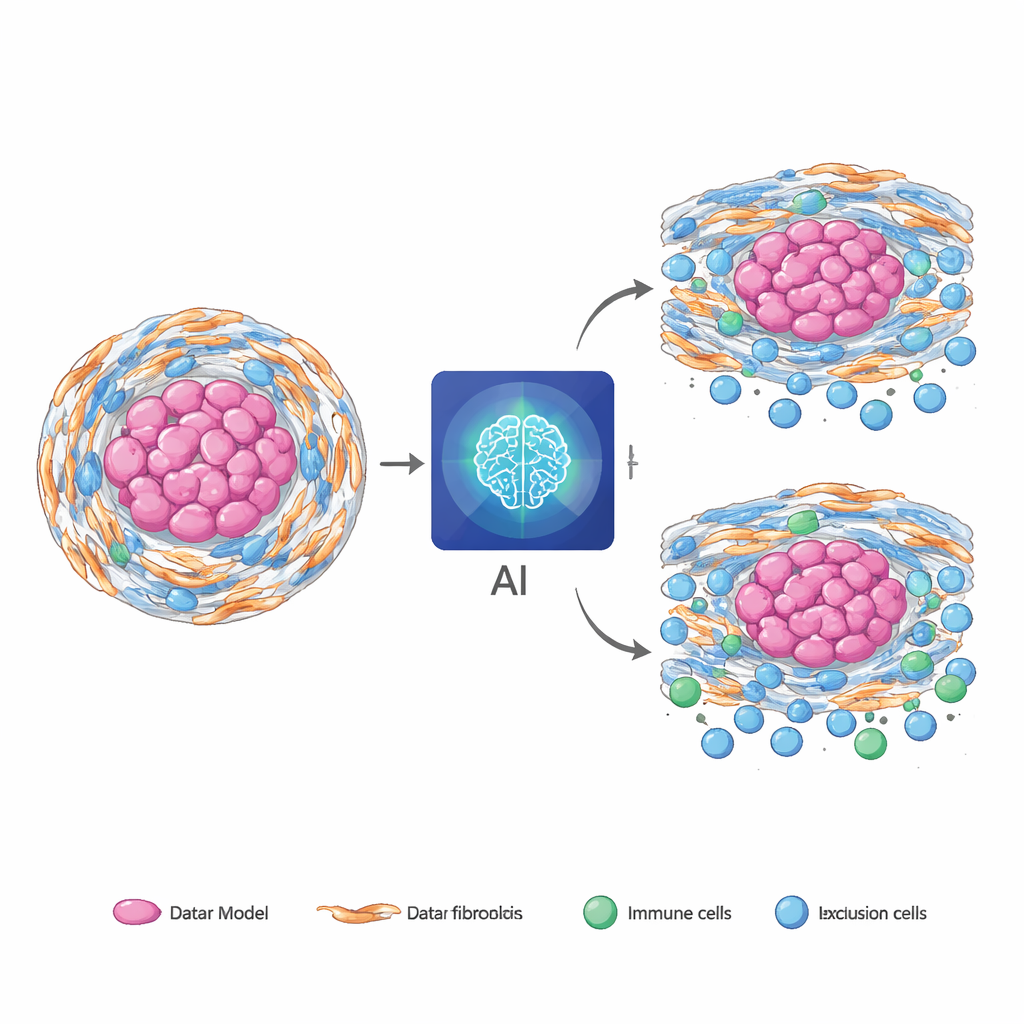
从罕见肿瘤到常见癌种的推广
一个关键测试是,完全在脊索瘤上训练的模型是否可以“原样”用于其他更常见的癌种。将该模型在未重新训练的情况下应用于来自大型公共数据集的胰腺、胃和结直肠肿瘤时,仅切片版本仍然显示其基于影像的预测与重新计算的 RNA‑基于评分之间具有有意义的一致性。在部分癌种中,AI 评分在标准临床信息之外提升了对患者生存的预测,并有助于区分哪些患者更可能从化疗中获益。为便于在数字病理受限的环境中部署,该团队还将完整的多模态模型蒸馏为仅 MRI 的版本,保留了大部分预测能力同时运行更快、计算资源占用更少。
这对患者可能意味着什么
综合来看,结果支持这样一个观点:常规医学影像悄然编码了有关受压支持细胞、免疫排斥和微环境多样性的信息——这些特征通常需要昂贵的分子检测才能获得。尽管当前工作是回顾性且需要前瞻性验证,但它指向一个未来:通过一次标准扫描和切片即可非侵入性地提示具有敌意纤维化免疫屏障的肿瘤,指导哪些患者可能需要额外检测或个体化治疗,并在不增加患者负担的前提下覆盖多种癌症类型。
引用: Zheng, BW., Xia, C., Tang, M. et al. Decoding the ERS–CAF immunoregulatory axis via multimodal AI and its pan-cancer prognostic and therapeutic predictive value. npj Digit. Med. 9, 199 (2026). https://doi.org/10.1038/s41746-026-02388-w
关键词: 肿瘤微环境, 癌症影像, 人工智能, 成纤维细胞, 免疫治疗