Clear Sky Science · zh
DARE-FUSE:面向联合脑肿瘤 MRI 分割与分类的领域对齐证据引导学习
为什么更智能的大脑成像很重要
脑肿瘤是医学中最令人害怕的诊断之一,磁共振成像(MRI)是医生用来判断肿瘤起止范围的主要工具。然而,即便是资深放射科医生,有时也难以精确描绘肿瘤边界并判断其随时间的变化,尤其当肿瘤边缘与水肿脑组织模糊相连时。本文提出了 DARE-FUSE,一种新的人工智能系统,旨在更可靠地解读脑部 MRI 扫描,画出更清晰的肿瘤边界并为其决策提供更明确的解释,以支持外科医生、肿瘤科医生和患者。
模糊的边界与繁忙的诊室
在真实医院环境中,脑部 MRI 扫描往往杂乱无章。肿瘤常常与周围水肿融合,金属植入物会使图像失真,不同医院使用的扫描参数也略有差异。放射科医生需要手动翻阅数百张切片,一片片标注肿瘤,然后判断其变化情况。该工作既耗时又令人疲惫,而且不同专家之间常有分歧。现有的人工智能工具可帮助勾勒肿瘤或将影像标注为“有肿瘤”或“无肿瘤”,但大多数系统将这些任务分开处理,并且在图像来自新中心或肿瘤边缘出现细微、不规则生长时,性能往往下降。
用于肿瘤分割与分类的统一 AI 助手
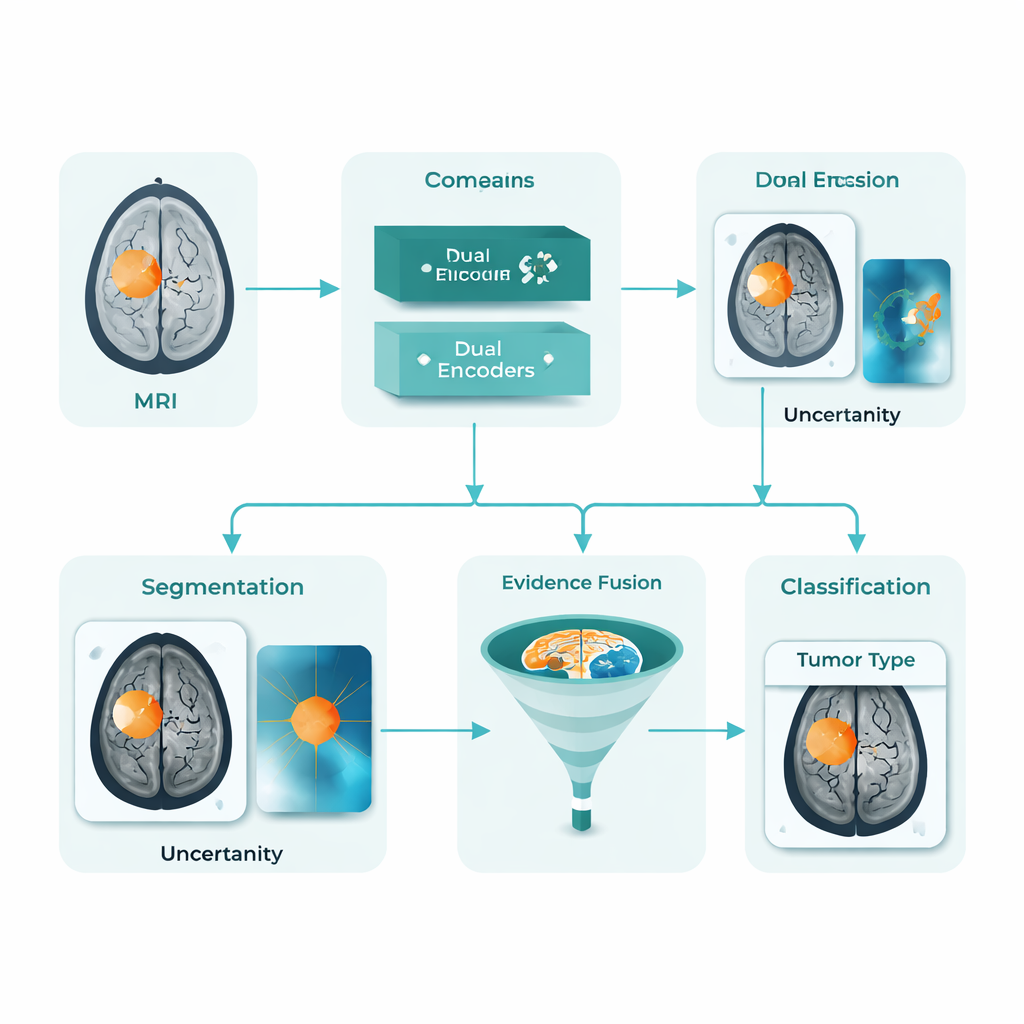
DARE-FUSE 同时应对以上多个挑战。它构建为一个单一流程,既在每个 MRI 切片上描绘肿瘤(分割),又将整张影像分类到诊断组别(分类)。系统核心由两种协同的“视角”组成:一个网络专注于细节形状与边界,另一个网络关注区分不同肿瘤类型的整体模式。一个专门的对齐模块使这些视角在不同医院和扫描仪间保持一致,从而避免从一个数据集学到的特征损害在另一处的表现。系统还会评估自身的不确定性,本质上标注出其对具体肿瘤轮廓不太确定的区域,这对于安全的临床应用至关重要。
来自热图与“无肿瘤”重建的线索
DARE-FUSE 不依赖单一信号,而是从多种证据中学习。一个分支生成热图,显示哪些脑区对 AI 的分类决策贡献最大;另一个分支使用生成模型想象如果去除肿瘤后同一扫描会是什么样子,然后将该“无肿瘤”版本与原图比较。两者的差异能强调那些在标准热图上可能不明显的微妙结构变化与边缘。一个融合模块随后将这些线索合成为连续的“肿瘤先验”地图:多个来源一致的区域被视为核心肿瘤,而不太确定的区域则更谨慎地被加入,并在模型不确定性高时被降权。这一混合先验指导最终的轮廓,帮助避免既漏检肿瘤小窝又产生健康组织中的伪岛。
在公开脑肿瘤数据集上的验证成果
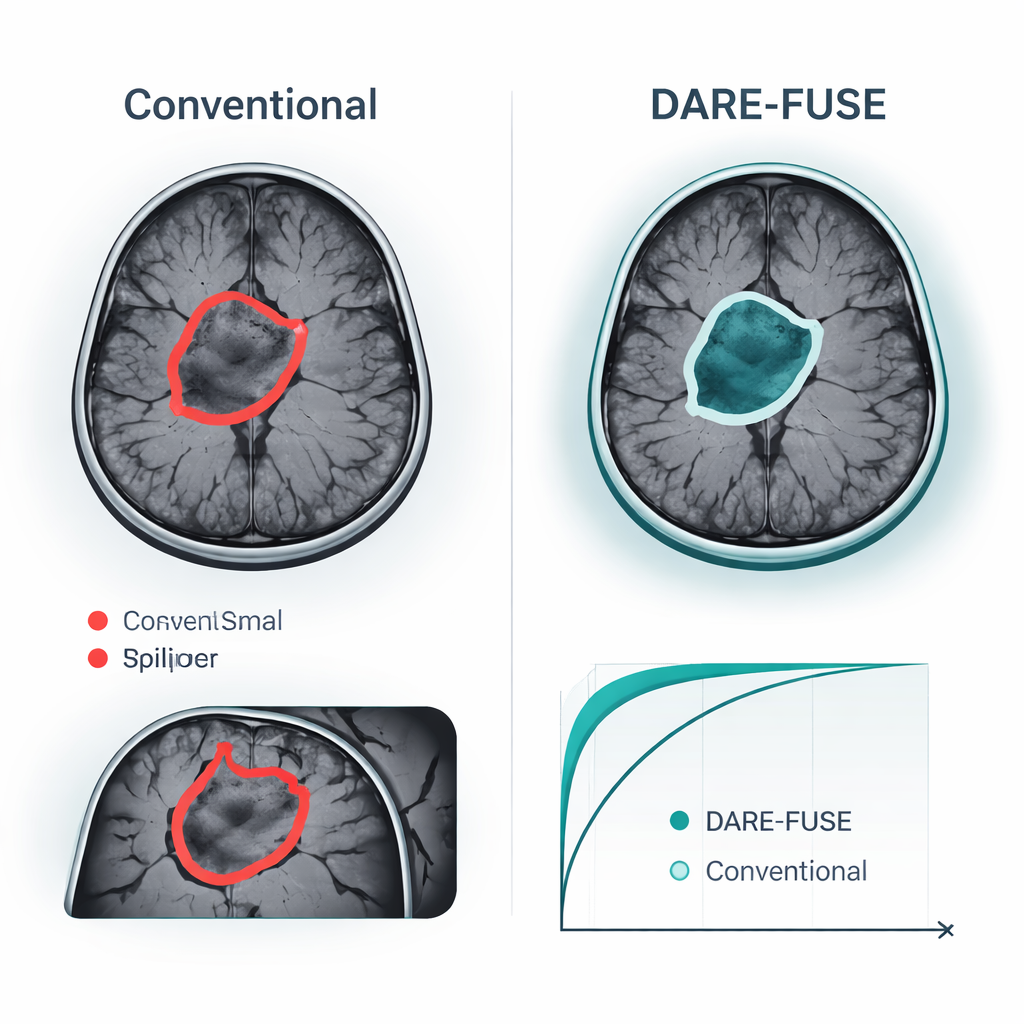
作者在六个大型多中心脑肿瘤挑战(BraTS 系列)以及四个用于影像级分类的公开 MRI 集合上测试了 DARE-FUSE。在所有 BraTS 版本中,该系统与近期顶尖深度学习模型不相上下或超过它们,实现了其预测的肿瘤掩码与专家标注之间略高的重叠度,并且在肿瘤表面测量误差上持续更小。此类改进在困难病例中最为显著:小肿瘤、低对比度边缘和复杂不规则形状。在分类任务上——例如判断扫描是胶质瘤、脑膜瘤、垂体肿瘤还是无肿瘤——DARE-FUSE 在准确率和常用判别度量(AUC)上也略胜强大的 Transformer 基线和弱监督基线。重要的是,当研究者人为减少详细标注数量时,该新系统退化更为平缓,仍保持相对于半监督和弱监督竞争方法的优势。
这对患者可能意味着什么
对患者和临床医生而言,DARE-FUSE 的主要承诺不是一个花哨的新算法,而是更可靠、可解释的影像辅助。在实践中,该系统可以建议肿瘤轮廓、标注其不太自信的区域,并显示解释其分类决策的热图。医生可以将低不确定性的区域作为起始轮廓,然后将注意力集中在已标注的疑点上,而不是从头重画全部切片。更准确且一致的肿瘤体积与形状测量可改善治疗规划、放疗靶区定位以及随时间的疗效跟踪。作者强调该工具是对专家判断的辅助——而非替代——但他们的结果指向了这样一种可能性:AI 系统既能更清晰地“看见”肿瘤,也能以临床可操作的方式传达其置信度。
引用: Liu, Y., Sun, C., Niu, Y. et al. DARE-FUSE: domain aligned evidence guided learning for joint brain tumor MRI segmentation and classification. npj Digit. Med. 9, 178 (2026). https://doi.org/10.1038/s41746-026-02365-3
关键词: 脑肿瘤 MRI, 医学图像分割, 放射学中的深度学习, 临床决策支持, 不确定性感知的人工智能