Clear Sky Science · zh
整合多组学和机器学习系统性解析从MASLD到MASH进展中的细胞异质性与纤维化调控网络
为什么这项肝病研究很重要
与肥胖和2型糖尿病相关的脂肪肝已成为全球最常见的肝脏问题之一。对许多人而言,这种情况保持轻度,但在相当一部分人中,它会悄然恶化为伴有炎症和瘢痕形成的侵袭性形式,最终可能导致肝硬化和肝癌。临床上仍难以预测谁会进展,也难以在无需活检的情况下早期发现这一危险阶段。本研究利用前沿的“多组学”工具和人工智能,聚焦单个肝细胞,揭示出一种新识别的免疫细胞类型及其信号通路,可能驱动有害瘢痕形成,并提出可通过血液检测将来无创识别高风险患者的潜在标志物。

从简单脂肪堆积到危险的肝损伤
研究者聚焦于代谢功能障碍相关脂肪性肝病(MASLD,常称脂肪肝)向其更严重的同类代谢功能障碍相关脂肪性肝炎(MASH)的转变。MASLD 非常普遍,全球超过三分之一的成年人受其影响,尤其常见于肥胖或糖尿病患者。大多数MASLD患者肝内有脂肪堆积但损伤较少。然而在MASH中,肝细胞受损、炎症增加并形成瘢痕组织。约五分之一到三分之一的MASH患者最终会发展为肝硬化或肝癌。现有的血液检测和影像检查无法准确识别器官内正在发生的这些微观细胞变化,因此常常错过早期干预的时机。
逐细胞观察肝脏
为了解决这一问题,研究团队整合了来自公开研究的多种强大数据类型。他们汇集了超过半百万个肝细胞的单细胞RNA测序数据、保留细胞在组织中位置信息的空间转录组学、来自整块活检的整体基因表达谱,以及显示哪些DNA区域开放活跃的染色质可及性图谱。借助复杂的软件,他们将细胞分为七大类,包括肝细胞、免疫细胞和称为肝星状细胞的支持性细胞。随后他们比较了健康肝脏、MASLD以及早期和晚期MASH,绘制出随着疾病恶化细胞组成及其通信网络如何变化的图谱。
驱动瘢痕的免疫细胞与支持细胞协同作用
研究揭示了一个显著模式:被称为单核细胞和巨噬细胞的免疫细胞与肝星状细胞在MASH中比早期阶段更为丰富,并且倾向于在病变组织的同一区域聚集。进一步分析中,科学家将星状细胞细分为五个亚型,范围从静息状态到完全激活、呈平滑肌样的形式。随着肝脏从MASLD转向MASH,静息星状细胞减少,而产瘢痕的激活型星状细胞增加,描绘出从静息到纤维化状态的清晰路径。空间分析显示这些激活的星状细胞与富集的巨噬细胞相邻,提示二者在构建肝脏瘢痕方面存在密切协作。
新发现的一种巨噬细胞类型与纤维化信号轴
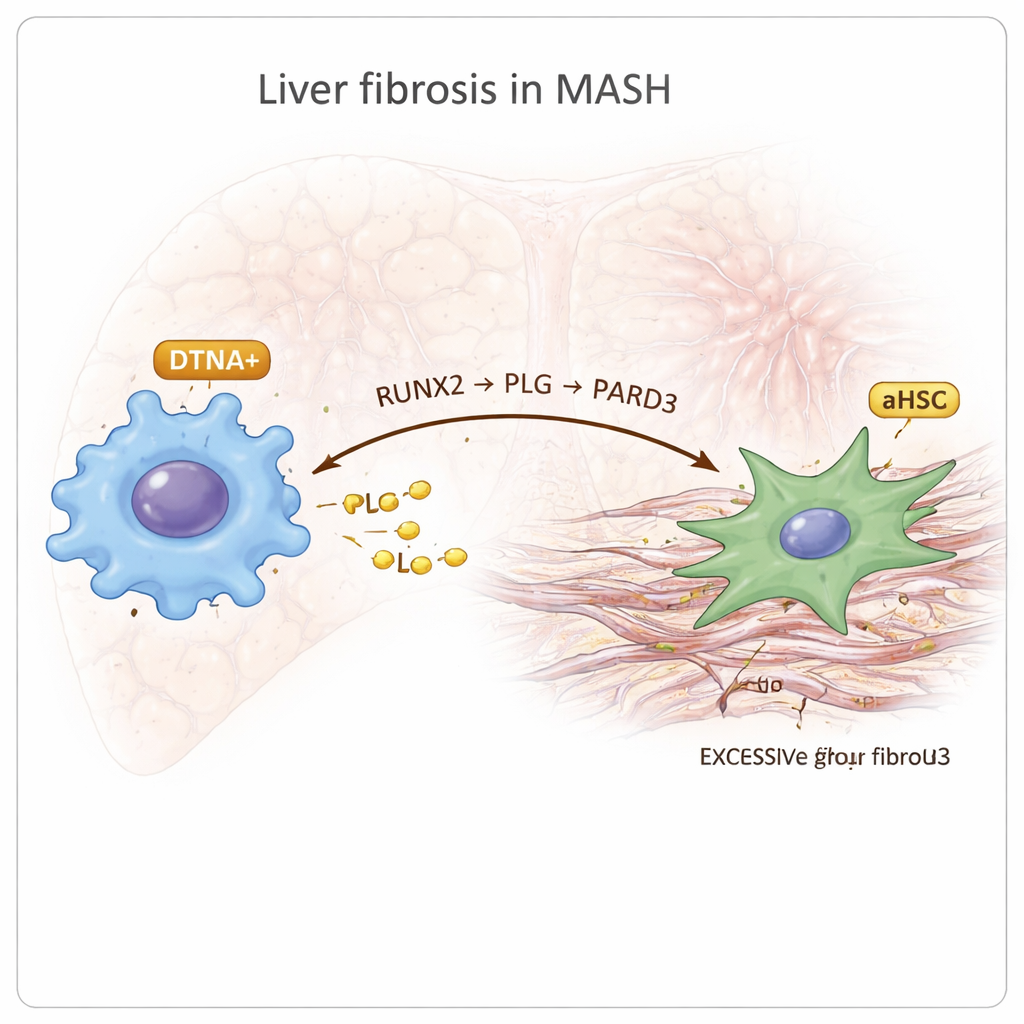
在免疫细胞中,研究者发现了一类以基因DTNA为标记的独特巨噬细胞亚群,这类细胞在MASH中特异性富集。这些DTNA阳性巨噬细胞表现出所谓M2极化的特征,M2常与慢性炎症和组织重塑相关,伴随低氧迹象和强烈的炎症信号。通过重建细胞发育“轨迹”,他们推测这些细胞来源于肝脏的固有库普弗细胞。调控网络分析指向转录因子RUNX2为这些巨噬细胞的主控开关。进一步的细胞间通信映射表明,DTNA阳性巨噬细胞通过一条被称为RUNX2–PLG–PARD3的链与激活的星状细胞对话:RUNX2在巨噬细胞中提升蛋白PLG的产生,PLG随后作用于表达PARD3的星状细胞,这一相互作用与更强烈的纤维化和改变的凝血活性相关。
从细胞图谱到潜在检测与治疗手段
为评估这些发现是否对患者有帮助,团队在来自MASLD和MASH患者的大型整体基因表达数据集上训练并测试了113种不同的机器学习模型。弹性网(Elastic Net)模型表现最佳,在多个独立队列中,有一个基因脱颖而出成为最强的预测因子:DTNA。DTNA及其相关基因(包括RUNX2)的更高表达,一致性地标识出MASH患者而非单纯脂肪肝患者。作者还筛查了现有的药物数据库,发现若干药物可能作用于新描述的RUNX2–PLG–PARD3通路,提示有药物再利用的可能,尽管这些想法仍需实验室和临床验证。
对脂肪肝患者意味着什么
从日常角度看,这项研究表明并非所有的肝脏免疫细胞和支持细胞都相同,且一种新强调的巨噬细胞亚型与产瘢痕的星状细胞之间的特定合作可能是推动脂肪肝走向危险性瘢痕化的关键动力。研究表明,检测如DTNA之类的标志物(在血液或组织中)将来可能帮助医生在无需依赖侵入性活检的情况下识别出最有可能进展为MASH的脂肪肝患者。它还将RUNX2–PLG–PARD3这一特定信号通路作为潜在药物靶点,以期减缓或逆转肝纤维化。尽管这些发现仍处于研究阶段并需进一步验证,但它们为将复杂的细胞数据转化为早期诊断与靶向治疗的实际工具提供了更清晰的路线图。
引用: Wen, W., Liu, Z., Tan, W. et al. Integrating multi-omics and machine learning systematically deciphers cellular heterogeneity and fibrotic regulatory networks in the progression from MASLD to MASH. npj Digit. Med. 9, 167 (2026). https://doi.org/10.1038/s41746-026-02352-8
关键词: 脂肪肝疾病, MASH, 巨噬细胞, 肝纤维化, 多组学