Clear Sky Science · zh
掩码自编码、可泛化预训练与集成专家以增强胶质瘤分割
为什么更智能的扫描对脑肿瘤很重要
被称为胶质瘤的脑肿瘤是最致命的癌症之一,但医生仍需花大量时间在MRI影像上手工描绘肿瘤边界。这样的精细勾画指导外科和放疗,但每例患者可能需15–20分钟,而且需要随时间重复。研究提出了MAGPIE,一种从数万张无标注脑部影像中学习的人工智能系统,然后仅需少量专家标注案例就能可靠地绘制出胶质瘤轮廓。对患者而言,这可能意味着更快、更一致的治疗规划,甚至在缺乏大型、精心整理数据集的医院也能实现。
以新方式“看”到肿瘤
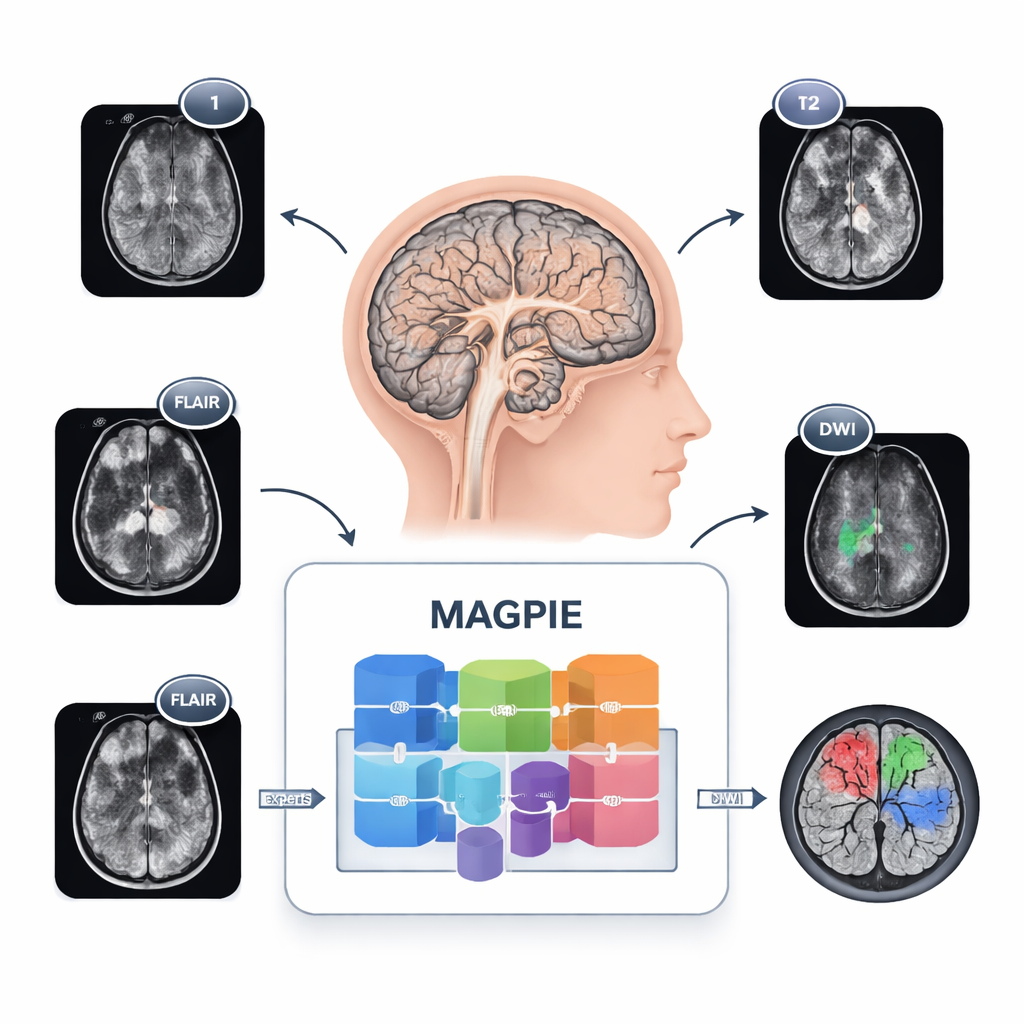
胶质瘤难以描绘,因为它们并不形成整齐的球体。癌细胞沿脑部纤维扩散,形成模糊的边缘和难以察觉的小卫星灶。不同医院使用不同的MRI设置和序列组合,因此在某处训练的工具在另一处可能表现不佳。MAGPIE同时应对了这些挑战。它首先接触了来自多项研究和多种扫描仪类型的43,505张无标注脑部MRI影像。在此阶段,它通过尝试重建图像中缺失的部分并比较同一脑部的不同增强视图,学会了健康与病变脑组织的一般模式,迫使模型关注稳定且有意义的特征,而非脆弱的像素细节。
让多个专家分担工作
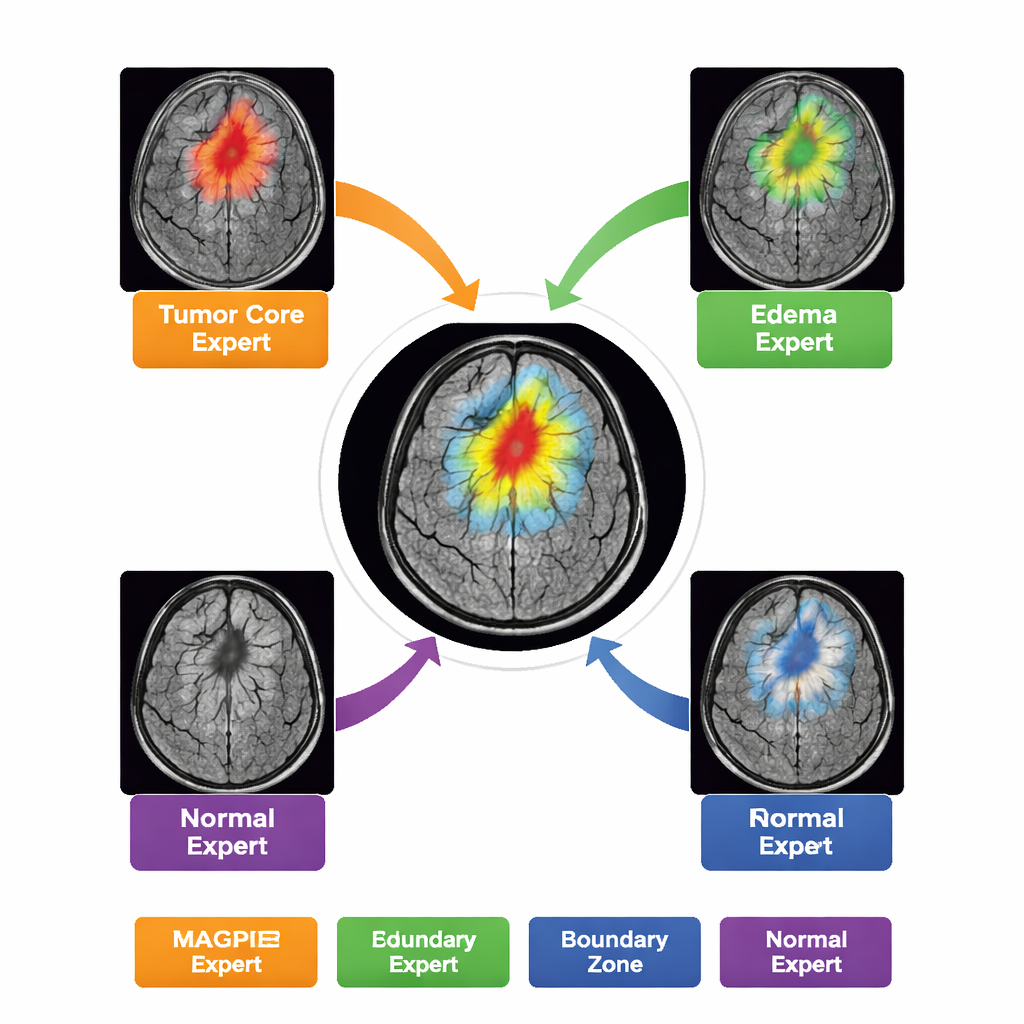
MAGPIE并非作为单一整体模型运行,而是内含一种“专家混合”结构。当分析新影像时,它仅为图像的每个区域激活八个专门子网络中的一小部分。随着训练进行,这些专家自然分工:有的对肿瘤明亮、活动性生长的边缘敏感;有的锁定坏死的肿瘤核心;有的学习肿瘤周围的模糊水肿环;还有的主要关注正常脑组织和边界。作者通过测量每个专家的激活与放射科医师标注的不同肿瘤区域的重叠程度来展示这一点。这种分工在保持计算可控的同时提高了准确性——对于任一图像补丁,约只有一半的模型参数处于激活状态。
应对杂乱的真实世界扫描
临床MRI协议差异很大。有些患者有四个序列,另一些则更少;不同厂商的机器会产生细微不同的图像。MAGPIE的设计将每个MRI序列视为独立的“令牌”,并在运行时学习给每个序列分配多少权重,而不是期望固定顺序和固定输入集合。这种通道不可知的方式意味着系统可以自适应,例如在对比增强序列缺失但FLAIR可用的情况下仍能工作。模型还使用了先进的注意力机制,使其既能“看得远”,捕捉沿白质束的远距离扩散,也能“看得准”,发现仅几毫米大小的微小病灶。
用极少标注做更多工作
在预训练后,研究人员仅用20例完全标注的胶质瘤病例对MAGPIE进行微调,并在相同条件下将其与从头训练的标准模型比较。在一个主要的脑肿瘤基准(BraTS21)上,MAGPIE取得了约61%的Dice分数——这一医学影像中常用的重叠度量——比表现最好的从零开始训练版本高出约2.6个百分点,并且在与先前强大的自监督方法比较时没有出现有害的“负迁移”。在具有挑战性的分布外数据集(来自不同疾病、不同扫描仪类型和不同成像设置的扫描)上,它也表现更稳健:在一个白质病灶数据集上无需额外微调就超过了70%的Dice。关键是,通常达到此类表现大约需要400例标注病例;MAGPIE仅用约5%的标注量就能实现相当水平。
这对患者和临床的可能意义
对非专家而言,核心信息是MAGPIE能把大量无标注的MRI影像变成一个强大的助手,只需极少的专家训练即可具备临床价值。它能够以逼真的边界描绘复杂脑肿瘤,检测其他系统可能漏掉的小卫星灶,并在影像来自陌生机器或缺少某些序列时仍保持可靠。这种组合可能将放射科医师的标注时间减少约95%,降低小型医院部署先进成像AI的门槛,并支持更精确的外科和放疗规划。虽然仍需对罕见肿瘤类型和低级别病例进行更多验证,但这项研究展示了精心设计的自监督学习如何使稳健且数据高效的脑肿瘤分割更接近日常临床应用。
引用: Xie, M., Xiao, Q., Wu, H. et al. Masked autoencoding, generalizable pretraining, and integrated experts for enhanced glioma segmentation. npj Digit. Med. 9, 163 (2026). https://doi.org/10.1038/s41746-026-02347-5
关键词: 胶质瘤分割, 脑部磁共振成像, 自监督学习, 专家混合模型, 医学成像人工智能