Clear Sky Science · zh
定量化组织和血浆HER2分析可预测曲妥珠单抗艾美妥(trastuzumab deruxtecan)对乳腺癌的疗效
这项研究对患者的重要性
对于患有转移性乳腺癌的人来说,新药带来希望——但并非对所有人都同样有效。本研究提出了一个实用问题:我们能否更好地预测谁会从一种广泛使用的靶向药物曲妥珠单抗艾美妥(通常缩写为 T-DXd)中受益最多且持续时间最长?通过对肿瘤样本和血液进行更精细、更精确的检测,研究者表明对一种称为 HER2 的分子以及某些 DNA 和蛋白标志物进行细致测量,可以揭示哪些癌症最有可能对该疗法产生反应。
一种疗效不均的靶向药物
T-DXd 属于“抗体-药物偶联物”,类似一枚制导导弹,定位表达 HER2 蛋白的细胞并将类化疗药物的有效载荷直接递送到细胞内部。它最初用于 HER2 水平非常高的肿瘤,但现在已获批用于近九成的转移性乳腺癌患者,包括那些按常规检测被判定为 HER2 低表达或甚至无表达的患者。然而在临床实践中,部分患者在 T-DXd 治疗下可以获得长期的疾病控制,而另一些患者的肿瘤仅在几个月后就出现进展。传统的实验室方法将肿瘤分为 HER2 阳性、HER2 低或 HER2 零类别,但对此类差异的解释能力有限。
追踪肿瘤随时间的变化
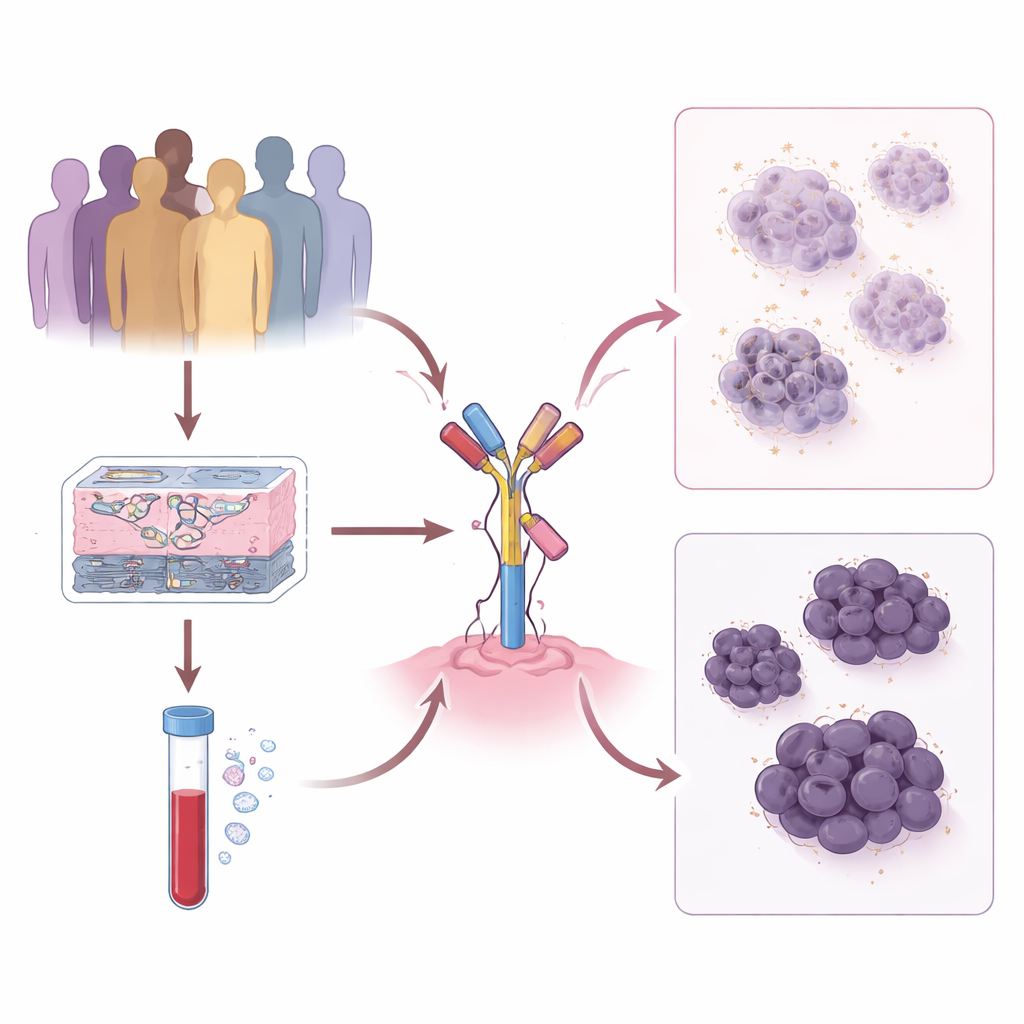
研究团队回顾性分析了两家美国大型癌症中心接受 T-DXd 治疗的 191 名患者,审视肿瘤的临床行为以及从原发肿瘤到后期转移灶中 HER2 水平的变化。他们发现,简单的一次性标注(如 HER2 低或 HER2 零)忽略了重要的动态变化。那些持续明显为 HER2 阳性的患者在 T-DXd 治疗下生存期最长,其次是那些肿瘤持续显示低但稳定 HER2 水平的患者。相比之下,当 HER2 随时间在低表达与零表达之间转换时,从 T-DXd 获得的益处明显较短。这些模式提示,肿瘤对 HER2 的依赖性越稳定,药物效果可能越好。
用更精细的“尺子”测量 HER2
为超越粗略分类,研究者对肿瘤组织应用了一系列现代化检测。一种方法使用定量免疫荧光精确计数 HER2 蛋白;另一种使用高通量蛋白芯片;第三种测读与 HER2 基因组区域相关的基因表达谱。三种方法的结论一致:较高的定量 HER2 水平——无论是作为细胞表面的蛋白、被激活(磷酸化)的形式,还是信使 RNA 水平——都与延长下次治疗前的间隔时间和更好的总体生存期相关。在相同的患者中,常规病理学读数(HER2 阳性、低或零)几乎不能区分结局,这突显出“HER2 有多少”比勾选哪个分类更为重要。
来自血液检测和其他肿瘤标志物的线索
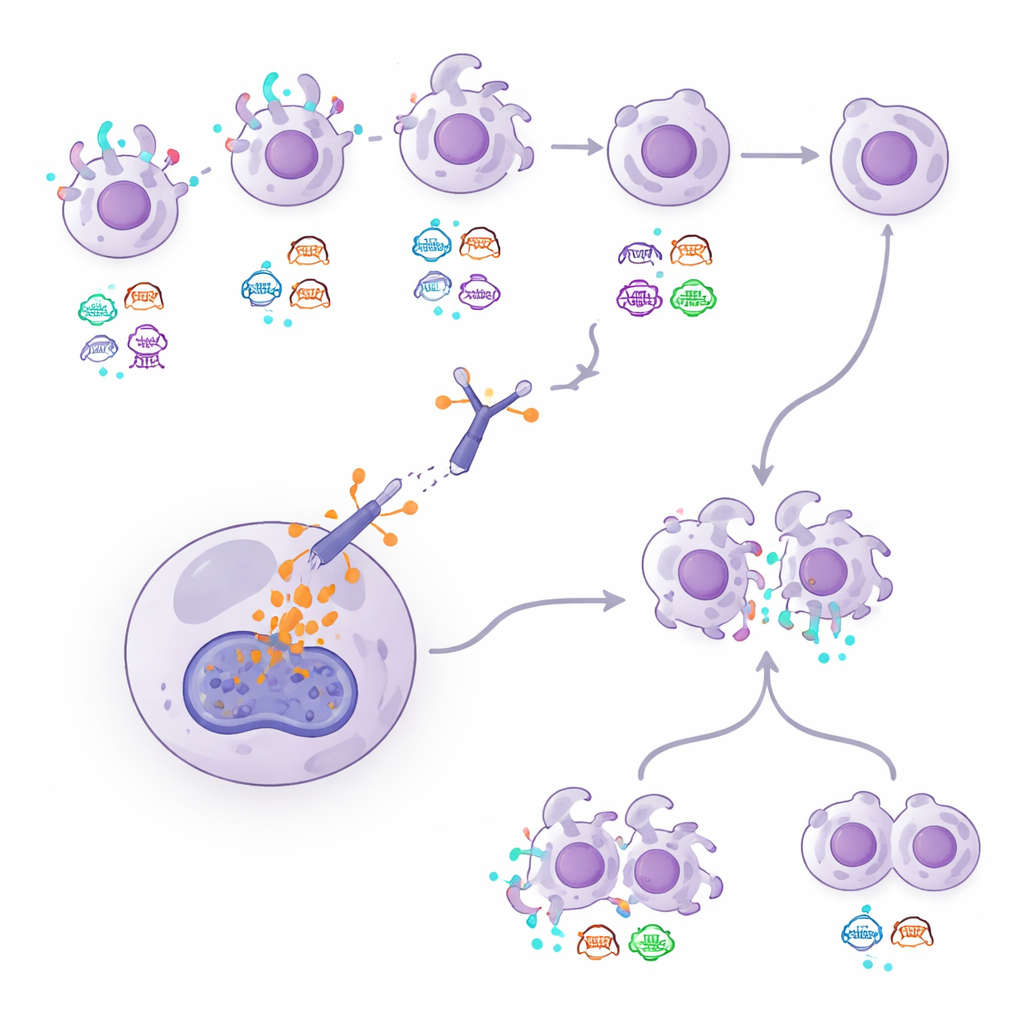
由于反复活检具有侵入性,研究还测试了一种基于血液的方法,分析循环血液中肿瘤 DNA 的片段。研究者使用一种称为 DNADX 的方法,将患者的血样分为生物学簇并计算与 HER2 相关的 DNA 签名。血液中 HER2 信号较强的患者倾向于在 T-DXd 治疗下停留更久,而呈现与更具侵袭性、快速生长疾病相关的 DNA 模式的患者预后较差。研究者还注意到,在被标注为 HER2 阴性的肿瘤中,细胞内一种名为拓扑异构酶 1(topoisomerase 1)的蛋白水平较高与较差结局相关,这提示药物载荷在细胞内的处理方式可能影响疗效。某些基因的缺失或突变,例如 ERBB2 与 TP53 的改变,以及治疗后 ARID1B 突变富集,显示为可能的耐药标志。
这对患者和临床医生意味着什么
总体而言,该研究表明 T-DXd 在真实世界中是一种有效的治疗选择,尤其适用于肿瘤受 HER2 强烈且持续驱动的患者。但研究也明确指出,传统的 HER2 检测过于粗糙,无法为这一强效药物提供充分的指导。通过在组织和血液上使用更灵敏的测量方法,医生最终可能能够更准确地识别最有可能从 T-DXd 受益的患者,避免对其他患者进行无效治疗,并更好地规划不同抗体-药物偶联物的使用顺序。虽然这些先进检测尚未成为常规并需在更大人群中验证,但它们指向了一个未来:转移性乳腺癌的治疗选择将基于详细的分子画像而非单一的粗略标签。
引用: Tarantino, P., Kim, SE., Hughes, M.E. et al. Quantitative HER2 tissue and plasma profiling predicts the activity of trastuzumab deruxtecan for breast cancer. npj Precis. Onc. 10, 141 (2026). https://doi.org/10.1038/s41698-026-01365-6
关键词: HER2 检测, 曲妥珠单抗艾美妥, 转移性乳腺癌, 液体活检, 抗体-药物偶联物